Содержание
Слайд 2
Все кислоты изменяют окраску индикаторов: лакмус станет красным, метилоранж – розовым,
Все кислоты изменяют окраску индикаторов: лакмус станет красным, метилоранж – розовым,
фенолфталеин – бесцветным, индикаторная бумага – красный.
Кислота+активный Ме=соль + Н2
2HCl+Mg=MgCl2+H2
Кислота+все основания=соль+вода
HCl+KOH=KCl+H2O
Кислота + основный оксид/амфотерный оксид=соль+вода
2HCl+MgO=MgCl2+H2O
2HCl+ZnO=ZnCl2+H2O
Кислота+соль=новая кислота+новая соль
Условия: новая кислота или соль (кто-то один) должен быть М или Н в таблице растворимости.
H2SO4+BaCl2=BaSO4+2HCl
Если образуется H2CO3, то она разлагается на H2O и CO2.
Кислота+активный Ме=соль + Н2
2HCl+Mg=MgCl2+H2
Кислота+все основания=соль+вода
HCl+KOH=KCl+H2O
Кислота + основный оксид/амфотерный оксид=соль+вода
2HCl+MgO=MgCl2+H2O
2HCl+ZnO=ZnCl2+H2O
Кислота+соль=новая кислота+новая соль
Условия: новая кислота или соль (кто-то один) должен быть М или Н в таблице растворимости.
H2SO4+BaCl2=BaSO4+2HCl
Если образуется H2CO3, то она разлагается на H2O и CO2.
Слайд 3
Сборник задач №191, №192, №193, №194
Сборник задач №191, №192, №193, №194


 Титриметрический метод анализа
Титриметрический метод анализа Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною
Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Хімічні явища в побуті
Хімічні явища в побуті Железо и его свойства
Железо и его свойства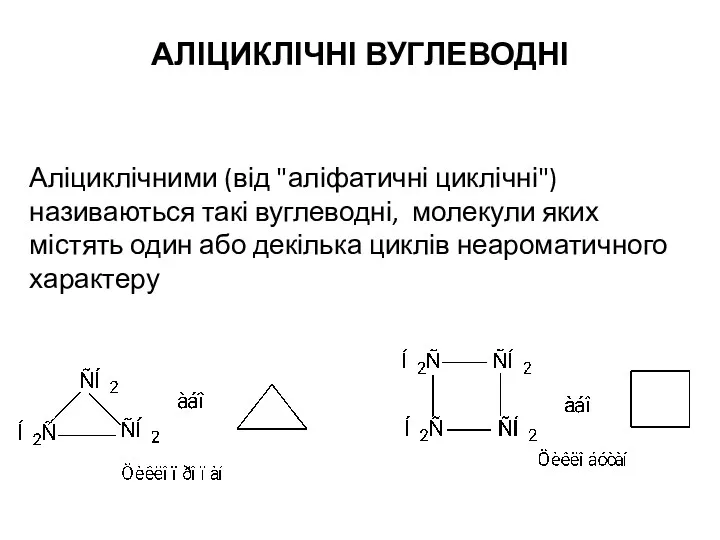 Аліциклічні вуглеводні
Аліциклічні вуглеводні Соединения серы
Соединения серы Соединения кальция. Жесткость воды и способы её устранения
Соединения кальция. Жесткость воды и способы её устранения Конструкционные функциональные волокнистые композиты. Стеклопластики
Конструкционные функциональные волокнистые композиты. Стеклопластики Удивительные свойства воды
Удивительные свойства воды Азотсодержащие органические соединения. Амины. Анилинароматический амин
Азотсодержащие органические соединения. Амины. Анилинароматический амин Романенко
Романенко Извлечение из растворов экстракцией органическими растворителями
Извлечение из растворов экстракцией органическими растворителями Бета-окисление жирных кислот
Бета-окисление жирных кислот Дизельное топливо. Требования, предъявляемые к дизельным топливам
Дизельное топливо. Требования, предъявляемые к дизельным топливам Электронные конфигурации атомов. Периодический Закон. Периодическая система Д.И. Менделеева. Химическая связь
Электронные конфигурации атомов. Периодический Закон. Периодическая система Д.И. Менделеева. Химическая связь 20230416_urok_na_20.02.2023
20230416_urok_na_20.02.2023 Химическая термодинамика. Термохимия
Химическая термодинамика. Термохимия Анализ и синтез химических веществ
Анализ и синтез химических веществ Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас Реконструкция установки получения элементарной серы
Реконструкция установки получения элементарной серы Метод электронного баланса для уравнивания окислительно-восстановительных реакций
Метод электронного баланса для уравнивания окислительно-восстановительных реакций Общие способы получения металлов
Общие способы получения металлов История развития промышленности переработки полимеров
История развития промышленности переработки полимеров Фізичні властивості та хімічний склад природних вод
Фізичні властивості та хімічний склад природних вод Активные формы кислорода. Антиоксиданты их физиологическая роль
Активные формы кислорода. Антиоксиданты их физиологическая роль Геохимия гранитоидов, зоны гипергенеза, осадочного процесса
Геохимия гранитоидов, зоны гипергенеза, осадочного процесса