Содержание
- 2. IVA-группа. Подгруппа углерода. Общая электронная конфигурация валентного уровня: ns2np2 Валентные возможности: II, IV Преимущественные степени окисления:
- 3. IVA-группа. Углерод. Нахождение в природе: Карбонаты Каменный уголь Нефть Алмаз Графит Газ
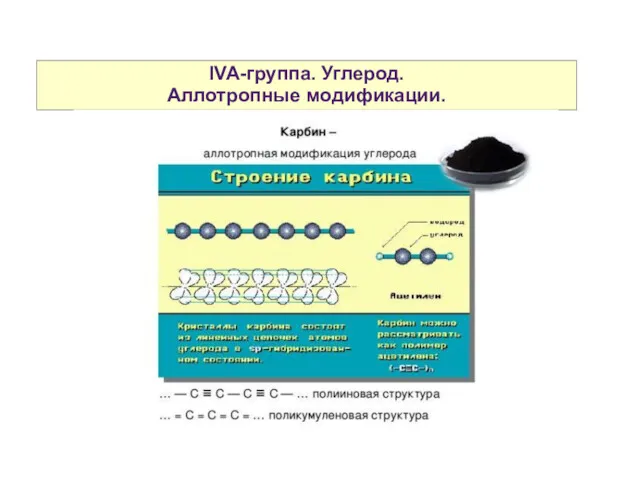
- 4. IVA-группа. Углерод. Аллотропные модификации.
- 5. IVA-группа. Углерод. Аллотропные модификации.
- 6. IVA-группа. Углерод. Аллотропные модификации.
- 7. IVA-группа. Углерод. Аллотропные модификации.
- 8. IVA-группа. Углерод. CO2 и Н2СО3 Кислотный оксид. Взаимодействие с основными оксидами, щелочами, с образованием двух видов
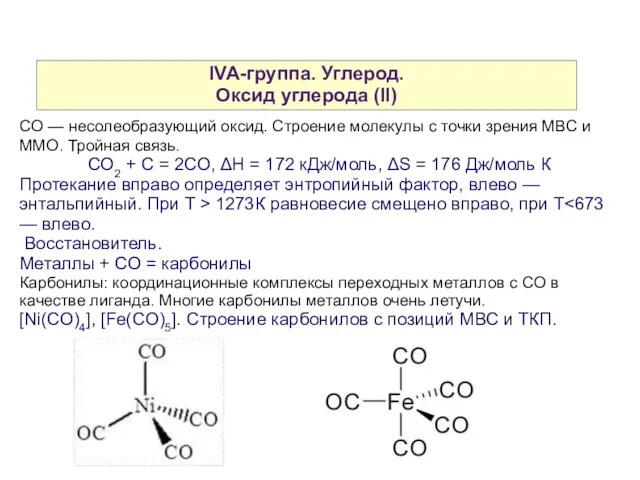
- 9. IVA-группа. Углерод. Оксид углерода (II) CO — несолеобразующий оксид. Строение молекулы с точки зрения МВС и
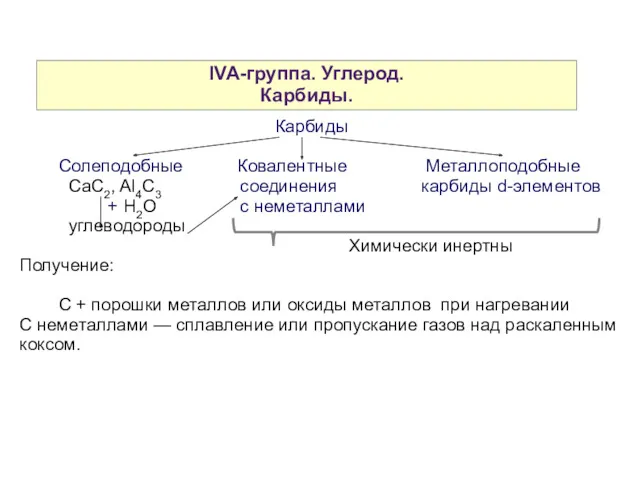
- 10. IVA-группа. Углерод. Карбиды. Карбиды Солеподобные Ковалентные Металлоподобные CaC2, Al4C3 соединения карбиды d-элементов + H2O с неметаллами
- 11. IVA-группа. Кремний. Содержание в земной коре ≈28% по массе. Второе место после кислорода. В основном в
- 12. IVA-группа. Кремний. При комн температуре реагирует только со фтором. Медленно — с хлором и растворами щелочей.
- 13. IVA-группа. Кремний. Cоединения кремния. Силаны. Силаны (кремневодороды, гидриды кремния) — соединения кремния с водородом общей формулы
- 14. IVA-группа. Кремний. Бинарные соединения кремния +4 Si (IV) входит в соединения с галогенами, кислородом, серой, азотом,
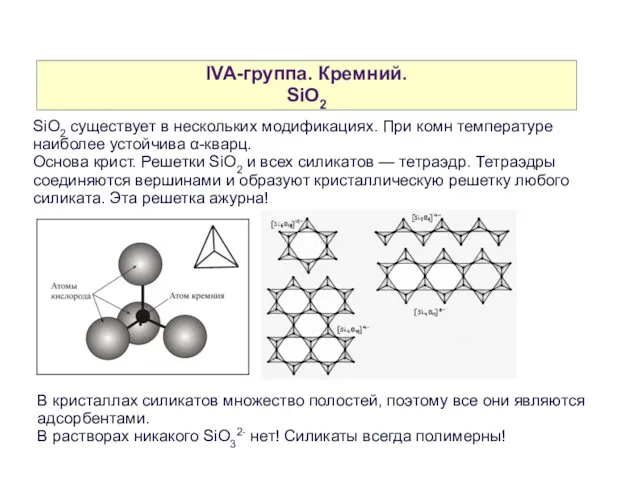
- 15. IVA-группа. Кремний. SiO2 SiO2 существует в нескольких модификациях. При комн температуре наиболее устойчива α-кварц. Основа крист.
- 16. IVA-группа. Кремний. SiO2 При комн температуре на SiO2 действуют только HF и щелочи: H2[SiF6] и силикаты.
- 17. IVA-группа. Подгруппа германия. Ge, Sn, Pb. Тенденция: при движении вниз по подгруппе, низшая положительная степень окисления
- 18. IVA-группа. Подгруппа германия. E°(Ge2+/Ge) = 0B E°(Sn2+/Sn) = -0,14B E°(Pb2+/Pb) = -0,13B Каково отношение к минеральным
- 19. IVA-группа. Подгруппа германия. Sn и Pb амфотерны. Растворяются в щелочах и сплавляются с ними, вытесняя водород:
- 20. IVA-группа. Подгруппа германия. Водородные соединения можно получить лишь косвенно (не в лоб): Mg2Ge + 4 HCl
- 21. IVA-группа. Подгруппа германия. Дигалогениды: Ge + GeCl4 = 2GeCl2 нагревание Sn + 2HCl = SnCl2 +
- 22. IVA-группа. Подгруппа германия. Оксиды этих элементов можно получить термическим разложением соответствующих гидроксидов: Э(ОН)2 => ЭО +
- 23. VA-группа. Азот N2 — ¾ земной атмосферы Ежегодно выносится с урожаем из почвы ≈100 млн.т. Промышленное
- 24. VA-группа. Азот. Нитриды. При высоких температурах азот окисляет многие металлы и неметаллы, образуя нитриды: 3Mg +
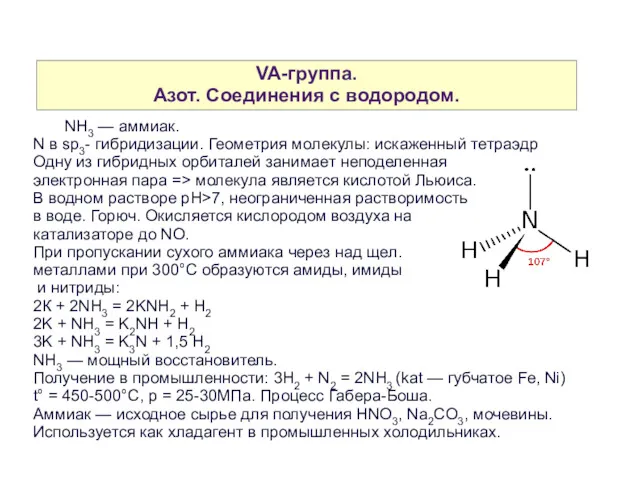
- 25. VA-группа. Азот. Cоединения с водородом. NH3 — аммиак. N в sp3- гибридизации. Геометрия молекулы: искаженный тетраэдр
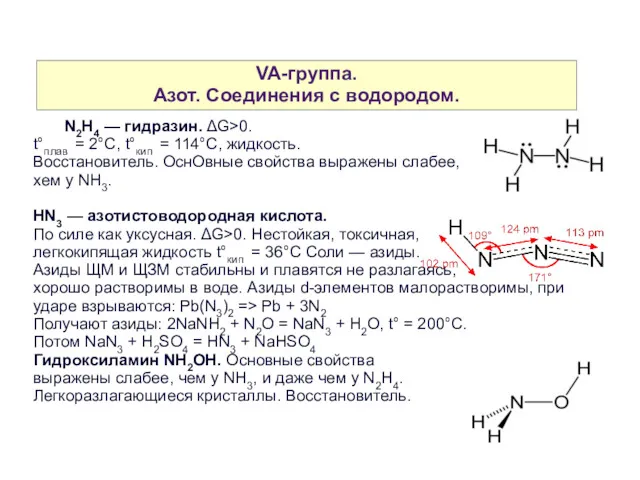
- 26. VA-группа. Азот. Cоединения с водородом. N2H4 — гидразин. ΔG>0. t°плав = 2°C, t°кип = 114°C, жидкость.
- 27. VA-группа. Азот. Кислородные соединения. .
- 28. VA-группа. Азот. Азотная кислота. HNO3 — одна из самых сильных кислот, сильнейший окислитель. t°плав = -42°C,
- 29. VA-группа. Фосфор. Валентность: III, IV Степени окисления: -3, 0, +3, +5 В отличие от азота sp-
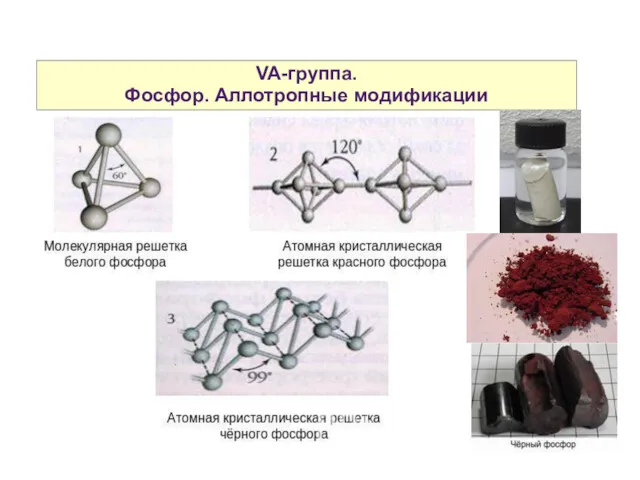
- 30. VA-группа. Фосфор. Аллотропные модификации
- 31. VA-группа. Фосфор. Нахождение в природе.
- 32. VA-группа. Фосфор. Фосфор-восстановитель: с кислородом, галогенами, серой. При недостатке окислителя получаются соединения фосфора (III): P2O3, PCl3,
- 33. VA-группа. Фосфор. Фосфор-восстановитель: с кислородом, галогенами, серой. При недостатке окислителя получаются соединения фосфора (III): P2O3, PCl3,
- 34. VA-группа. Фосфор. Галогениды. Известны два ряда галогенидов фосфора — производные трехвалентного и пятивалентного фосфора. Получение: прямое
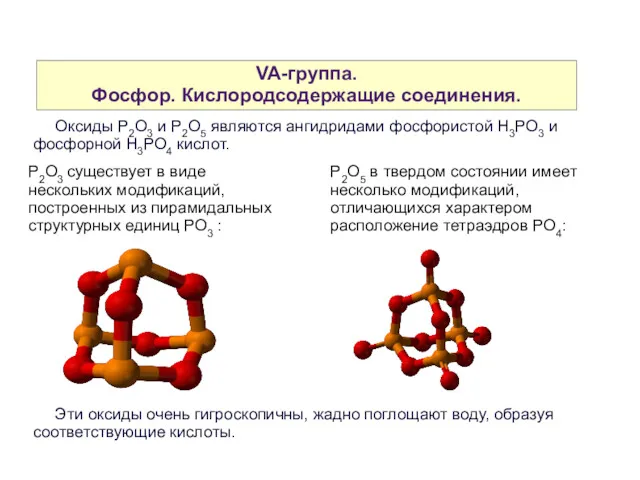
- 35. VA-группа. Фосфор. Кислородсодержащие соединения. Оксиды P2O3 и P2O5 являются ангидридами фосфористой Н3РО3 и фосфорной Н3РО4 кислот.
- 36. VA-группа. Фосфор. Кислородсодержащие соединения. Фосфорноватисная кислота H3PO2 — одноосновная кислота средней силы. Хорошо растворимые в воде
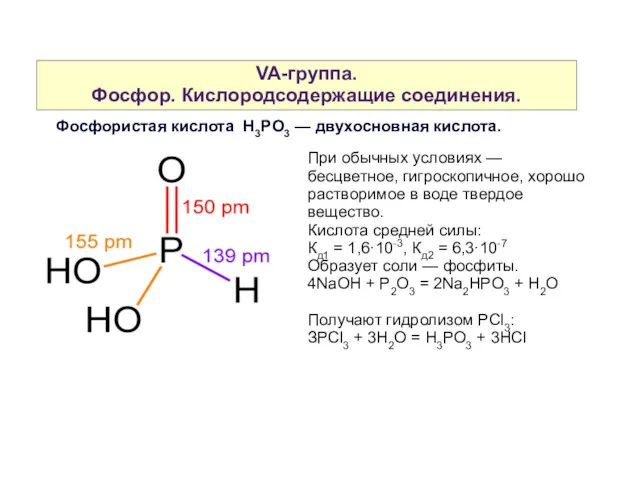
- 37. VA-группа. Фосфор. Кислородсодержащие соединения. Фосфористая кислота H3PO3 — двухосновная кислота. При обычных условиях — бесцветное, гигроскопичное,
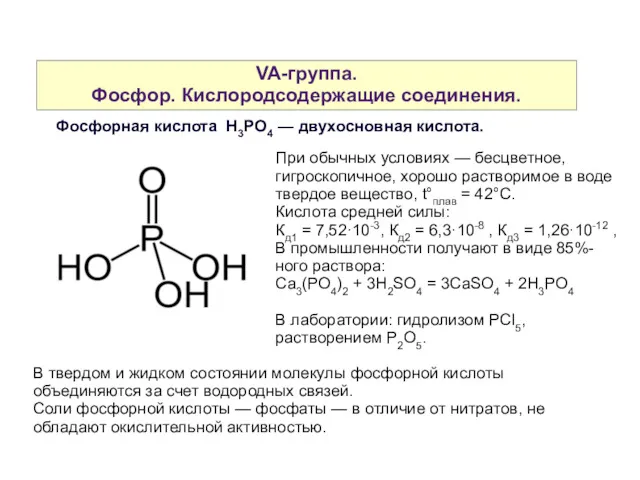
- 38. VA-группа. Фосфор. Кислородсодержащие соединения. Фосфорная кислота H3PO4 — двухосновная кислота. При обычных условиях — бесцветное, гигроскопичное,
- 39. VA-группа. Фосфор. Кислородсодержащие соединения. Все три кислоты обладают примерно равной силой, во всех этих кислотах и
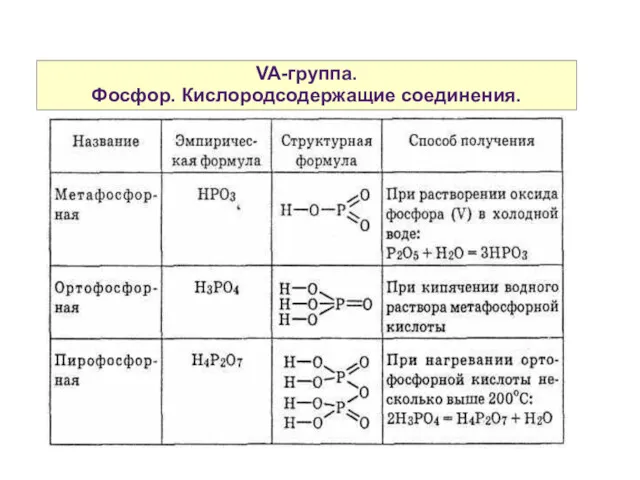
- 40. VA-группа. Фосфор. Кислородсодержащие соединения.
- 41. VA-группа. Подгруппа мышьяка. Мышьяк As, сурьма Sb, висмут Bi. Полные электронные аналоги с конфигурацией s2p3. В
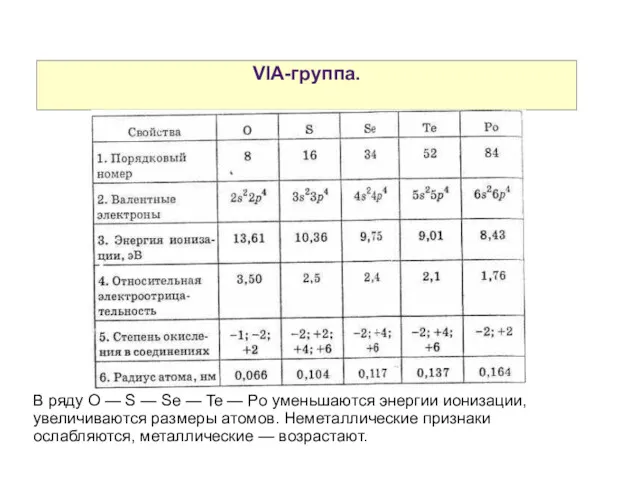
- 42. VIA-группа. В ряду O — S — Se — Te — Po уменьшаются энергии ионизации, увеличиваются
- 43. VIA-группа. В ряду O — S — Se — Te — Po уменьшаются энергии ионизации, увеличиваются
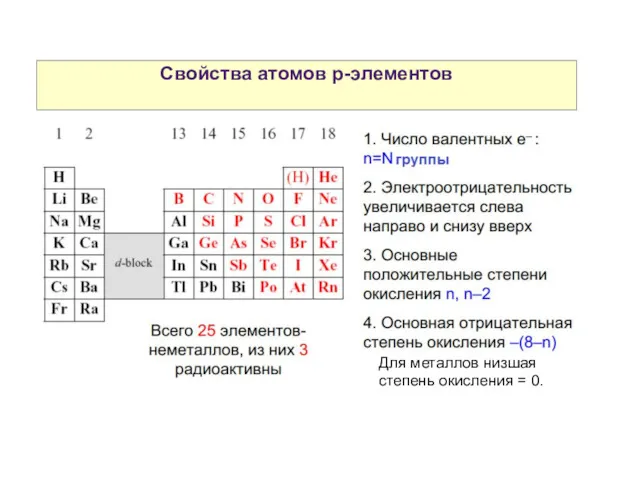
- 44. Свойства атомов р-элементов Для металлов низшая степень окисления = 0.
- 46. Скачать презентацию






























 Химия в организме человека
Химия в организме человека Поделочные камни
Поделочные камни Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Электроотрицательность химических элементов
Электроотрицательность химических элементов Химические реакции
Химические реакции Твердое состояние вещества. Кристаллические и аморфные тела
Твердое состояние вещества. Кристаллические и аморфные тела Основные классы неорганических соединений
Основные классы неорганических соединений Степень окисления
Степень окисления Бальзам-ополаскиватель для волос
Бальзам-ополаскиватель для волос Химиялық реакциялардың типтері
Химиялық реакциялардың типтері Конструкционные материалы. Пластмассы
Конструкционные материалы. Пластмассы Нахождение массовой доли
Нахождение массовой доли Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Химические свойства оснований, кислот и солей в свете теории электролитической диссоциации
Химические свойства оснований, кислот и солей в свете теории электролитической диссоциации Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Реакции ионного обмена
Реакции ионного обмена Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Форми періодичної системи хімічних елементів
Форми періодичної системи хімічних елементів Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Подготовка обучающихся к выполнению заданий КИМ ЕГЭ по химии при изучении темы Гидролиз
Подготовка обучающихся к выполнению заданий КИМ ЕГЭ по химии при изучении темы Гидролиз Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Бұл суреттерді не біріктіреді деп ойлайсыздар?
Бұл суреттерді не біріктіреді деп ойлайсыздар? Функциональные производные с простой связью C-“Э”. Часть 2. Галогенпроизводные
Функциональные производные с простой связью C-“Э”. Часть 2. Галогенпроизводные Сера. Нахождение в природе. Химические свойства серы
Сера. Нахождение в природе. Химические свойства серы Мінеральні добрива
Мінеральні добрива Аммиак. Состав. Строение
Аммиак. Состав. Строение серная кислота и ее соли 9 класс
серная кислота и ее соли 9 класс