Содержание
- 2. Степень окисления – это условный заряд атомов х.э. в соединении, вычисленный на основе предположения, что все
- 3. СО атомов в простых веществах равна нулю 0 0 0 0 0 Al H2 F2 Ca
- 4. С.О. кислорода всегда равна «-2» Исключение: +1 -1 пероксиды H2O2 +2 -1 фторид кислорода OF2 запомните
- 5. C.О. водорода всегда равна «+1» Исключение: гидриды металлов +1 -1 +2 -1 +3 -1 NaH CaH2
- 6. Металлы в соединениях всегда имеют положительное значение степени окисления С.О. металлов главных подгрупп численно равна номеру
- 7. В соединениях сумма значений положительных и отрицательных степеней окисления равна нулю +3 -2 Al2O3 (+3)*2 +
- 8. Бинарные соединения Бинарные соединения – это соединения, в состав которых входят атомы двух х.э. (би –
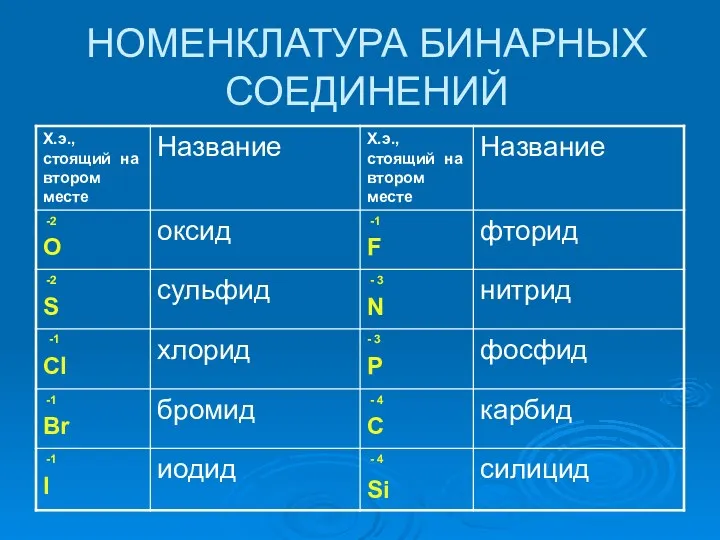
- 9. НОМЕНКЛАТУРА БИНАРНЫХ СОЕДИНЕНИЙ
- 10. Определение степени окисления в бинарных соединениях В бинарных соединениях С.О. х.э., стоящего на втором месте, находим
- 11. Если атом одного х.э. может принимать несколько значений С.О., в названии указывают С.О. римскими цифрами в
- 12. Как вы думаете, можно ли составить формулу вещества, зная степени окисления химических элементов, из которых состоит
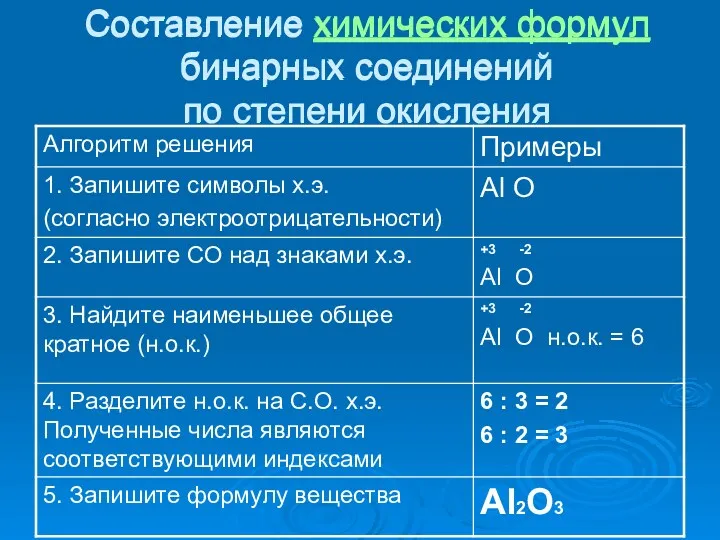
- 13. Составление химических формул бинарных соединений по степени окисления (алгоритм) 1. Запишите символы х.э. (согласно электроотрицательности) 2.
- 14. Составление химических формул бинарных соединений по степени окисления Составление химических формул бинарных соединений по степени окисления
- 15. ЗАДАНИЕ 1. Расставьте степени окисления, составьте формулы: Оксид углерода (II) Оксид углерода (IV) Хлорид кальция Сульфид
- 18. Скачать презентацию













 Элемент V группы фосфор
Элемент V группы фосфор Первичная переработка нефти
Первичная переработка нефти Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Железо
Железо Основные классы неорганических соединений
Основные классы неорганических соединений Нуклеопротеины
Нуклеопротеины Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Оксиды неметаллов и кислородсодержащие кислоты. 11 класс
Оксиды неметаллов и кислородсодержащие кислоты. 11 класс Фазовые равновесия в системе ограниченно смешивающихся жидкостей
Фазовые равновесия в системе ограниченно смешивающихся жидкостей Реакции ионного обмена
Реакции ионного обмена Спирты. Физические и химические свойства
Спирты. Физические и химические свойства Алкалоиды, производные тропана
Алкалоиды, производные тропана Титриметрический метод анализа
Титриметрический метод анализа Figure
Figure Урок 25
Урок 25 Лекция 8.3. Реакции окисления и восстановления органических соединений
Лекция 8.3. Реакции окисления и восстановления органических соединений Халькогены. Кислород
Халькогены. Кислород Химические свойства кислот в свете теории электролитической диссоциации
Химические свойства кислот в свете теории электролитической диссоциации Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Кристаллические решетки
Кристаллические решетки Создание слоев пористого кремния на p-Si
Создание слоев пористого кремния на p-Si Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Химическая связь
Химическая связь Chemistry th 11 grade The end of second Term
Chemistry th 11 grade The end of second Term Методика изучения современной теории строения как фундамента курса органической химии в старшей школе
Методика изучения современной теории строения как фундамента курса органической химии в старшей школе Производные пиримидина
Производные пиримидина Синтез олиголактозаминов – лигандов галектинов
Синтез олиголактозаминов – лигандов галектинов