Содержание
- 2. Электронная формула, степени окисления 1S22S22p63S23p3 -3 , 0 , +3 , +5 Открытие фосфора: Х.Бранд (1669г.)
- 3. Картина Джозефа Райта «Алхимик, открывающий фосфор» предположительно описывающая открытие фосфора Хеннигом Брандом, 1771 год.
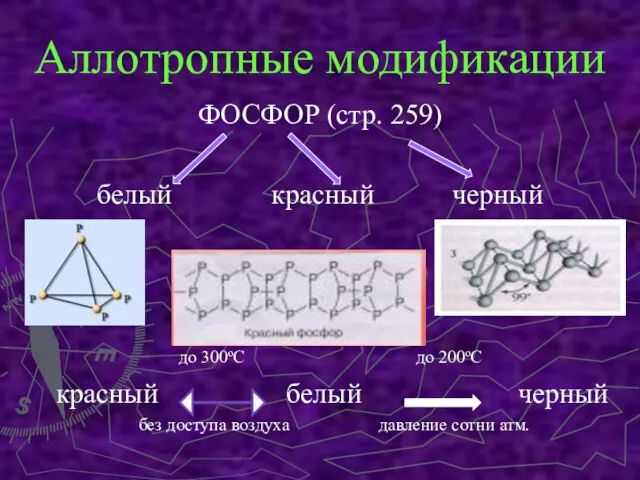
- 4. Аллотропные модификации ФОСФОР (стр. 259) белый красный черный до 300оС до 200оС красный белый черный без
- 6. Аллотропные модификации Белый фосфор (Р4) – молекулярная кристал-лическая решетка, летуч, пластичен, ядовит, светится в темноте свечение
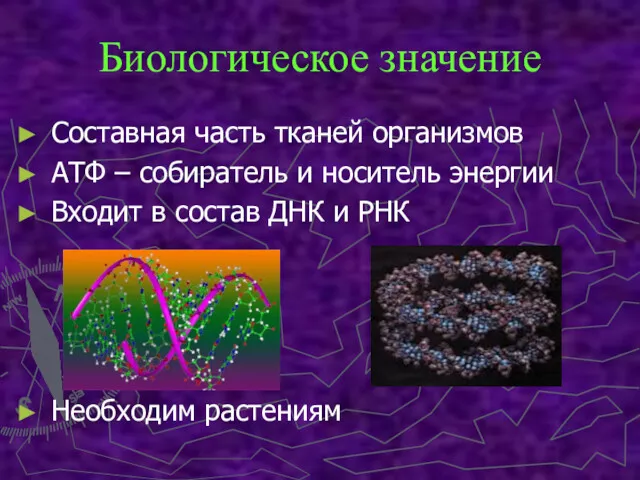
- 7. Биологическое значение Составная часть тканей организмов АТФ – собиратель и носитель энергии Входит в состав ДНК
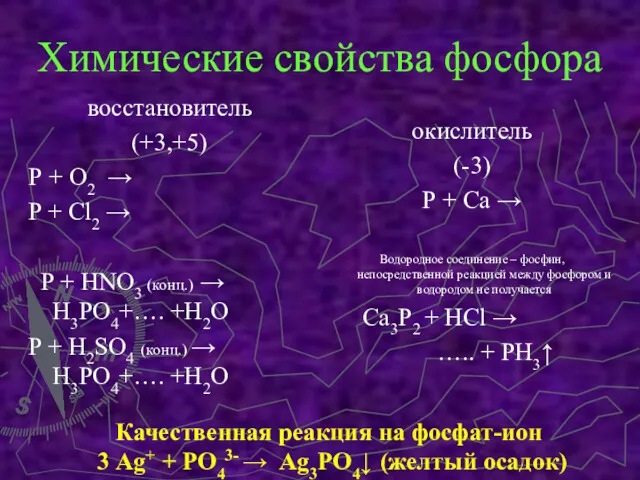
- 8. Химические свойства фосфора восстановитель (+3,+5) Р + О2 → P + Cl2 → P + HNO3
- 9. Применение фосфора Производство спичек (в головке спички) Водоотнимающее средство (Р2О5) Производство ядохимикатов (дихлофос) Для создания дымовых
- 10. Установить соответствие а) P2O5 б) H3PO3 в) K3PO4 г) H3PO4 д) PH3 е) P2O3 1. -
- 11. Найти соответствие а) P2O5 б) H3PO3 в) K3PO4 г) H3PO4 д) PH3 е) KH2PO4 1.Фосфин 2.Фосфат
- 13. Скачать презентацию







 Хімічні формули речовин
Хімічні формули речовин Водород
Водород Химиялық қауіптілер. Нитраттар
Химиялық қауіптілер. Нитраттар Кислоты в свете теории электролитической диссоциации (ТЭД)
Кислоты в свете теории электролитической диссоциации (ТЭД) Кристаллическое строение и свойства металлов
Кристаллическое строение и свойства металлов Материаловедение промышленного производства. Особенности строения твердых тел
Материаловедение промышленного производства. Особенности строения твердых тел Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника
Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника Химия в Великую Отечественную войну
Химия в Великую Отечественную войну Массовая доля вещества в растворе
Массовая доля вещества в растворе Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Современные химические технологии
Современные химические технологии Каталитический риформинг
Каталитический риформинг Получение, собирание, распознавание газов. (Практическая работа 2)
Получение, собирание, распознавание газов. (Практическая работа 2) Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы
Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы Простые вещества
Простые вещества Незвичайна вода
Незвичайна вода Фазовое равновесие
Фазовое равновесие Химия в повседневной жизни человека
Химия в повседневной жизни человека Химическая очистка сточных вод. Окисление и восстановление
Химическая очистка сточных вод. Окисление и восстановление Растворы: состав и их коллигативные свойства
Растворы: состав и их коллигативные свойства Щелочные и щелочноземельные металлы
Щелочные и щелочноземельные металлы Относительная молекулярная масса вещества. Задачи
Относительная молекулярная масса вещества. Задачи Химические свойства карбокатионов
Химические свойства карбокатионов Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Скорость химических реакций
Скорость химических реакций