Изучение физико-химических свойств мицеллярных растворов индивидуальных ПАВ, композиций различных ПАВ презентация
Содержание
- 2. Кафедра коллоидной химии им. С.С. Воюцкого 2 Цель дисциплины Целью учебной дисциплины «Коллоидная химия ПАВ» является
- 3. имеющие дифильное (амфифильное строение) от греческого слова «ampfi», «оба» Гидрофобная часть молекулы ПАВ может быть линейной
- 4. Лекция 1: Введение в химию поверхностно-активных веществ 4 Природные ПАВ К ПАВ природного происхождения прежде всего
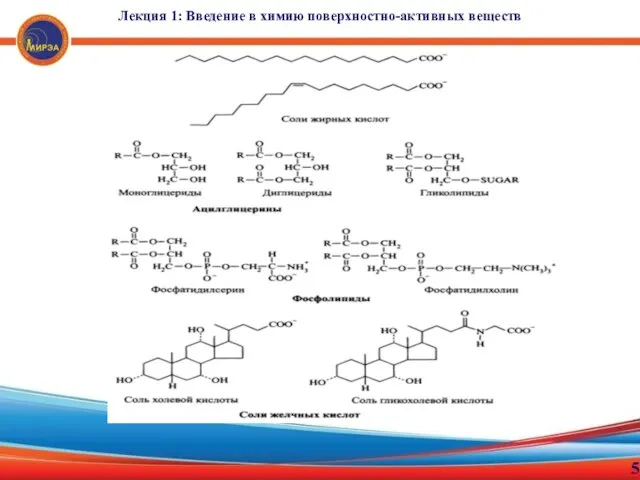
- 5. Лекция 1: Введение в химию поверхностно-активных веществ 5
- 6. Лекция 1: Введение в химию поверхностно-активных веществ 6 ОЛЕОХИМИЧЕСКИЕ (источник сырья – растительные масла) Производят из
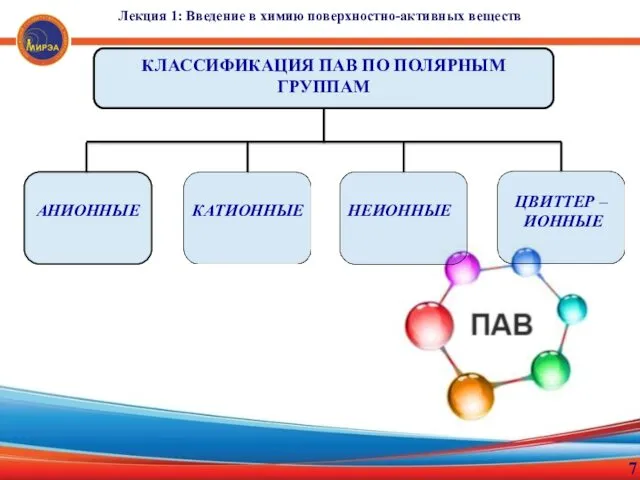
- 7. Лекция 1: Введение в химию поверхностно-активных веществ 7 АНИОННЫЕ КЛАССИФИКАЦИЯ ПАВ ПО ПОЛЯРНЫМ ГРУППАМ КАТИОННЫЕ НЕИОННЫЕ
- 8. Лекция 1: Введение в химию поверхностно-активных веществ 8 Анионными ПАВ (АПАВ) называют вещества, содержащие в молекуле
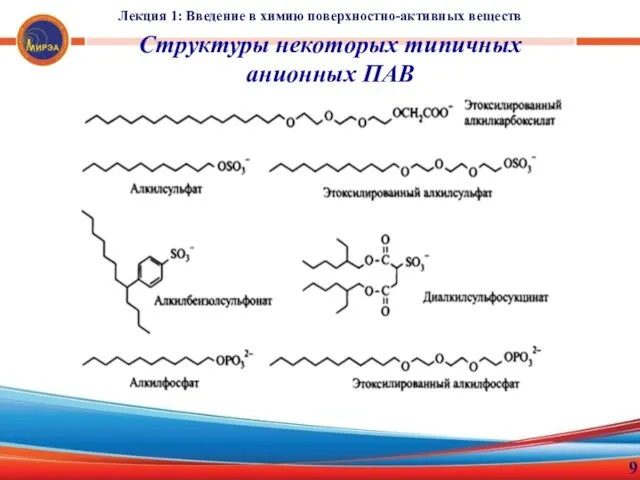
- 9. Лекция 1: Введение в химию поверхностно-активных веществ 9 Структуры некоторых типичных анионных ПАВ
- 10. Лекция 1: Введение в химию поверхностно-активных веществ 10 Соли карбоновых кислот (мыла) и их синтез Суммарная
- 11. Лекция 1: Введение в химию поверхностно-активных веществ 11 Алкилсульфаты Получение первичных алкилсульфатов и алкилэтоксисульфатов осуществляют путем
- 12. Лекция 1: Введение в химию поверхностно-активных веществ 12 Алкиларилсульфонаты Алкиларилсульфонаты представляют собой продукт сульфирования алкилароматических углеводородов.
- 13. Лекция 1: Введение в химию поверхностно-активных веществ 13 Получение алкилароматических углеводородов Хлоралканы получают путем хлорирования фракций
- 14. Лекция 1: Введение в химию поверхностно-активных веществ 14 Сульфирование алкилароматических углеводородов осуществляют: олеумом, триоксидом серы, хлорсульфоновой
- 15. Лекция 1: Введение в химию поверхностно-активных веществ 15 Алкилсульфонаты . Алкилсульфонаты обычно получают в виде смесей
- 16. Лекция 1: Введение в химию поверхностно-активных веществ 16 Фосфат - содержащие ПАВ . Фосфат – содержащие
- 17. Лекция 1: Введение в химию поверхностно-активных веществ 17 Важнейшие сведения об анионных ПАВ .
- 18. Лекция 1: Введение в химию поверхностно-активных веществ 18 Катионные ПАВ Катионными ПАВ (КПАВ) называют такие вещества,
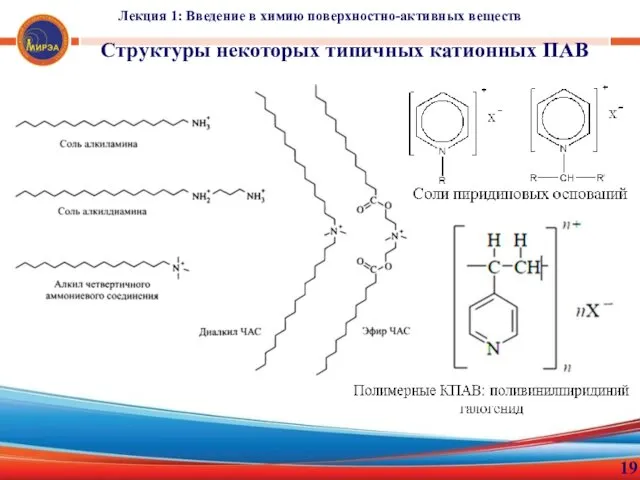
- 19. Лекция 1: Введение в химию поверхностно-активных веществ 19 Структуры некоторых типичных катионных ПАВ
- 20. Лекция 1: Введение в химию поверхностно-активных веществ 20 Синтез катионных ПАВ Синтез неэфирных четвертичных аммониевых ПАВ
- 21. Лекция 1: Введение в химию поверхностно-активных веществ 21 Четвертичные аммониевые соединения обычно получают из третичных аминов
- 22. Лекция 1: Введение в химию поверхностно-активных веществ 22 Применение катионных ПАВ, обусловленное их адсорбцией на поверхностях.
- 23. Лекция 1: Введение в химию поверхностно-активных веществ 23 Важнейшие сведения о катионных ПАВ
- 24. Лекция 1: Введение в химию поверхностно-активных веществ 24 Цвиттер – ионные ПАВ Цвиттер – ионные ПАВ
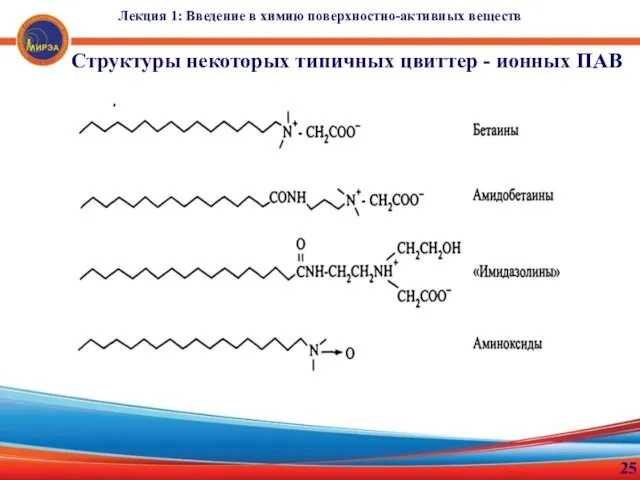
- 25. Лекция 1: Введение в химию поверхностно-активных веществ 25 Структуры некоторых типичных цвиттер - ионных ПАВ
- 26. Лекция 1: Введение в химию поверхностно-активных веществ 26 Полимерные амфотерные ПАВ 1) природные, к которым относят
- 27. Лекция 1: Введение в химию поверхностно-активных веществ 27 Синтез цвиттер - ионных ПАВ Наиболее распространенный тип
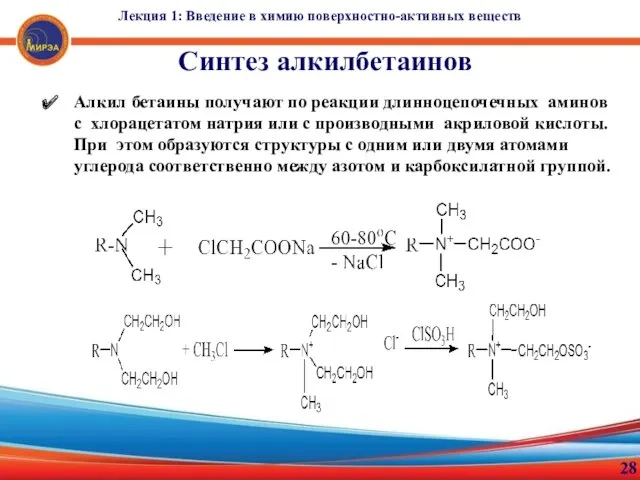
- 28. Лекция 1: Введение в химию поверхностно-активных веществ 28 Синтез алкилбетаинов Алкил бетаины получают по реакции длинноцепочечных
- 29. Лекция 1: Введение в химию поверхностно-активных веществ 29 Важнейшие сведения о цвиттер – ионных ПАВ
- 30. Лекция 1: Введение в химию поверхностно-активных веществ 30 Неионные ПАВ Неионные ПАВ (НПАВ) имеют общую формулу:
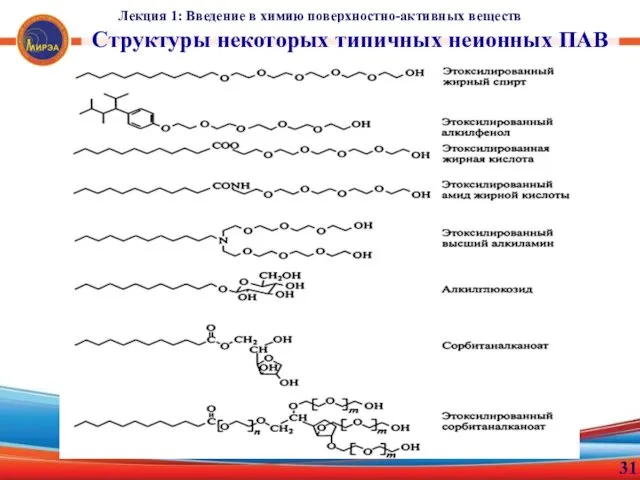
- 31. Лекция 1: Введение в химию поверхностно-активных веществ 31 Структуры некоторых типичных неионных ПАВ
- 32. Лекция 1: Введение в химию поверхностно-активных веществ 32 Важнейшие сведения о неионных ПАВ
- 33. Лекция 1: Введение в химию поверхностно-активных веществ 33 Фторуглеродные ПАВ Гидрофобная часть имеет формулу Сn F2n
- 34. Лекция 1: Введение в химию поверхностно-активных веществ 34 Фторуглеродные ПАВ обладают при одинаковом числе атомов углерода
- 35. Лекция 1: Введение в химию поверхностно-активных веществ 35 Синтез фторуглеродных ПАВ Синтез перфторалкильной цепи проводят путем
- 36. Лекция 1: Введение в химию поверхностно-активных веществ 36 Важнейшие сведения о фторуглеродных ПАВ
- 38. Скачать презентацию




























 Щелочные металлы
Щелочные металлы Аллотропные модификации углерода. Алмазы
Аллотропные модификации углерода. Алмазы Закон сохранения массы веществ. Уравнения химических реакций
Закон сохранения массы веществ. Уравнения химических реакций Различные теории кислот и оснований
Различные теории кислот и оснований Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Параметры токсичности продуктов горения материала. (Задача 3)
Параметры токсичности продуктов горения материала. (Задача 3) Эндогенная серия. Альбитит-грейзеновая группа
Эндогенная серия. Альбитит-грейзеновая группа Натуральный каучук
Натуральный каучук Валентность химического элемента. Определение валентности по химической формуле
Валентность химического элемента. Определение валентности по химической формуле Rate of reactions. (Chapter 2)
Rate of reactions. (Chapter 2)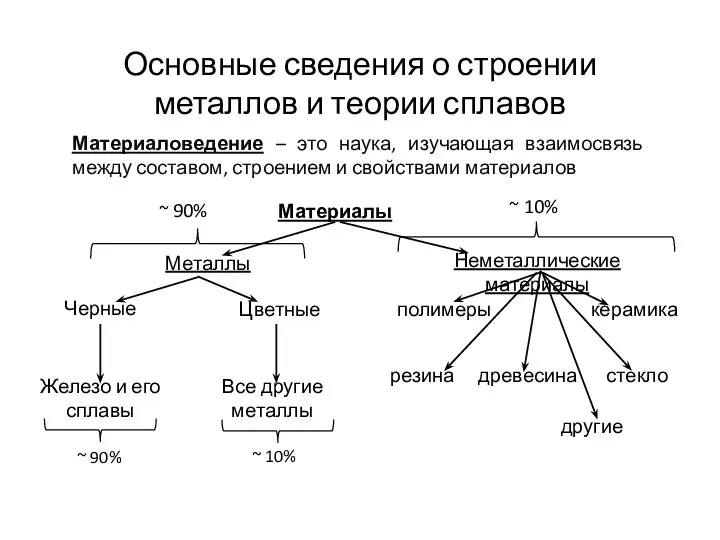 Основные сведения о строении металлов и теории сплавов
Основные сведения о строении металлов и теории сплавов Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Магматизм. (Лекция 6)
Магматизм. (Лекция 6) Типы химических реакций
Типы химических реакций Углерод и его соединения
Углерод и его соединения Растворы. Лекция №5
Растворы. Лекция №5 Висмут, ртуть, сурьма
Висмут, ртуть, сурьма Аналітична хімія. Лекція 1
Аналітична хімія. Лекція 1 Si - Silicon. Distribute Properties
Si - Silicon. Distribute Properties Непредельные углеводороды
Непредельные углеводороды Калийные удобрения
Калийные удобрения Химия нефти и газа. Переработка нефти
Химия нефти и газа. Переработка нефти Electrolysis
Electrolysis Минералогия. Формы нахождения минералов в природе. Свойства минералов
Минералогия. Формы нахождения минералов в природе. Свойства минералов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Получение и применение радиоактивных изотопов
Получение и применение радиоактивных изотопов Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)
Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13) Твёрдое агрегатное состояние. Кристалические решетки. Урок 4
Твёрдое агрегатное состояние. Кристалические решетки. Урок 4