Слайд 2
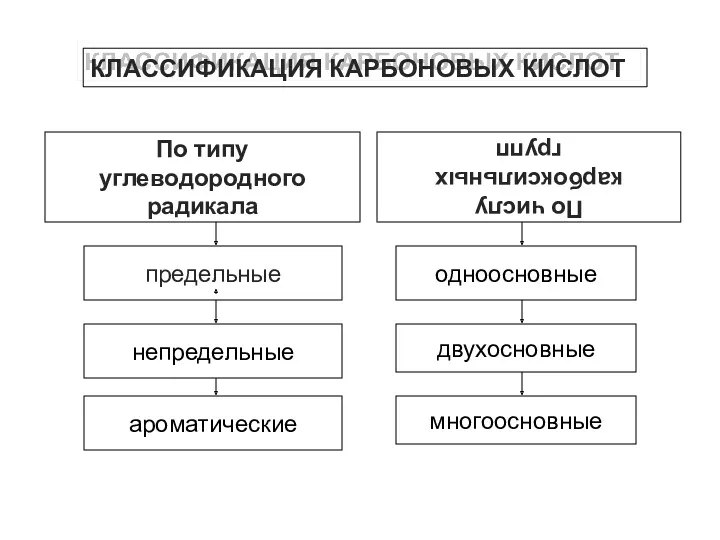
КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ
По числу карбоксильных
групп
непредельные
ароматические
одноосновные
двухосновные
многоосновные
предельные
По типу углеводородного
радикала
Слайд 3

ОБЩАЯ ФОРМУЛА ОДНООСНОВНЫХ КИСЛОТ ПРЕДЕЛЬНОГО РЯДА
СnH2n+1COOН
где n может быть равно нулю.
Слайд 4

Слайд 5

Физические свойства
Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в
воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой (н-нонановой) СН3-(СН2)7-СООН, — твердые вещества, без запаха, нерастворимые в воде. Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота.
Слайд 6

Характерные химические реакции
Наиболее важные химические свойства, характерные для большинства карбоновых кислот:
1)
Карбоновые кислоты при реакции с металлами или их осно́вными гидроксидами дают соли соответствующих металлов:
Также карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
(потом разлагается на углекислый газ и воду)
2) Карбоновые кислоты в присутствии кислого катализатора 2) Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
CH3COOH + СН3СН2ОН = CH3COOCH2СН3 + H2O
Слайд 7
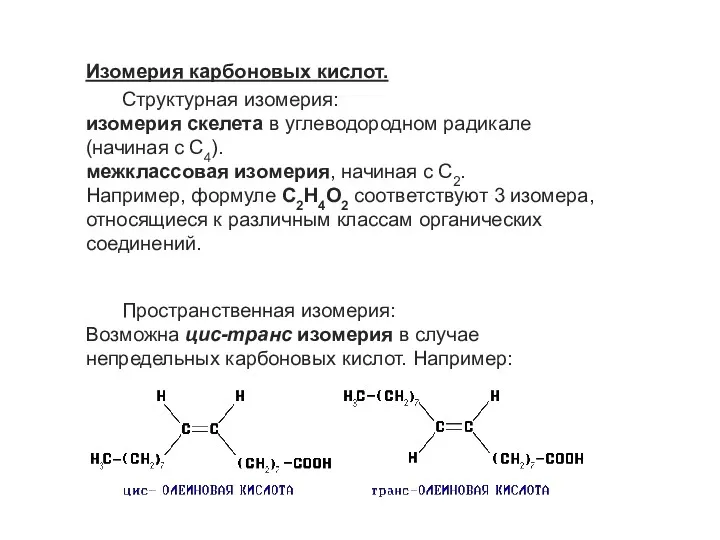
Изомерия карбоновых кислот.
Cтруктурная изомерия:
изомерия скелета в углеводородном радикале (начиная с C4).
межклассовая изомерия, начиная с C2.
Например, формуле C2H4O2 соответствуют 3 изомера, относящиеся к различным классам органических соединений.
Пространственная изомерия:
Возможна цис-транс изомерия в случае непредельных карбоновых кислот. Например:
Слайд 8
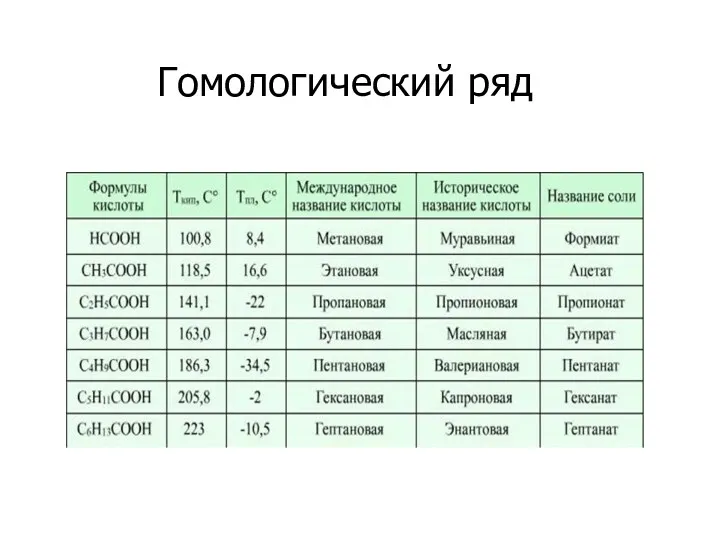







 Состояние и свойства воды
Состояние и свойства воды Нефть и ее роль в мировой экономике
Нефть и ее роль в мировой экономике Химическая кинетика
Химическая кинетика Релаксационные процессы в полимерах
Релаксационные процессы в полимерах Минералы для ИЗБ
Минералы для ИЗБ Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды Запалювання нагрітим тілом та електричним розрядом
Запалювання нагрітим тілом та електричним розрядом Химические методы синтеза наночастиц
Химические методы синтеза наночастиц Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Окислительно- восстановительные реакции
Окислительно- восстановительные реакции Морские льды. Их классификация и закономерности движения
Морские льды. Их классификация и закономерности движения Химические реакции. Реакции разложения
Химические реакции. Реакции разложения Окисно-відновні реакції. Гальванічні елементи
Окисно-відновні реакції. Гальванічні елементи Полипропилен. Области применения полипропилена
Полипропилен. Области применения полипропилена Серная кислота. Занимательные опыты
Серная кислота. Занимательные опыты Проектная работа. Косметика своими руками
Проектная работа. Косметика своими руками Водород. Положение в периодической системе
Водород. Положение в периодической системе Магний. Электронное строение атома Mg
Магний. Электронное строение атома Mg Закон сохранения массы веществ
Закон сохранения массы веществ Химическая кинетика. Катализ. Химическое равновесие
Химическая кинетика. Катализ. Химическое равновесие Ерiтiндiлер туралы iлiм. Сұйытылған бейэлектролит және электролит ерiтiнндiлерiнiң коллигативтiк қасиеттерi
Ерiтiндiлер туралы iлiм. Сұйытылған бейэлектролит және электролит ерiтiнндiлерiнiң коллигативтiк қасиеттерi Химия и сельское хозяйство
Химия и сельское хозяйство Дисперсные системы
Дисперсные системы Застосування радіонуклідів у медицині, тваринництві та археології
Застосування радіонуклідів у медицині, тваринництві та археології Азо-, диазосоединения
Азо-, диазосоединения Инертные газы
Инертные газы Природные и синтетические полимеры
Природные и синтетические полимеры