Слайд 2

.
Вода
Сложное вещество, состоящее из двух химических элементов. Является оксидом.
Слайд 3

.
Молекулярная формула воды
Формула воды - Н2О
В молекуле воды:
2 атома водорода;
1
атом кислорода;
Относительная молекулярная масса (Mr) = 18
Слайд 4
Типы химических реакций воды
Реакция разложения
Реакция соединения
Реакция замещения
Реакция обмена
Слайд 5

Реакция разложения
.
Электролиз воды – разложение молекулы воды под действием электрического
тока.
2H2O 2H2 + O2
Слайд 6
.
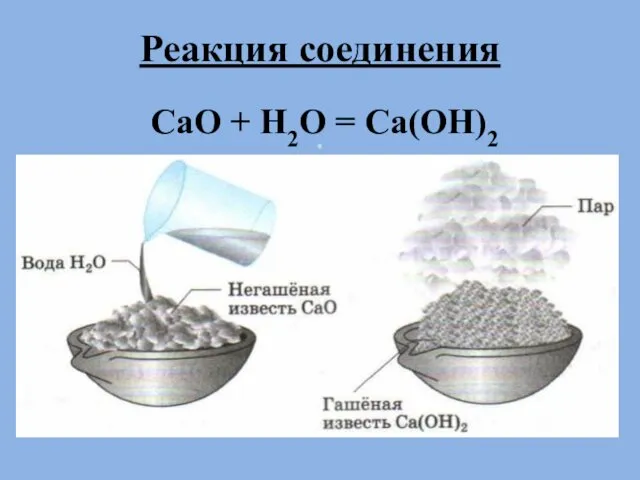
Реакция соединения
CaO + H2O = Ca(OH)2
Слайд 7

.
Реакция соединения
Правило: вода реагирует с оксидами металлов в том случае, если
образуется растворимое вещество (щелочь).
Li2O + H2O = 2LiOH - щелочь
FeO + H2O = реакция не идет,
т.к. не образуется растворимого соединения
Слайд 8

.
Реакция соединения
Правило: вода реагирует с оксидами неметаллов в том случае, если
образуется растворимое вещество (кислородсодержащая кислота).
SO3 + H2O = H2SO4 – растворимая кислота
SiO2 + H2O = реакция не идет, т.к. не образуется растворимого соединения
Слайд 9

.
Реакция замещения
2Na + 2H2O = 2NaOH + H2
Слайд 10

.
Реакция обмена
Гидролиз – обменное взаимодействие веществ с водой, приводящее к их
разложению.
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
CaC2 + 2H2O = C2H2 + Ca(OH)2
Слайд 11

.
Обобщение темы
«Проверь себя»
1) Гидролиз - это:
а) реакция разложения
б) реакция обмена
в)реакция
замещения
2) Молекулярная формула воды состоит из:
а) два атома кислорода и один атом водорода
б) один атом водорода и один атом кислорода
в) два атома водорода и один атом кислорода
3) С каким оксидом вода не реагирует:
а) CaO
б) FeO
в) SO3
Слайд 12

ПРАВИЛЬНО
Вернуться к вопросу
.
Слайд 13

НЕПРАВИЛЬНО
Вернуться к вопросу
Слайд 14

Домашнее задание:
§ 33, упр. 1, 2.













 Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии
Анри Ле Шателье. 1850-1963. Принцип Ле Шателье в химии Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде
Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде Химический элемент: йод
Химический элемент: йод Полисахариды. Крахмал
Полисахариды. Крахмал Почва. Интегрированный урок по химии и географии
Почва. Интегрированный урок по химии и географии Азотовмісні сполуки
Азотовмісні сполуки Строение атома. Химия. 11 класс
Строение атома. Химия. 11 класс Теория электролитической диссоциации
Теория электролитической диссоциации Химические и физические свойства кремния
Химические и физические свойства кремния Функциональные производные карбоновых кислот
Функциональные производные карбоновых кислот Промышленные катализаторы
Промышленные катализаторы Nuclear Energy, Controlled Fission and Fusion 2016
Nuclear Energy, Controlled Fission and Fusion 2016 Предмет аналитической химии и ее основные понятия
Предмет аналитической химии и ее основные понятия Общие свойства металлов
Общие свойства металлов Щелочные металлы
Щелочные металлы Стекло. Виды стекол
Стекло. Виды стекол Физико-химические методы анализа. Лекция 3
Физико-химические методы анализа. Лекция 3 Теория электролитической диссоциации
Теория электролитической диссоциации Тема 7-Карбоновые кислоты
Тема 7-Карбоновые кислоты Основні закони хімії.Класи та номенклатура неорганічних сполук
Основні закони хімії.Класи та номенклатура неорганічних сполук Минерализация, иммобилизация, нитрификация және денитрификация процестері
Минерализация, иммобилизация, нитрификация және денитрификация процестері Химические реакции. Реакции разложения
Химические реакции. Реакции разложения Химическая кинетика
Химическая кинетика Наука о веществе - химия
Наука о веществе - химия Кислоты
Кислоты Азотная кислота и ее соли. 9 класс
Азотная кислота и ее соли. 9 класс Синтетические моющие средства. Механизм моющего действия
Синтетические моющие средства. Механизм моющего действия Массовая доля вещества в растворе
Массовая доля вещества в растворе