Содержание
- 2. Кислоты (по виду кислотного остатка)
- 3. Кислоты (по виду кислотного остатка) м кислотный остаток не содержит кислорода бескислородные
- 4. Кислоты (по виду кислотного остатка) м кислотный остаток не содержит кислорода бескислородные м кислородосодержащие кислотный остаток
- 5. Кислоты (по виду кислотного остатка) м кислотный остаток не содержит кислорода бескислородные м кислородосодержащие кислотный остаток
- 6. Кислоты (по виду кислотного остатка) м кислотный остаток не содержит кислорода бескислородные м кислородосодержащие кислотный остаток
- 7. Кислоты (по заряду кислотных остатков)
- 8. одноосновные Кислоты (по заряду кислотных остатков)
- 9. одноосновные двухосновные Кислоты (по заряду кислотных остатков)
- 10. одноосновные двухосновные трёхосновные Кислоты (по заряду кислотных остатков)
- 11. Одноосновные кислоты Заряд кислотного остатка -1, который соответственно соединяется с одним атомом водорода.
- 12. Одноосновные кислоты Заряд кислотного остатка -1, который соответственно соединяется с одним атомом водорода. HCl — cоляная
- 13. Двухосновные кислоты Заряд кислотного остатка -2, который соответственно соединяется с двумя атомами водорода.
- 14. Двухосновные кислоты Заряд кислотного остатка -2, который соответственно соединяется с двумя атомами водорода. H2SO4 — серная
- 15. Трёхосновные кислоты Заряд кислотного остатка -3, который соответственно соединяется с тремя атомами водорода.
- 16. Трёхосновные кислоты Заряд кислотного остатка -3, который соответственно соединяется с тремя атомами водорода. H3PO4 — фосфорная
- 17. Кислоты (по растворимости в воде)
- 18. растворимые Кислоты (по растворимости в воде)
- 19. растворимые нерастворимые Кислоты (по растворимости в воде)
- 20. растворимые нерастворимые Кислоты (по растворимости в воде) Сернистая кислота (H2SO3) и угольная кислота (H2CO3) существуют только
- 21. Растворимые кислоты: H2SO4 — серная кислота, H2S — сероводородная кислота, HNO3 — азотная кислота. Кислоты (по
- 22. Растворимые кислоты: H2SO4 — серная кислота, H2S — сероводородная кислота, HNO3 — азотная кислота. Кислоты (по
- 23. Кислоты (летучесть)
- 24. Кислоты (летучесть) летучие
- 25. Кислоты (летучесть) летучие нелетучие
- 26. Кислоты (летучесть) летучие нелетучие H2S — сероводородная кислота, HCl — хлороводородная кислота, соляная кислота, HNO3 —
- 27. Кислоты (летучесть) летучие нелетучие H2S — сероводородная кислота, HCl — хлороводородная кислота, соляная кислота, HNO3 —
- 28. Кислоты (по степени электролитической диссоциации )
- 29. Кислоты (по степени электролитической диссоциации ) сильные
- 30. Кислоты (по степени электролитической диссоциации ) сильные слабые
- 31. Кислоты (по степени электролитической диссоциации ) сильные слабые H2SO4 — серная кислота, HCl — хлороводородная кислота,
- 32. Кислоты (по степени электролитической диссоциации ) сильные слабые H2SO4 — серная кислота, HCl — хлороводородная кислота,
- 33. Стабильность кислоты — это степень устойчивости её состава при обычных условиях.
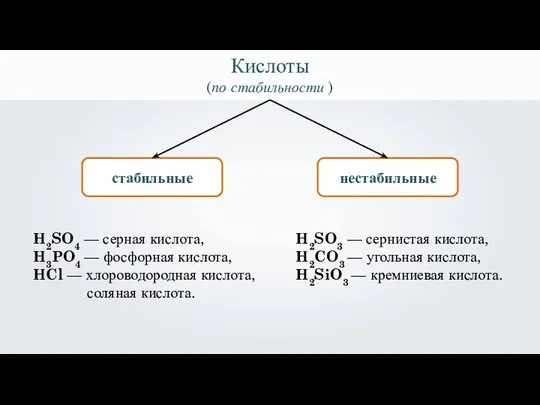
- 34. Кислоты (по стабильности )
- 35. Кислоты (по стабильности ) стабильные
- 36. Кислоты (по стабильности ) стабильные нестабильные
- 37. Кислоты (по стабильности ) стабильные нестабильные H2SO4 — серная кислота, H3PO4 — фосфорная кислота, HCl —
- 38. Кислоты (по стабильности ) стабильные нестабильные H2SO4 — серная кислота, H3PO4 — фосфорная кислота, HCl —
- 39. Кислоты (по агрегатному состоянию) твёрдые кремниевая кислота (H2SiO3) Майя Пчёлка
- 40. Кислоты (по агрегатному состоянию) твёрдые кремниевая кислота (H2SiO3) Майя Пчёлка жидкие серная кислота (H2SO4)
- 41. Кислоты (по агрегатному состоянию) твёрдые кремниевая кислота (H2SiO3) Майя Пчёлка жидкие серная кислота (H2SO4) хлороводородная кислота
- 42. Газообразные кислоты (HCl, HBr, H2S) при обычных условиях могут существовать в водных растворах.
- 43. Слабые кислоты (H2SO3, H2CO3 ) легко разлагаются на газ и воду, существуют только в водных растворах.
- 44. Летучесть — это способность кислоты испаряться при обычных условиях, не распадаясь на отдельные новые молекулы. H2SiO3
- 45. Большинство кислот не имеют окраски. Только хромовая кислота (H2CrO4) имеет жёлтую окраску, а марганцевая (HMnO4) —
- 47. Скачать презентацию



































 Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы
Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы Кислоты, их состав и названия
Кислоты, их состав и названия Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Ароматические углеводороды
Ароматические углеводороды Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Горение топлива
Горение топлива Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології
Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології Основные классы неорганических соединений
Основные классы неорганических соединений Соли, их классификация и свойства
Соли, их классификация и свойства Органічна хімія
Органічна хімія Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Жёсткость воды
Жёсткость воды Полисахариды: крахмал и целлюлоза
Полисахариды: крахмал и целлюлоза Растворы. Часть 2. Лекция №7
Растворы. Часть 2. Лекция №7 Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Буферные системы
Буферные системы Белки. Строение
Белки. Строение Классификация химических элементов. Составитель. 8 класс
Классификация химических элементов. Составитель. 8 класс Минералы для ИЗБ
Минералы для ИЗБ Концентрация растворов. Массовая доля растворенного вещества. Урок 1
Концентрация растворов. Массовая доля растворенного вещества. Урок 1 Химический элемент медь
Химический элемент медь Кинетика химических реакций
Кинетика химических реакций Кремний и его соединения
Кремний и его соединения Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Гидролиз солей
Гидролиз солей