Содержание
- 2. Реакции бывают: Гетерогенные Если реакция протекает между веществами, образующими гетерогенную систему, то она может идти только
- 3. В связи с этим скорость гомогенной реакции и скорость гетерогенной реакции определяются различно. Скоростью гомогенной реакции
- 4. Скоростью гетерогенной реакции называется количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени
- 5. Факторы, влияющие на скорость химической реакции: природа реагирующих веществ; их концентрации; температура; присутствие в системе катализаторов.
- 6. Зависимость скорости реакции от концентрации реагирующих веществ Закон действующих масс К.М. Гульдберг и П. Вааге (1867
- 7. Зависимость скорости реакции от температуры Правило Вант-Гоффа: При повышении температуры на каждые 10°С скорость реакции и
- 8. Правило Вант-Гоффа довольно грубо описывает зависимость скорости от температуры. Значительно более точно зависимость константы скорости к
- 9. Величина энергии активизации может быть определена, если известны два значения константы скорости К1 и К2 при
- 10. Теория соударений Согласно этой теории: частицы должны столкнуться с энергией, достаточной для того, чтобы разорвать существующие
- 11. Изменение потенциальной энергии между реакционными центрами в бимолекулярной реакции АВ и PQ – исходные вещества; АР
- 12. Схема синтеза иодоводорода
- 13. Зависимость скорости реакции от катализатора Вещества, не расходующиеся в результате протекания реакции, но влияющие на ее
- 14. Энергетическая схема реакции, протекающей с участием катализатора АВ и PQ – исходные вещества; АР и BQ
- 15. Катализ бывает: Гомогенный (каталитическое разложение перекиси водорода в водном растворе на воду и кислород. Ионы СгО42-,
- 16. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 17. По обратимости реакции делят на: Необратимые Zn+4HNO3= Zn(NO3)3 + 2NO2 + 2Н2О Обратимые N2 + 3H2
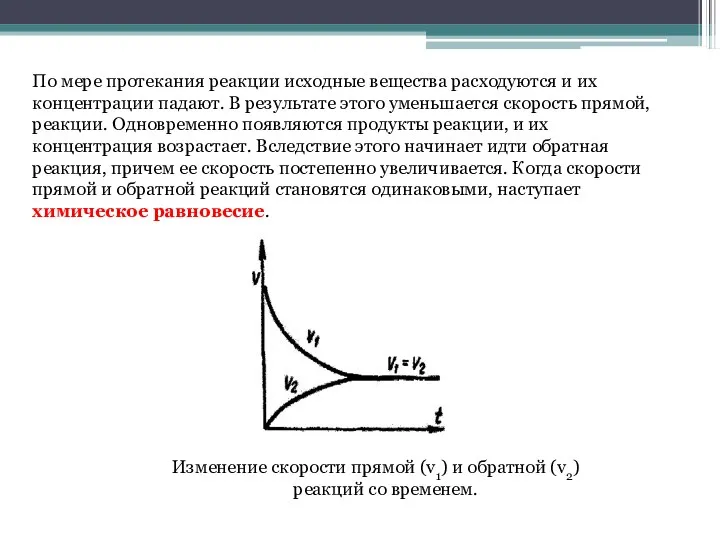
- 18. Изменение скорости прямой (v1) и обратной (v2) реакций со временем. По мере протекания реакции исходные вещества
- 19. Согласно закону действия масс, скорости прямой (υ1) и обратной (υ2) реакций выражаются уравнениями: υ1= k1 [H2][I2]
- 20. аА+ bВ + … = рР + qQ+... ; ; Отношение констант скорости прямой и обратной
- 21. Равновесие в гетерогенных системах СО2(г) + С(тв) ⇄ 2СО(г) В случае гетерогенных реакций в выражение константы
- 22. Равновесие в гомогенных системах N2(г) + 3H2(г) ⇄ 2NH3(г)
- 23. Связь константы равновесия с энергией Гиббса ΔG = - RT · ln K p (кДж/моль) Если
- 24. Если система находится в состоянии равновесия, то она будет пребывать в нем до тех пор, пока
- 25. Нарушение равновесия вследствие изменения давления Правило: при увеличении давления путем сжатия системы равновесие сдвигается в сторону
- 26. Принцип Ле-Шателье – Брауна: Если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате
- 28. Скачать презентацию
























 Фенолы
Фенолы Алюминий и бор
Алюминий и бор Одноатомные спирты
Одноатомные спирты Спирты
Спирты Пластмаси та їх роль у сучасному виробництві
Пластмаси та їх роль у сучасному виробництві Аргентум, или серебро
Аргентум, или серебро Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Каменный уголь. Фенол
Каменный уголь. Фенол Органическая химия. Олигосахариды. Полисахариды
Органическая химия. Олигосахариды. Полисахариды 10 самых смертельно опасных камней и минералов
10 самых смертельно опасных камней и минералов Термодинамика химического равновесия
Термодинамика химического равновесия Зерттеу әдістері
Зерттеу әдістері Кремний и его соединения. Аллотропные модификации
Кремний и его соединения. Аллотропные модификации Химические понятия
Химические понятия Спирти
Спирти Необратимые электродные процессы. Часть 2
Необратимые электродные процессы. Часть 2 Химические свойства кислот как электролитов
Химические свойства кислот как электролитов Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Алмаз. Алмаз дегеніміз не
Алмаз. Алмаз дегеніміз не Простые вещества - неметаллы
Простые вещества - неметаллы Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Растворы. Массовая доля растворённого вещества
Растворы. Массовая доля растворённого вещества Валентность химических элементов. 8 класс
Валентность химических элементов. 8 класс В мире химии. Периодический закон и ПСХЭ
В мире химии. Периодический закон и ПСХЭ Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Защита от коррозии каменных и бетонных строительных материалов и конструкций
Защита от коррозии каменных и бетонных строительных материалов и конструкций Физико-химические свойства алкенов
Физико-химические свойства алкенов Химическая промышленность. Минеральные удобрения
Химическая промышленность. Минеральные удобрения