Содержание
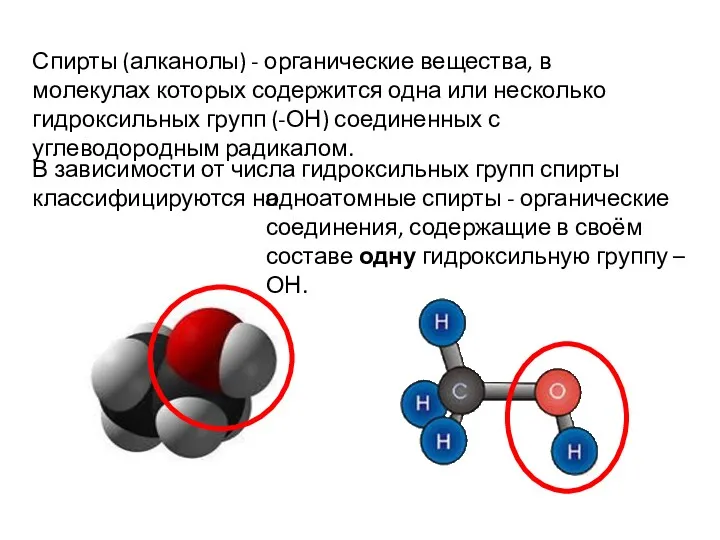
- 2. Спирты (алканолы) - органические вещества, в молекулах которых содержится одна или несколько гидроксильных групп (-ОН) соединенных
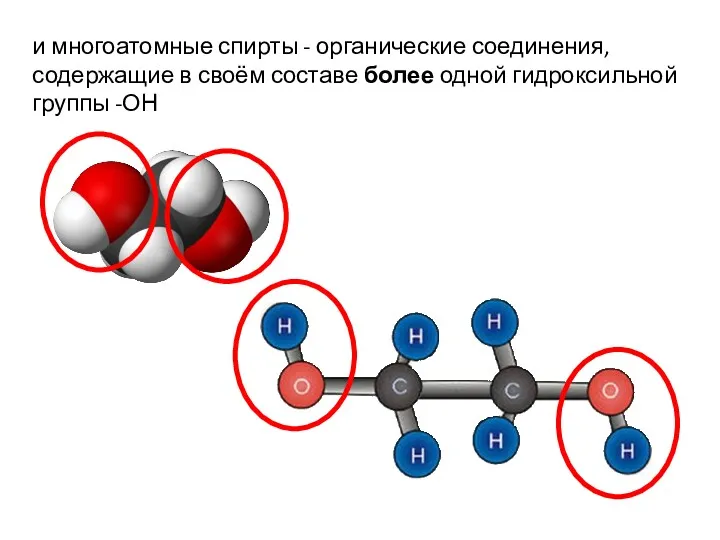
- 3. и многоатомные спирты - органические соединения, содержащие в своём составе более одной гидроксильной группы -ОН
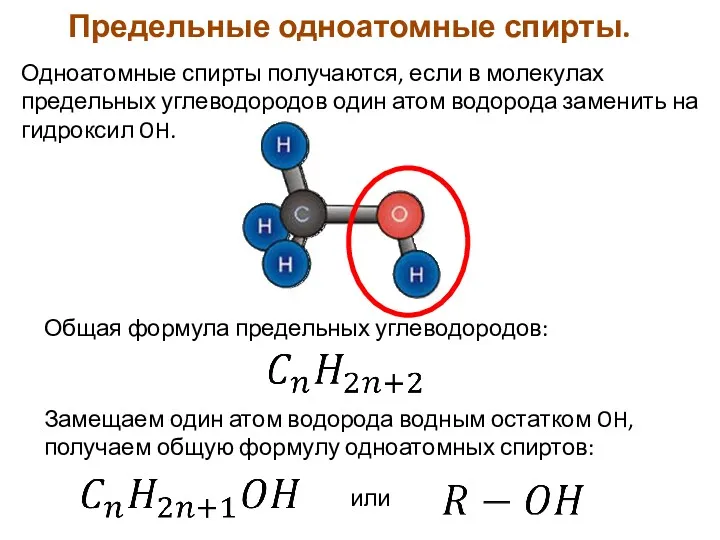
- 4. Одноатомные спирты получаются, если в молекулах предельных углеводородов один атом водорода заменить на гидроксил OH. Общая
- 5. Из метана получаем метанол: Из этана получаем этанол: Из пропана получаем пропанол: Из бутана получаем бутанол:
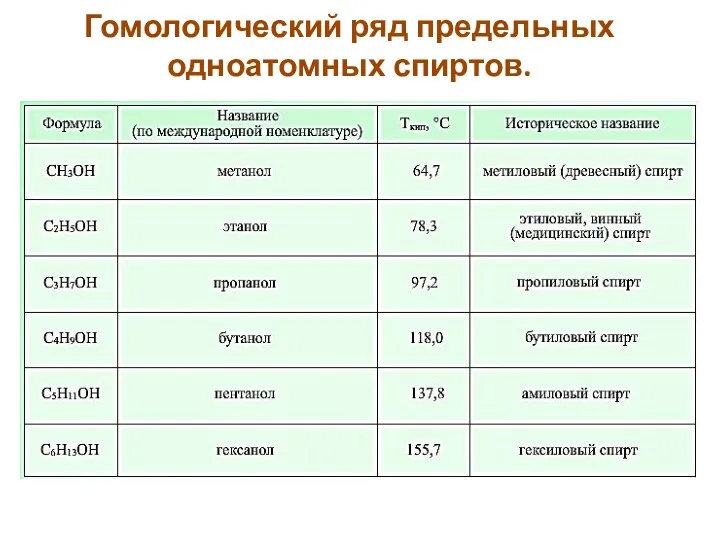
- 6. Гомологический ряд предельных одноатомных спиртов.
- 7. В любом гомологическом ряду существует закономерность. С увеличением молекулярной массы предельных углеводородов и спиртов увеличивается температура
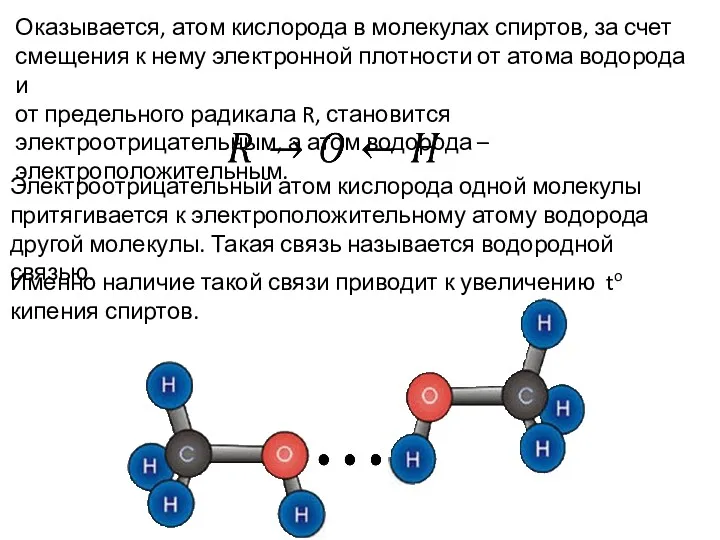
- 8. Оказывается, атом кислорода в молекулах спиртов, за счет смещения к нему электронной плотности от атома водорода
- 9. Спирты растворяются в воде. Однако с увеличением молекулярной массы спиртов растворимость их в воде ухудшается.
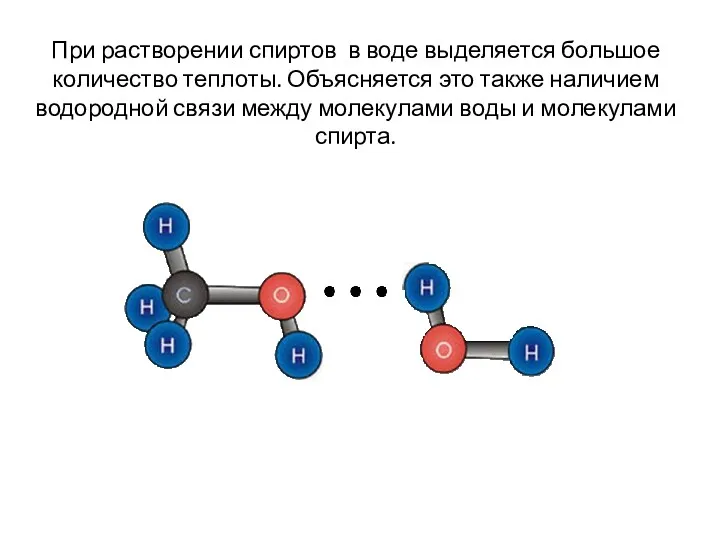
- 10. При растворении спиртов в воде выделяется большое количество теплоты. Объясняется это также наличием водородной связи между
- 11. Изомерия предельных одноатомных спиртов. От того, к какому атому углерода прикреплена функциональная группа OH и строения
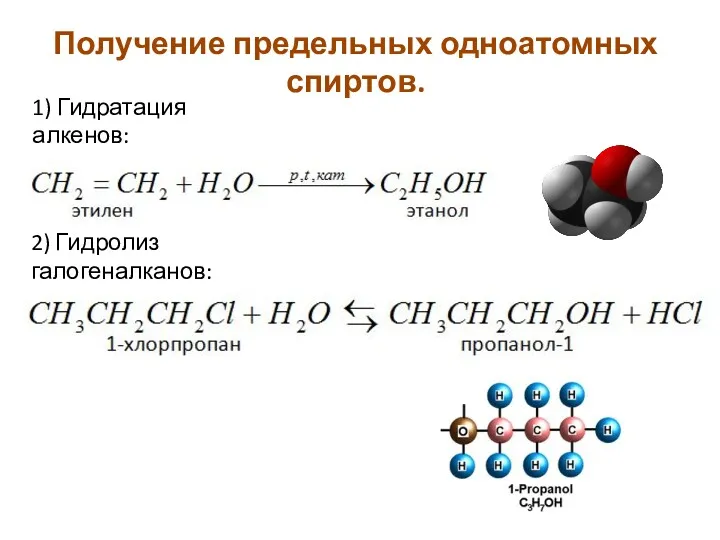
- 12. Получение предельных одноатомных спиртов. 2) Гидролиз галогеналканов: 1) Гидратация алкенов:
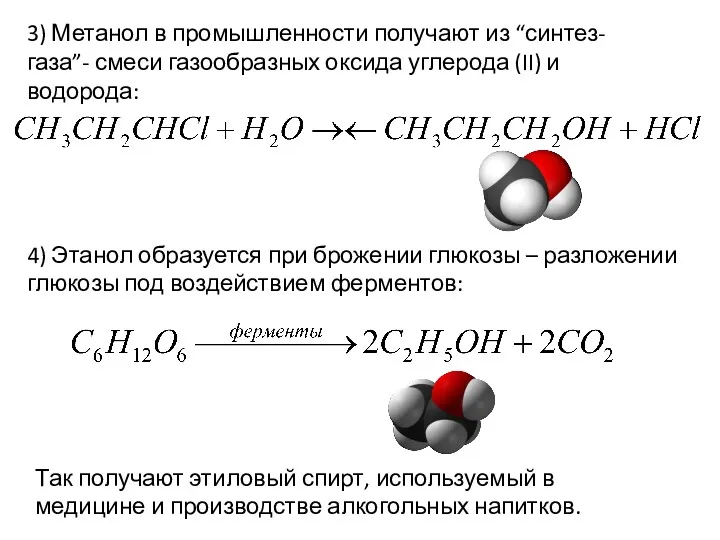
- 13. 3) Метанол в промышленности получают из “синтез-газа”- смеси газообразных оксида углерода (II) и водорода: 4) Этанол
- 14. Тема: «Многоатомные спирты» 900igr.net
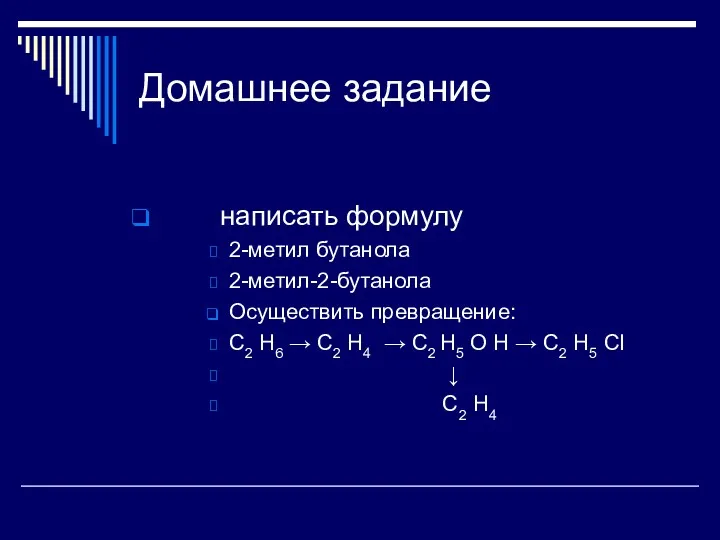
- 15. Домашнее задание написать формулу 2-метил бутанола 2-метил-2-бутанола Осуществить превращение: C2 H6 → C2 H4 → C2
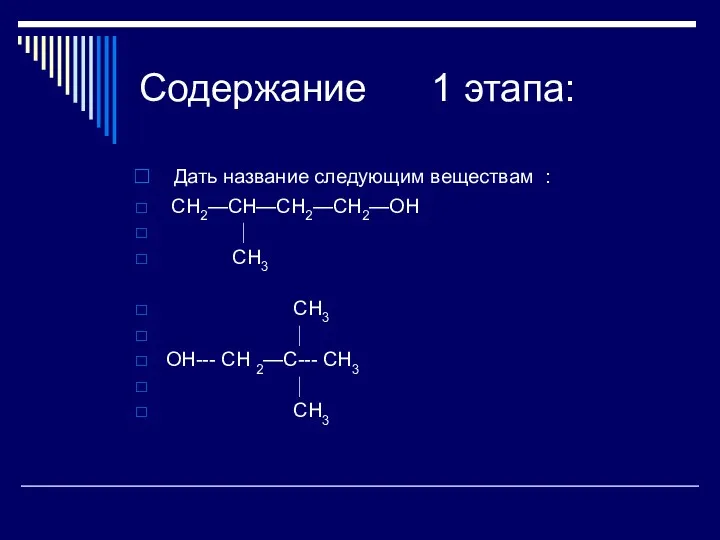
- 16. Содержание 1 этапа: Дать название следующим веществам : CH2—CH—CH2—CH2—OH ⏐ CH3 CH3 ⏐ OH--- CH 2—C---
- 17. Химические свойства многоатомных спиртов Взаимодействие с металлами Взаимодействие с гидроксидом меди Взаимодействие с азотной кислотой
- 18. Генетическая связь многоатомных спиртов
- 19. Применение спиртов Использование в косметике Использование в медицине Использование в текстильной промышленности Использование в радиаторах машин
- 20. Представленные вещества
- 21. Тосол ЭТИЛЕНГЛИКОЛЬ - двухатомный спирт. Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от чего
- 22. Тосол Тосол этиленгликоль Многоатомный спирт
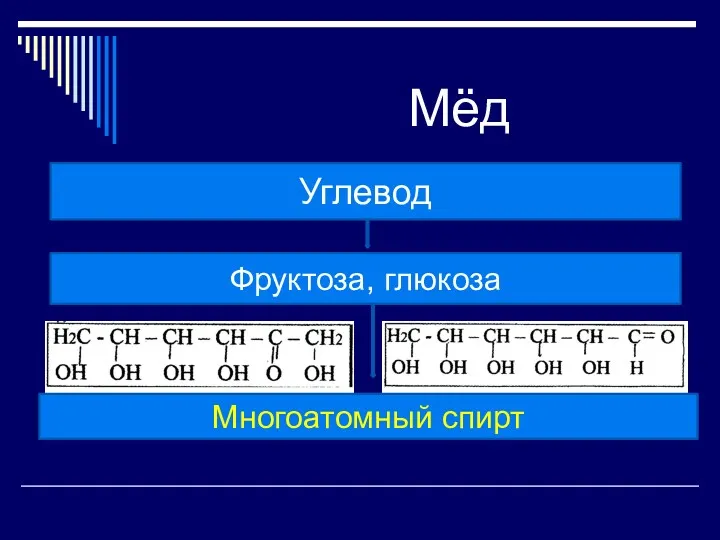
- 23. Мёд Основной составной частью мёда всех видов являются углеводы. В процентном отношении глюкоза составляет около 35%
- 24. Мёд Углевод Фруктоза, глюкоза Многоатомный спирт
- 25. Маннит Маннит — шестиатомный спирт, содержится во многих растениях. Сорбит – является составной частью маннита. Сорбит
- 26. Маннит Сорбит Многоатомный спирт
- 27. Жевательная резинка Жева́тельная рези́нка — вид конфеты, которая состоит из несъедобной эластичной основы и различных вкусовых
- 28. Жевательная резинка Ксилит Многоатомный спирт
- 29. Детский крем (глицерин) Глицерин – трёхатомный спирт. Это бесцветная, вязкая, гигроскопи-чная, сладкая на вкус жидкость. Смешивается
- 30. Детский крем Глицерин Многоатомный спирт
- 31. Растительное масло Жиры – это сложные эфиры глицерина и высших карбоновых кислот. Насыщенные кислоты образуют твердые
- 33. Скачать презентацию


















 Titration and Acid-Base Neutralization
Titration and Acid-Base Neutralization Мына қосылыстардағы элементтердің тотығу дәрежелерін анықтаңдар
Мына қосылыстардағы элементтердің тотығу дәрежелерін анықтаңдар Классы неорганических соединений
Классы неорганических соединений Current Condition(Revision C)
Current Condition(Revision C) Металдар
Металдар Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Генетичні зв’язки між неорганічними речовинами. Практична робота 2
Генетичні зв’язки між неорганічними речовинами. Практична робота 2 Ауыр металлдар
Ауыр металлдар Вода как среда и участник протекания биохимических процессов в организме
Вода как среда и участник протекания биохимических процессов в организме Производство чугуна и стали
Производство чугуна и стали Пластмассы в автомобилестроении
Пластмассы в автомобилестроении Натрий алкилсульфонаттарын алу. №4 лекция
Натрий алкилсульфонаттарын алу. №4 лекция Кислотно-основное титрование
Кислотно-основное титрование Гетерофункциональные производные бензольного ряда как лекарственные средства
Гетерофункциональные производные бензольного ряда как лекарственные средства Открытие новых химических элементов с атомными номерами 113, 115, 117 и 118
Открытие новых химических элементов с атомными номерами 113, 115, 117 и 118 Iron Oxide
Iron Oxide Коррозия металлов и способы защиты от коррозии
Коррозия металлов и способы защиты от коррозии Синтетические моющие средства
Синтетические моющие средства Цинк
Цинк Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння
Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння Кислоты и основания. (Лекция 16)
Кислоты и основания. (Лекция 16)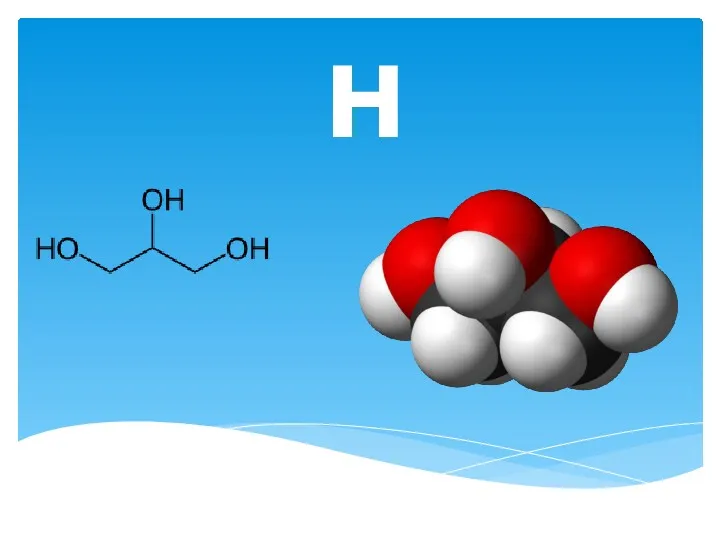 Глицерин. Основные способы получения
Глицерин. Основные способы получения Основні класи неорганічних сполук
Основні класи неорганічних сполук Твердость минералов и их применение
Твердость минералов и их применение Хімічний зв’язок. Типи хімічного зв’язку
Хімічний зв’язок. Типи хімічного зв’язку Резина. Свойства резины
Резина. Свойства резины Физико-химические методы анализа. Лекция 3
Физико-химические методы анализа. Лекция 3 Серная кислота и ее соли
Серная кислота и ее соли