Слайд 2

План:
Сущность кислотно-основного титрования.
Первичные стандарты метода кислотно-основного титрования.
рН-индикаторы. Теории кислотно-основных индикаторов.
Способы подбора
индикаторов
Слайд 3

Сущность кислотно-основного титрования
В основе метода кислотно-основного титрования лежат реакции, связанные с
переносом ионов водорода между веществами, проявляющими кислотно-основные свойства.
НА + В ↔ НВ+ + А-
а1 b2 а2 b1
Слайд 4

Титранты метода КОТ
В методе ацидиметрии в качестве титрантов применяют
0,01-1 М растворы кислот (HCl, H2SO4, HNO3, HClO4), в методе алкалиметрии – 0,01-1 М растворы щелочей (NaOH, KOH, Ba(OH)2).
Ba2+ + CO32- ⇄ BaCO3↓
Слайд 5

Тетраборат натрия декагидрат, бура (Na2B4O7 ∙10H2O)
B4O72- + 2H+ + 5H2O ⇄
4H3BO3
fэ (Na2B4O7 . 10H2O) = ½
индикатор – метиловый красный, метиловый оранжевый
Слайд 6

Карбонат натрия (Na2CO3)
CO32- + 2H+ ⇄ H2CO3
fэ (Na2CO3) = ½
индикатор –
метиловый красный, метиловый оранжевый
CO32- + H+ ⇄ HCO3 –
fэ (Na2CO3) = 1
индикатор – фенолфталеин
Слайд 7

Оксалат натрия (Na2C2O4)
Гидротартрат натрия (NaНC4H4O6) после
прокаливания
обеих солей
получают Na2CO3
Слайд 8

Щaвeлeвaя киcлотa H2C2O4·2 H2O (Ka1=5,6·10-2; Ka2=5,4·10-5)
H2C2O4 + 2OH- ⇄ C2O4 2-
+ 2H2О
fэ (H2C2O4) = ½
индикатор – фенолфталеин
Янтарная кислота H2C4H4O4 (Ka1 = 1,6·10-5;
Ka2 = 2,3·10-6)
H2C4H4O4 + 2OH- ⇄ C4H4O42-
fэ (H2C4H4O4) = ½
индикатор – фенолфталеин
Слайд 9

HInd ⇄ H+ + Ind-
К ауксохромам относятся группы -ОН, -NH2, -СООН,
-ОСН3, -N(CH3)2 и др.
Слайд 10

Слайд 11

∆рН = рКа ±1
Слайд 12
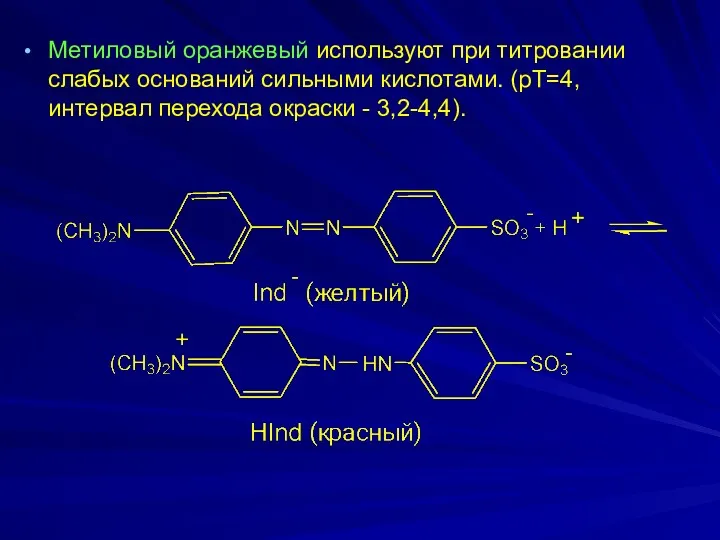
Метиловый оранжевый используют при титровании слабых оснований сильными кислотами. (рТ=4, интервал
перехода окраски - 3,2-4,4).
Слайд 13
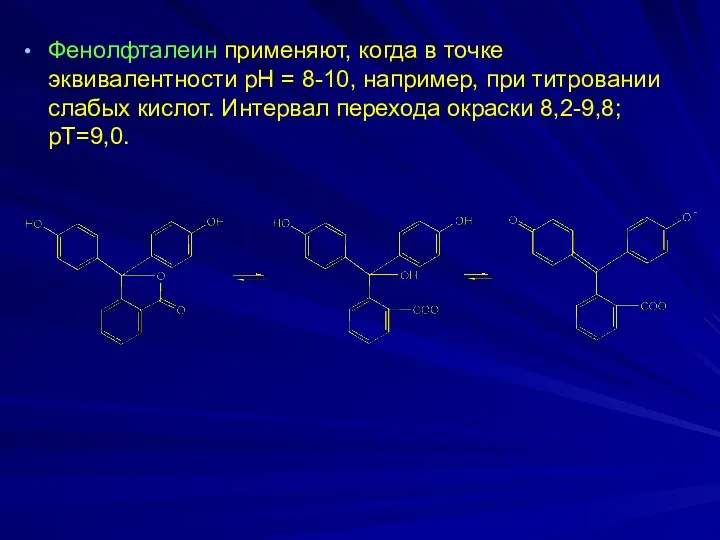
Фенолфталеин применяют, когда в точке эквивалентности рН = 8-10, например, при
титровании слабых кислот. Интервал перехода окраски 8,2-9,8; рТ=9,0.
Слайд 14
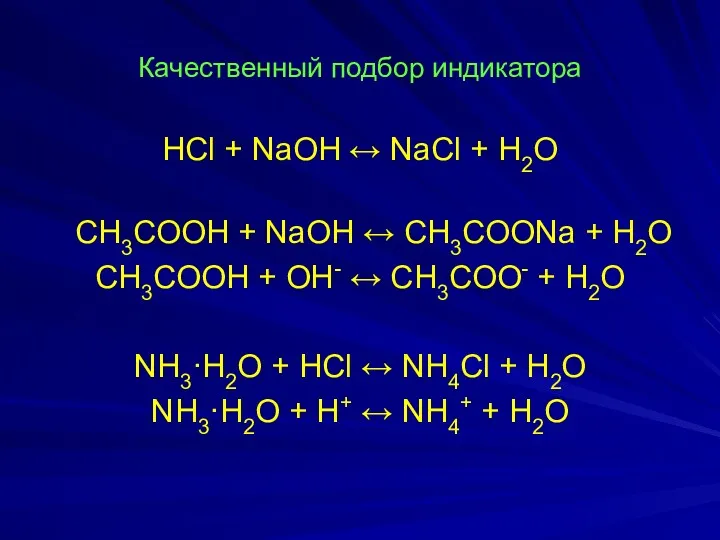
Качественный подбор индикатора
HCl + NaOH ↔ NаCl + H2O
СH3COOH + NaOH
↔ СH3COONa + H2O
СH3COOH + OH- ↔ СH3COO- + H2O
NH3·H2O + HCl ↔ NH4Cl + H2O
NH3·H2O + H+ ↔ NH4+ + H2O













 Растворы электролитов. Буферные растворы. Лекция 4
Растворы электролитов. Буферные растворы. Лекция 4 Гидроксиды. Основания. Состав, классификация, свойства, получение
Гидроксиды. Основания. Состав, классификация, свойства, получение Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Бутадиеновые каучуки
Бутадиеновые каучуки Көпатомды спирттер. Химиялық қасиеттері
Көпатомды спирттер. Химиялық қасиеттері Задачи на растворы
Задачи на растворы Гідроліз солей
Гідроліз солей Полимерные материалы. Пластические массы и строительные материалы на их основе
Полимерные материалы. Пластические массы и строительные материалы на их основе Классификация реакций и реагентов органической химии
Классификация реакций и реагентов органической химии Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання
Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання Дисперсные системы
Дисперсные системы Химический состав воздуха
Химический состав воздуха Массовая доля элемента в сложном веществе
Массовая доля элемента в сложном веществе Химическая связь
Химическая связь Физические и химические свойства воды
Физические и химические свойства воды Чистые вещества и смеси
Чистые вещества и смеси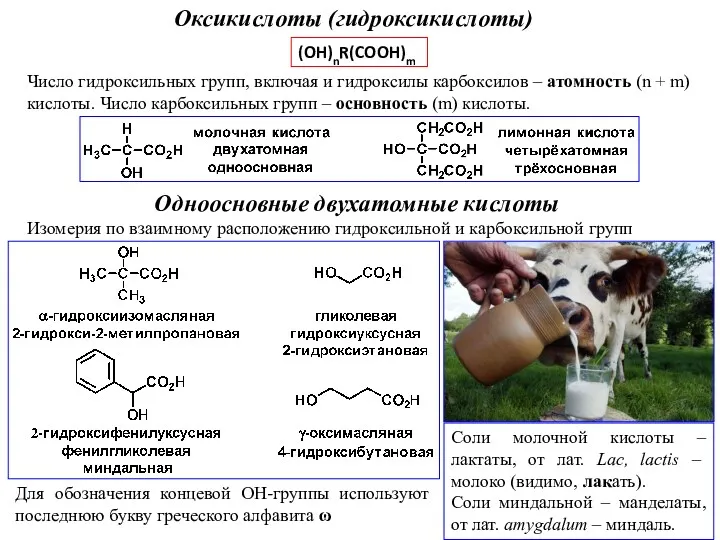 Оксикислоты (гидроксикислоты)
Оксикислоты (гидроксикислоты) Польза и вред химического производства
Польза и вред химического производства Химические свойства металлов
Химические свойства металлов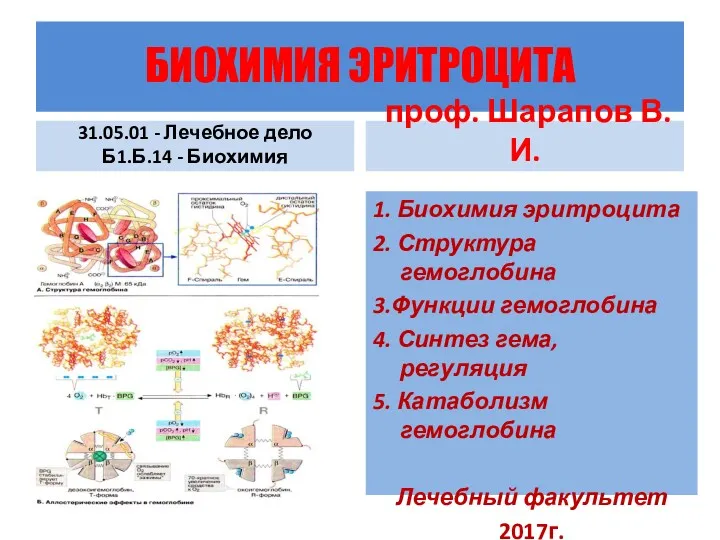 Биохимия эритроцита
Биохимия эритроцита Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички
Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички Растворы. Термодинамика образования растворов. Растворимость веществ (Лекция 3)
Растворы. Термодинамика образования растворов. Растворимость веществ (Лекция 3) Менделеевские уроки. День науки
Менделеевские уроки. День науки Хімічні явища у природі
Хімічні явища у природі Конденсация. Капельная и пленочная конденсация
Конденсация. Капельная и пленочная конденсация Лекция 6. Алициклические углеводороды (циклоалканы, нафтены)
Лекция 6. Алициклические углеводороды (циклоалканы, нафтены) Хроматографические методы анализа
Хроматографические методы анализа Сложные эфиры
Сложные эфиры