Содержание
- 2. Тема:“Типи хімічного зв’язку» Мета: сформувати уявлення про природу хімічного зв’язку; механізм утворення ковалентного та йонного зв’язку;
- 3. Цілі Природа хімічного зв’язку; Механізм утворення ковалентного зв’язку; Види ковалентних зв’язків; Йонний зв’язок.
- 4. Хімі́чний зв'язо́к —це енергія взаємодії між атомами, яка утримує їх у молекулі чи твердому тілі. Хімічні
- 5. Електронегативність Електронегативність — здатність атома притягати до себе електрони інших атомів Відносна електронегативність відповідає Періодичному закону:
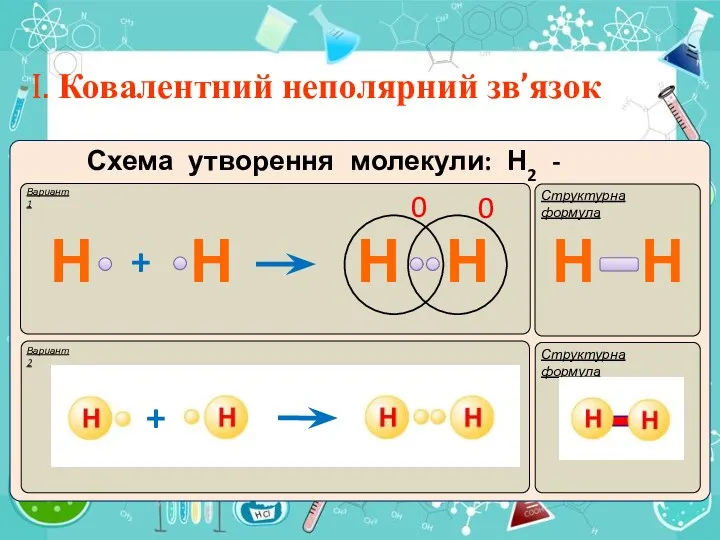
- 6. I. Ковалентний неполярний зв’язок Вариант 1 Структурна формула Н Н
- 7. Вариант 1 Структурна формула
- 8. . Вариант 1 Структурна формула
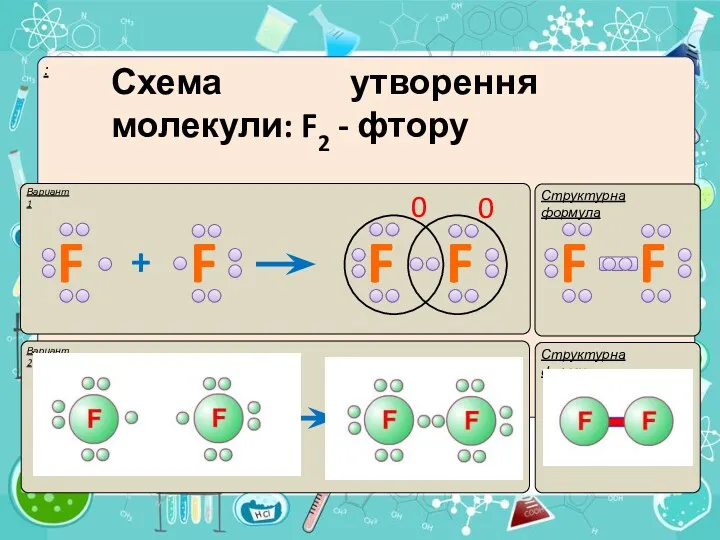
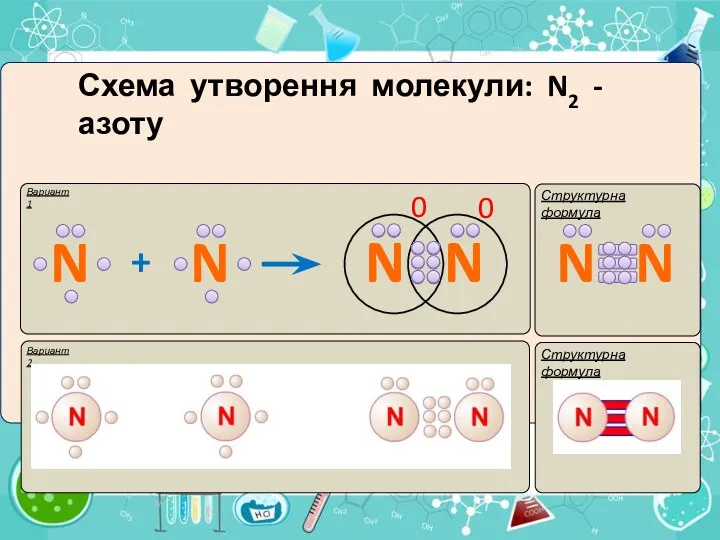
- 9. I. Ковалентний неполярний зв’язок
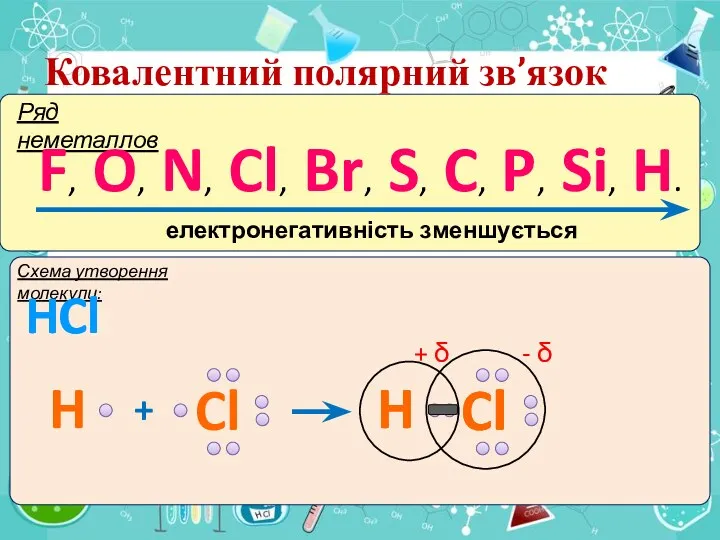
- 10. IІ. Ковалентний полярний зв’язок Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H.
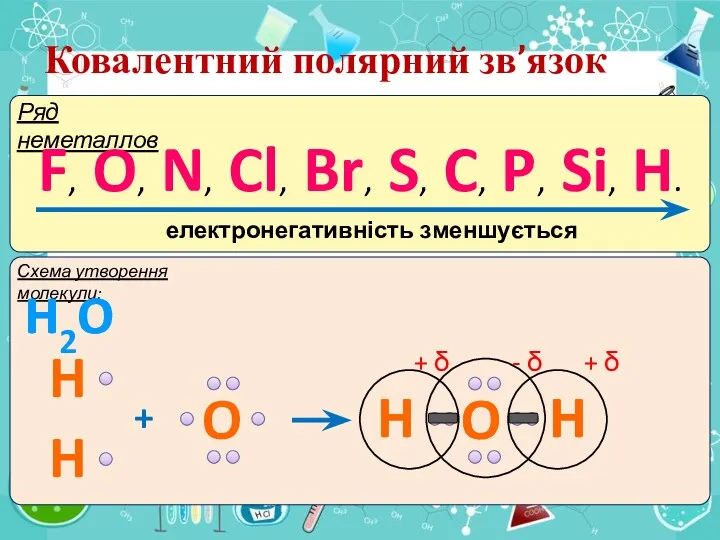
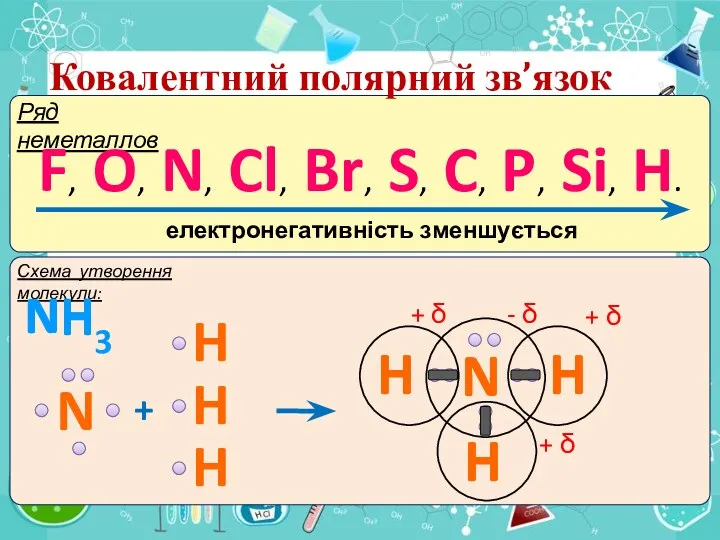
- 11. Ковалентний полярний зв’язок Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. електронегативність
- 12. Ковалентний полярний зв’язок Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. електронегативність
- 13. Ковалентний полярний зв’язок Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. електронегативність
- 15. Йонний з’язок 1ē
- 16. Частинка, яка віддає електрони, претворюється на позитивний йон. Частинка, яка приєднує електрони, претворюється на негативний йон.
- 17. IІ. Йонний зв’язок
- 19. Скачать презентацию










 Жидкие вещества
Жидкие вещества Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Важнейшие промышленные синтезы на основе переработки нефти и другого углеводородного сырья
Важнейшие промышленные синтезы на основе переработки нефти и другого углеводородного сырья Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Состав, строение и свойства аминокислот
Состав, строение и свойства аминокислот Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение Жидкокристаллические индикаторы
Жидкокристаллические индикаторы Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве
Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях Орбитали и связи
Орбитали и связи Ароматические кислоты и их соли
Ароматические кислоты и их соли Атомно-молекулярное учение. (Лекция 1)
Атомно-молекулярное учение. (Лекция 1) Спирты. Классификация спиртов
Спирты. Классификация спиртов Жиры. Мыла. 10 класс
Жиры. Мыла. 10 класс Зародження періодичної системи елементів Менделєєва
Зародження періодичної системи елементів Менделєєва Откуда берутся кристаллы
Откуда берутся кристаллы Основной государственный экзамен Химия 2021. Задание 5
Основной государственный экзамен Химия 2021. Задание 5 Текстуры и структуры метаморфических горных пород
Текстуры и структуры метаморфических горных пород Азот и его соединения
Азот и его соединения Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау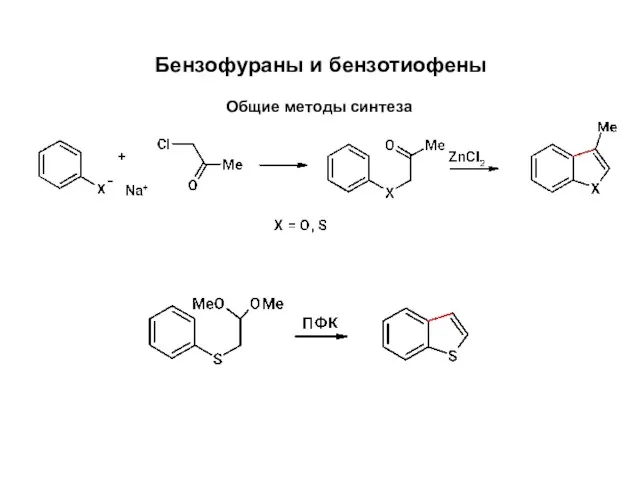 Бензофураны и бензотиофены. Общие методы синтеза
Бензофураны и бензотиофены. Общие методы синтеза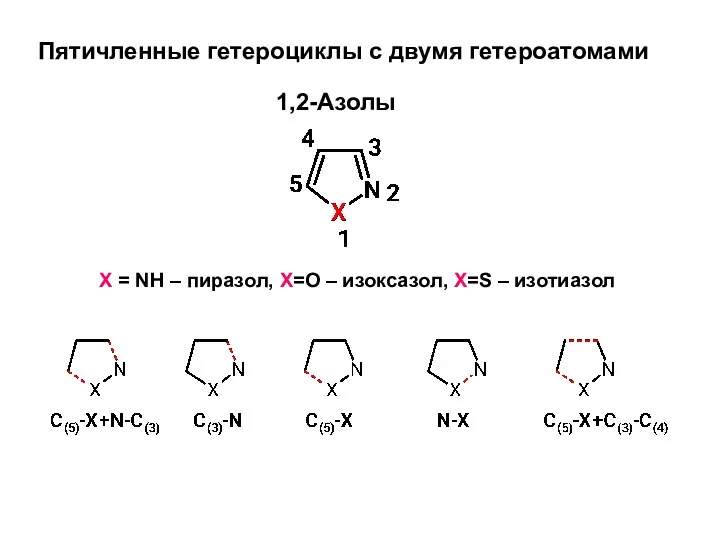 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами Заключительный урок в 8 классе Тест по химии.
Заключительный урок в 8 классе Тест по химии. Теория электролитической диссоциации
Теория электролитической диссоциации Классификация и свойства кислот
Классификация и свойства кислот Теории происхождения нефти
Теории происхождения нефти Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ Художественная обработка металла
Художественная обработка металла