Содержание
- 2. 2.6. КАТАЛИЗ Катализ - изменение скорости реакции под действием некоторых веществ, которые участвуют в реакции, но
- 3. Основные принципы катализа. 1) Катализ изменяет механизм реакции на энергетически более выгодный, т.е. снижает энергию активации.
- 4. Рассмотрим энергетическую диаграмму реакции и обратимую реакцию. Кравн=k1/k2=k0exp(-E1- ∆E)/k0exp(-E2-∆E)=Kkравн Катализатор увеличивает скорость реакции в: exp(∆E/RT) раз.
- 5. Активность катализатора измеряется числом молей вещества, реагирующих на поверхности за сек. при заданной концентрации. Она определяется
- 6. Каталитические яды: для железа при синтезе аммиака - вода, O, HCN, As. Объясняется тем, что яд
- 7. Пять стадий каталитической реакции на твердом катализаторе: 1) диффузия к поверхности 2) адсорбция 3) химическая реакция
- 8. Мультиплетная теория Баландина. Исходит из принципа структурного соответствия между расположением атомов в активных центрах и строением
- 11. Электронная теория катализа Волькенштейн создал теорию катализа на полупроводниках. Активным центром является свободный электрон или "дырка"
- 12. У ионов М+ и R- (например, Na+ и С1-) имеются замкнутые восьмиэлектронные оболочки и отсутствуют свободные
- 13. ЦЕПНЫЕ РЕАКЦИИ Это особый тип сложных реакций, широко распространенных в природе и технике (горение, взрыв, полимеризация
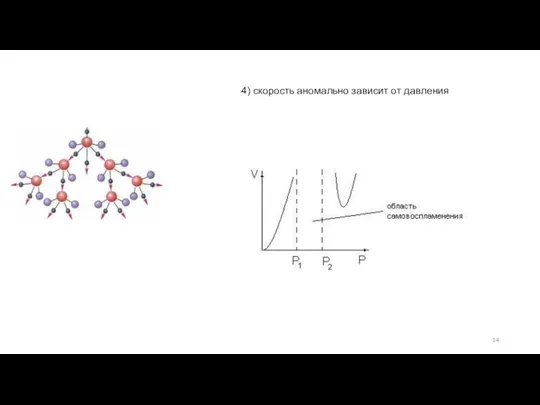
- 14. 4) скорость аномально зависит от давления
- 15. Теория цепных реакций Семенова и Хиншельвуда. Свободный радикал - фрагмент молекулы или атом, имеющие неспаренный электрон.
- 16. Согласно теории. 3 стадии цепных реакций: 1) зарождение цепи, 2)развитие цепи, 3)обрыв цепи. Рассмотрим 1-ю стадию.
- 17. Рассмотрим для примера реакцию Н2+Сl2=2HCl. Первая стадия: Cl2+hn=2Cl. Вторая: Cl. +H2=HCl+H. H. +Cl2=HCl+Cl. Эти две реакции
- 18. Третья стадия происходит при встрече двух радикалов. Но для того, чтобы произошло образование нормальной молекулы из
- 19. Характеризуем скорость реакции скоростью изменения числа радикалов dm/dt, где m - число радикалов в единице объема.
- 20. Исследуем три случая. а)сильное ветвление γ>β тогда при t→∞ m→∞ б)слабое ветвление γ тогда при t→∞
- 22. Скачать презентацию


















 Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Соединения железа
Соединения железа Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева
Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева Алканы. Строение, номенклатура, изомерия, химические и физические свойства
Алканы. Строение, номенклатура, изомерия, химические и физические свойства Общая характеристика неметаллов
Общая характеристика неметаллов Титан. Хром
Титан. Хром Современные проблемы молекулярной биологии
Современные проблемы молекулярной биологии Хімічні властивості кислот
Хімічні властивості кислот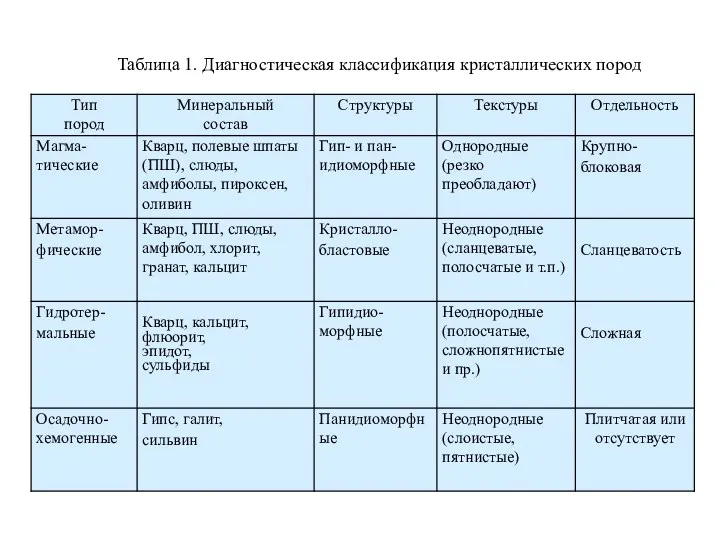 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород Нуклеиновые кислоты
Нуклеиновые кислоты Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар Аммиак. Строение атома азота
Аммиак. Строение атома азота Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Organic molecules
Organic molecules Щелочные металлы
Щелочные металлы Чисті речовини і суміші
Чисті речовини і суміші Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Полимерные материалы, пластмассы и изделия из них
Полимерные материалы, пластмассы и изделия из них Поливинилхлорид
Поливинилхлорид Неметаллы. Занятие 20
Неметаллы. Занятие 20 Омыватель лобового стекла
Омыватель лобового стекла Неон (Ne)
Неон (Ne) Основные разделы химии
Основные разделы химии Строение атома
Строение атома Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент
Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент Химия нефти и газа
Химия нефти и газа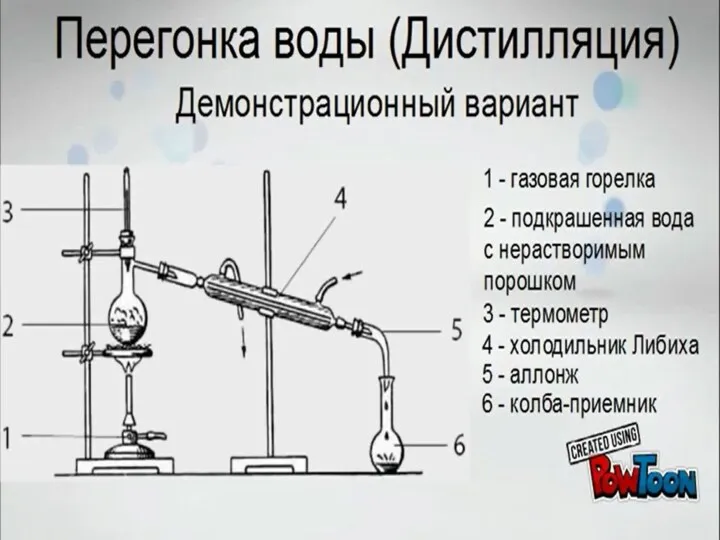 Перегонка воды (дистилляция). Демонстрационный вариант
Перегонка воды (дистилляция). Демонстрационный вариант Водород. Строение, свойства, получение, применение
Водород. Строение, свойства, получение, применение