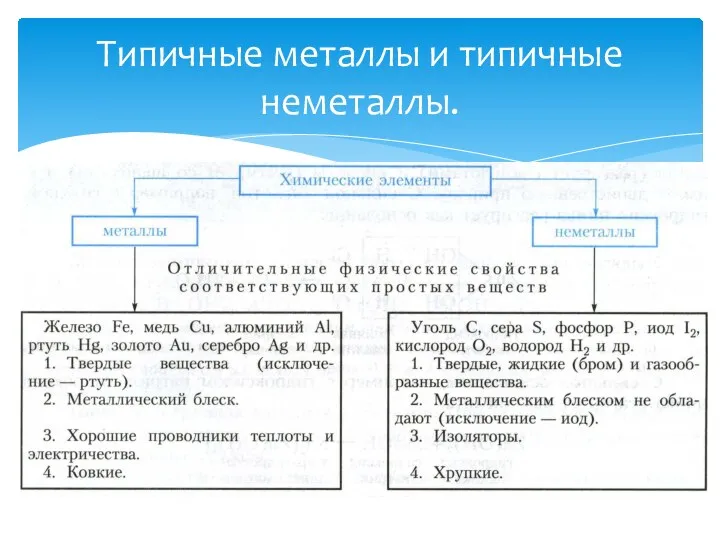
Типичный металл
взаимодействует с кислородом
и образует основный оксид:
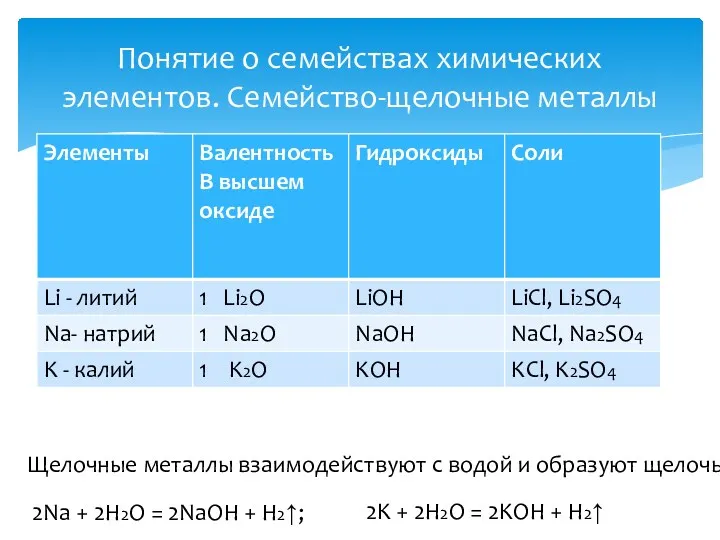
Na2O, MgO, CaO, BaO,
K2O.
2Ca + O2 = 2CaO оксид кальция
которому соответствует основание
СaO + H2O = Ca(OH)2 гидроксид кальция
Основание реагирует с кислотой,
образуя соль и воду:
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
хлорид кальция
Металл вытесняет из кислот водород:
Mg + H2SO4 = MgSO4 + H2↑.
сульфат магния
Типичный неметалл
взаимодействует с кислородом
и образует кислотный оксид:
CO2, SO2, P2O5, SiO2, SO3.
4P + 5O2 = 2P2O5
Которому соответствует кислота
P2O5 + 3H2O = 2H3PO4
Кислота реагирует с основанием,
Образуя соль и воду:
H3PO4 + 3NaOH = Na3PO4 + 3H2O
Неметалл с кислотой не реагирует.
Неметалл реагирует с водородом и образует летучее водородное соединение:
S + H2 = H2S.






 Генетическая связь органических и неорганических соединений
Генетическая связь органических и неорганических соединений Кремний. Основные минералы кремния
Кремний. Основные минералы кремния Закон постоянства состава. Молекулярная формула вещества
Закон постоянства состава. Молекулярная формула вещества Первичная переработка нефти
Первичная переработка нефти Оксид серы (IV). Сернистая кислота и её соли
Оксид серы (IV). Сернистая кислота и её соли Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды Алканы. Способы получения алканов. Химические свойства алканов
Алканы. Способы получения алканов. Химические свойства алканов Електроліти в сучасних акумуляторах
Електроліти в сучасних акумуляторах Электронные конфигурации атомов
Электронные конфигурации атомов Нефть. Свойства нефти
Нефть. Свойства нефти Строение атома углерода
Строение атома углерода Катализ. Классификация каталитических процессов. Механизм действия катализаторов
Катализ. Классификация каталитических процессов. Механизм действия катализаторов Минеральные вяжущие вещества, материалы и изделия на их основе
Минеральные вяжущие вещества, материалы и изделия на их основе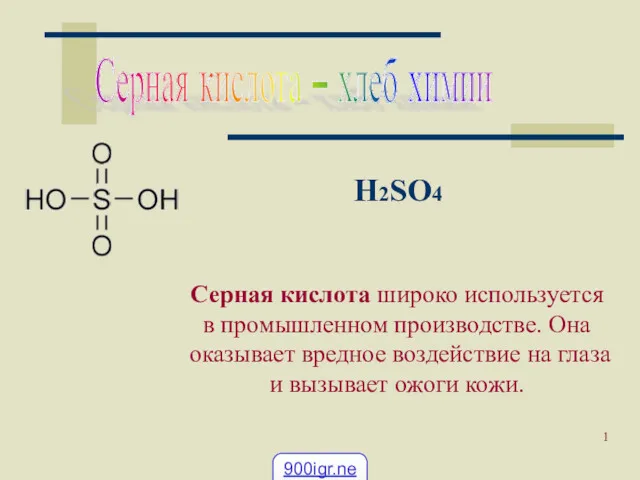 Применение серной кислоты
Применение серной кислоты Гигиена питания школьников
Гигиена питания школьников Классы неорганических веществ. Соли
Классы неорганических веществ. Соли Жасыл химия
Жасыл химия Стратегия химической промышленности
Стратегия химической промышленности Коррозия металлов
Коррозия металлов XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Nuclear Energy, Controlled Fission and Fusion 2016
Nuclear Energy, Controlled Fission and Fusion 2016 20230416_urok_na_20.02.2023
20230416_urok_na_20.02.2023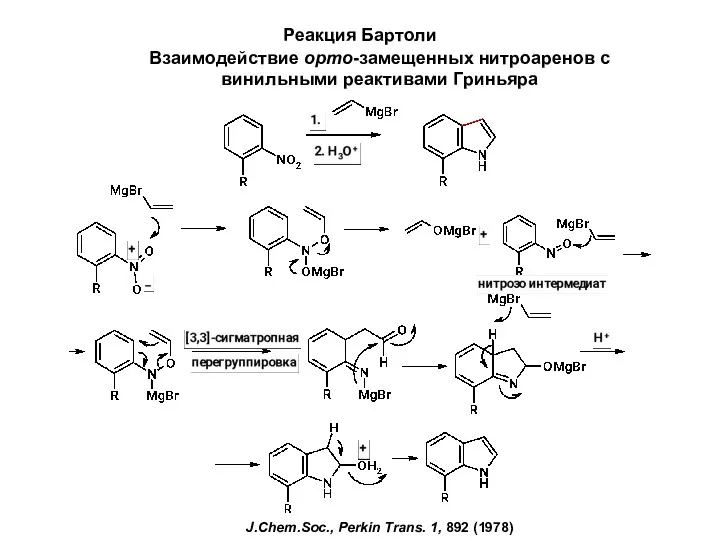 Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра
Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Методы в химии
Методы в химии Синтетические органические вещества
Синтетические органические вещества Качественные реакции на органические вещества
Качественные реакции на органические вещества Жиры
Жиры