Содержание
- 2. Все что нас окружает состоит из веществ. Кажется, что они живут своей жизнью, таинственной и непостижимой.
- 3. Отгадай загадку и узнай о чем пойдет речь на сегодняшнем уроке Она идет, она прошла! Никто
- 4. Что такое химическая реакция? Химические реакции или химические явления – это процессы, в результате которых из
- 5. По каким признакам можно определить химические реакции? Выделение газа; Образование осадка; Выделение (поглощение) тепла и света;
- 6. Каковы условия возникновения реакций: 1) Образование хлорида аммония 2) Горение магния 3) Взаимодействие алюминия с иодом
- 7. Химические реакции. Как классифицировать ?
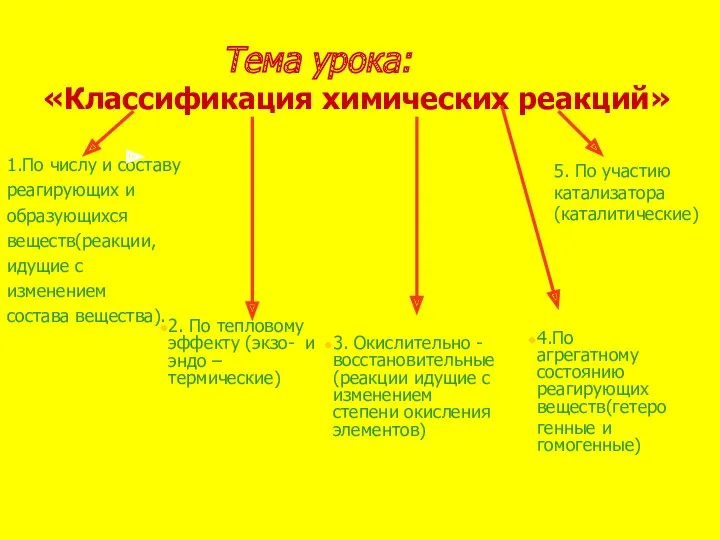
- 8. Тема урока: «Классификация химических реакций» 1.По числу и составу реагирующих и образующихся веществ(реакции, идущие с изменением
- 9. 2H2 + O2 → 2H2O CaO + H2O → Ca(OH)2 Cu(OH)2 → CuO + H2O; 2HgO
- 10. …Al +… O2 → …Al2O3 …P + …O2 → …P2O5 Na2O + SO3 → Na2SO4 Li2O
- 11. …Fe(OH)3 → Fe2O3 +… H2O …HgO → …Hg + O2 CaCO3 → CaO + CO2 …NO
- 12. CuCl2 + Fe → Cu + FeCl2 Cr2O3 + …Al → …Cr + Al2O3 Mg +
- 13. CuO + …HCl → CuCl2 + H2О BaCl2 + K2SO4 → BaSO4 + …KCl Что объединяет
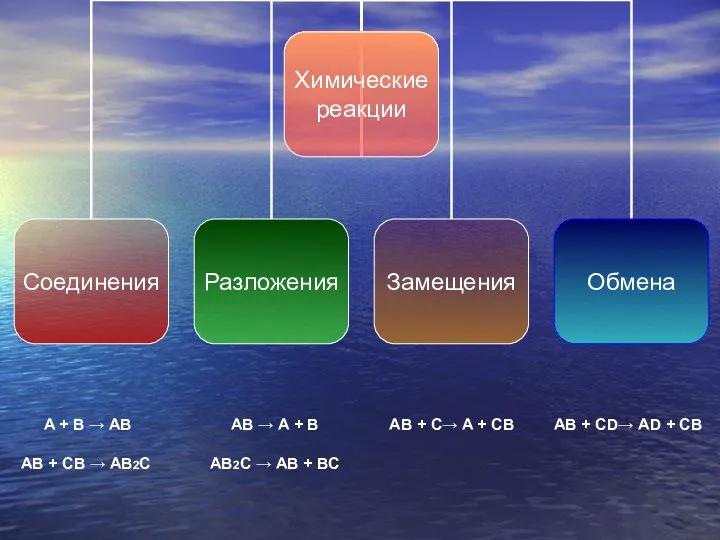
- 14. A + B → AB AB + CB → AB2C AB → A + B AB2C
- 15. Задания группам: Внимательно прочитайте инструктивную карточку по проведению опыта. Соблюдая технику безопасности проведите химическую реакцию. Определите
- 16. Уравнения к лабораторным опытам. 1. Zn +2HCl = ZnCl2 + H2 --- реакция замещения, выделяется газ
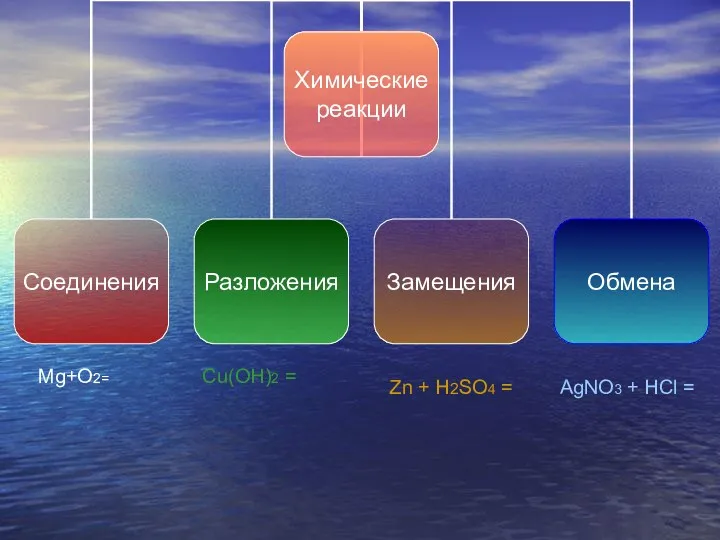
- 17. AgNO3 + HCl = Zn + H2SO4 = Cu(OH)2 = Mg+O2=
- 18. Проверим свои знания ! На листке с тестом запишите свою фамилию. Для заданий части А, правильные
- 20. Скачать презентацию














 Основы органической химии
Основы органической химии Получение металлов
Получение металлов Третья группа, главная подгруппа. 9 класс
Третья группа, главная подгруппа. 9 класс Современные химические технологии
Современные химические технологии Химические реакции
Химические реакции Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Цинк. Нахождение в природе
Цинк. Нахождение в природе Уральские самоцветы
Уральские самоцветы Нанотехнологии и Наноматериалы
Нанотехнологии и Наноматериалы Введение в геохимию
Введение в геохимию Ионный обмен. Хроматография
Ионный обмен. Хроматография Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Периодический закон химических элементов Д. И. Менделеева и периодическая система
Периодический закон химических элементов Д. И. Менделеева и периодическая система Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Буферные растворы
Буферные растворы Теория строения органических веществ. Предельные углеводороды. 9 класс
Теория строения органических веществ. Предельные углеводороды. 9 класс Галогенопроизводные углеводородов
Галогенопроизводные углеводородов Автомобильные бензины
Автомобильные бензины Методы защиты металлов от электрохимической коррозии. Классификация методов защиты бетона и железобетона
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты бетона и железобетона Радиогеохимия экзогенных процессов
Радиогеохимия экзогенных процессов Структура стекла
Структура стекла Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений
Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений Основные виды химических связей
Основные виды химических связей Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Техника безопасности на уроках химии
Техника безопасности на уроках химии Метал конструкциялық материалдар
Метал конструкциялық материалдар Минеральные воды
Минеральные воды