Содержание
- 2. Атомы каких элементов входят в состав всех органических веществ? А. углерода Б. углерода и водорода В.
- 3. Атомы каких элементов входят в состав всех органических веществ? Б. углерода и водорода
- 4. Какова электронная формула атома углерода в возбуждённом состоянии? А. 1s2 2s2 2p4 Б. 1s2 2s2 2p2
- 5. Какова электронная формула атома углерода в возбуждённом состоянии? В. 1s2 2s1 2p3
- 6. Какова валентность атома углерода в органических веществах? А. I Б. II В. III Г. IV
- 7. Какова валентность атома углерода в органических веществах? Г. IV
- 8. Какова валентность атома азота в органических веществах? А. II Б. III В. IV Г. V
- 9. Какова валентность атома азота в органических веществах? Б. III
- 10. Какое строение имеют большинство органических веществ? А. атомное Б. ионное В. металлическое Г. молекулярное
- 11. Какое строение имеют большинство органических веществ? Г. молекулярное
- 12. В молекуле какого вещества наиболее прочная химическая связь? А. F2 Б. Cl2 В. O2 Г. N2
- 13. В молекуле какого вещества наиболее прочная химическая связь? Г. N2
- 14. Кто является автором теории химического строения органических веществ? А. Бутлеров Б. Менделеев В. Кекуле Г. Берцелиус
- 15. Кто является автором теории химического строения органических веществ? А. Бутлеров
- 16. Предельные углеводороды Урок химии в 9 классе
- 17. Углеводороды (УВ) – органические вещества, состоящие только из атомов углерода и водорода
- 18. Предельные углеводороды – алканы, насыщенные углеводороды, парафины
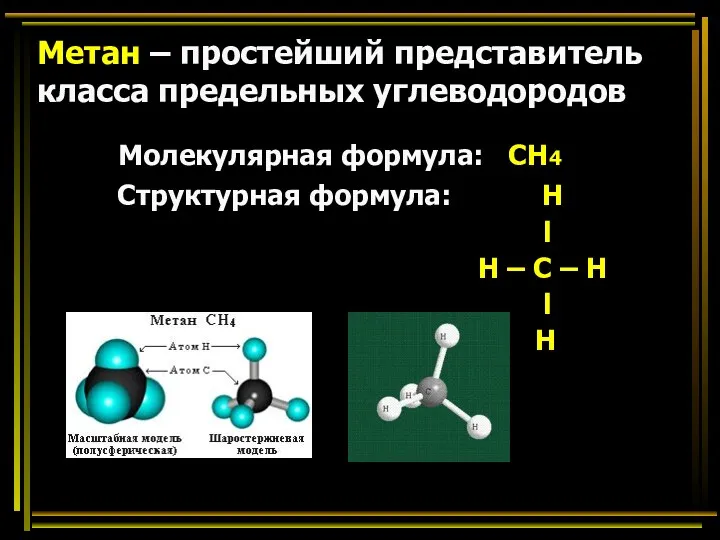
- 19. Метан – простейший представитель класса предельных углеводородов Молекулярная формула: СН4 Структурная формула: Н l Н –
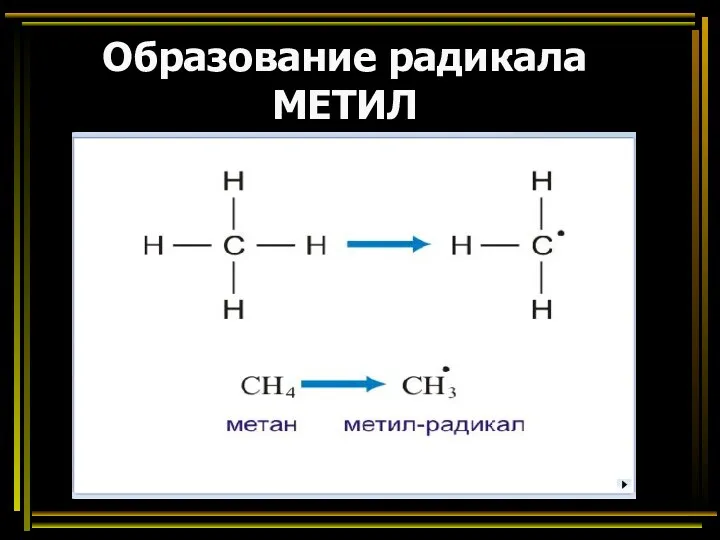
- 20. Образование радикала МЕТИЛ
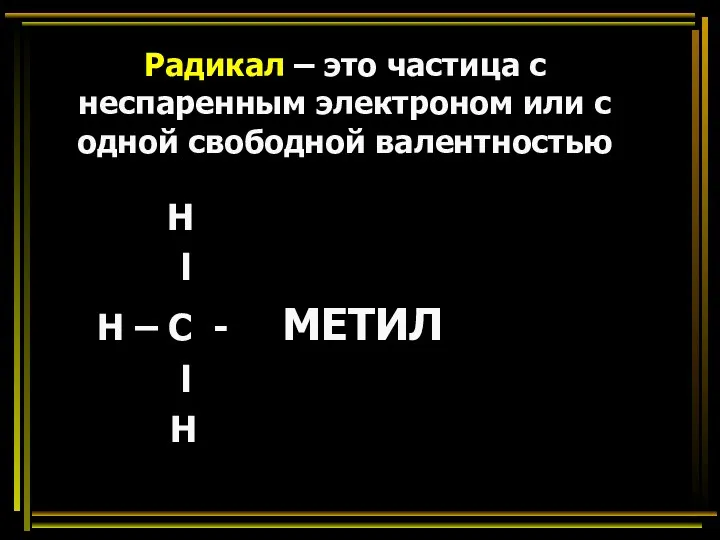
- 21. Радикал – это частица с неспаренным электроном или с одной свободной валентностью Н l Н –
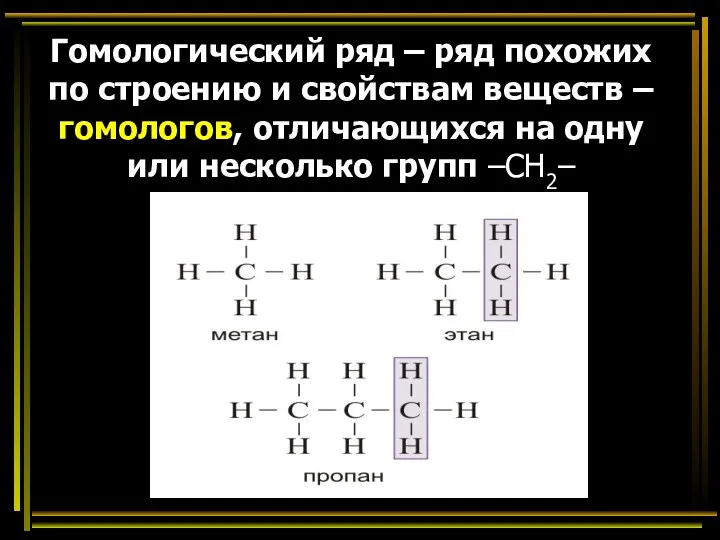
- 22. Гомологический ряд – ряд похожих по строению и свойствам веществ – гомологов, отличающихся на одну или
- 23. Алканы (предельные, насыщенные, парафины) – органические вещества, состоящие из атомов углерода и водорода, связанных между собой
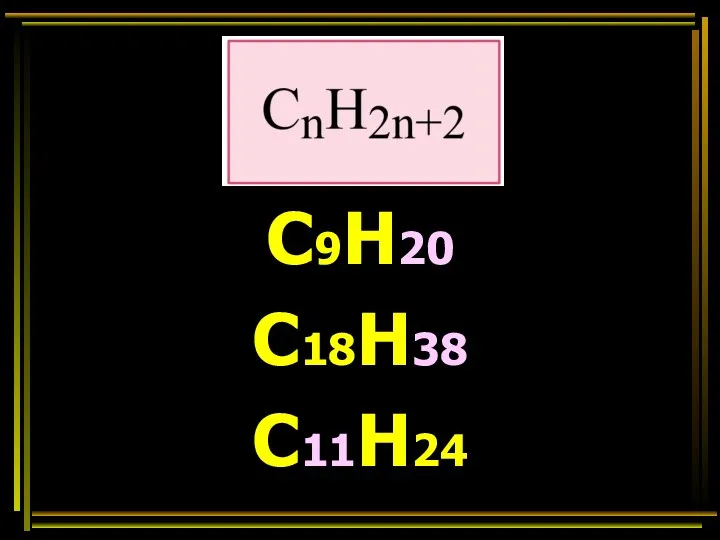
- 24. С9Н? С18Н? С?Н24
- 25. С9Н20 С18Н38 С11Н24
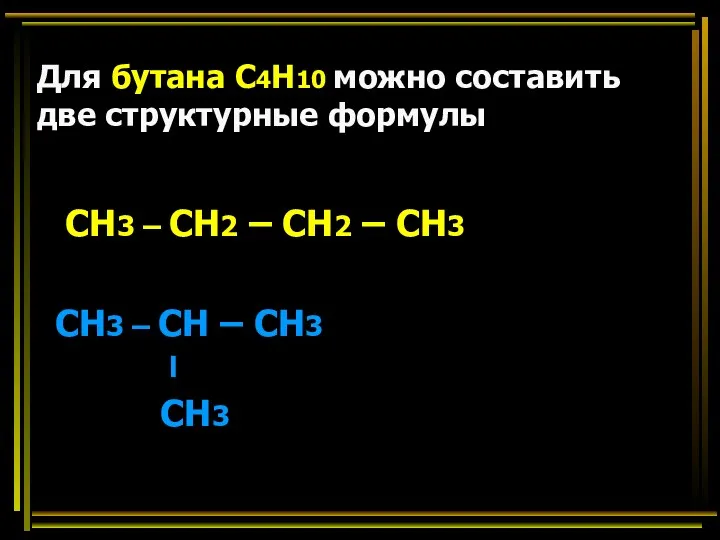
- 26. Для бутана С4Н10 можно составить две структурные формулы СН3 – СН2 – СН2 – СН3 СН3
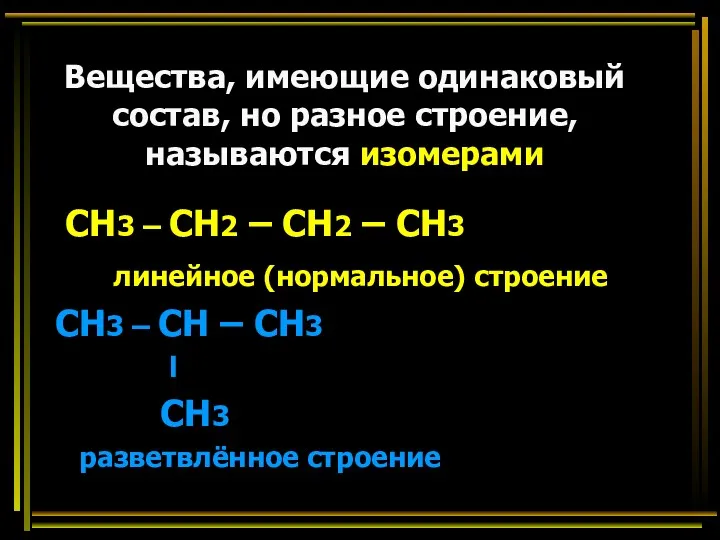
- 27. Вещества, имеющие одинаковый состав, но разное строение, называются изомерами СН3 – СН2 – СН2 – СН3
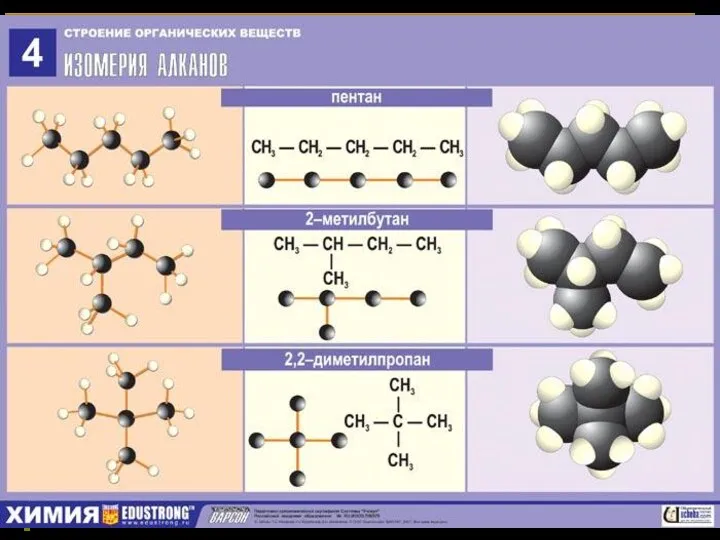
- 28. Изомерия, изомеры
- 29. Номенклатура алканов СН3 1 2l 3 4 СН3 – С – СН2 – СН3 l СН3
- 30. Изомеры пентана
- 31. Химические свойства алканов Реакция горения Реакция замещения c галогенами Реакция термического разложения – дегидрирования
- 32. Уравнение реакции горения метана
- 33. Нахождение в природе: Природный газ на 75%-85% состоит из метана, от 25%-2% этана, пропана и других
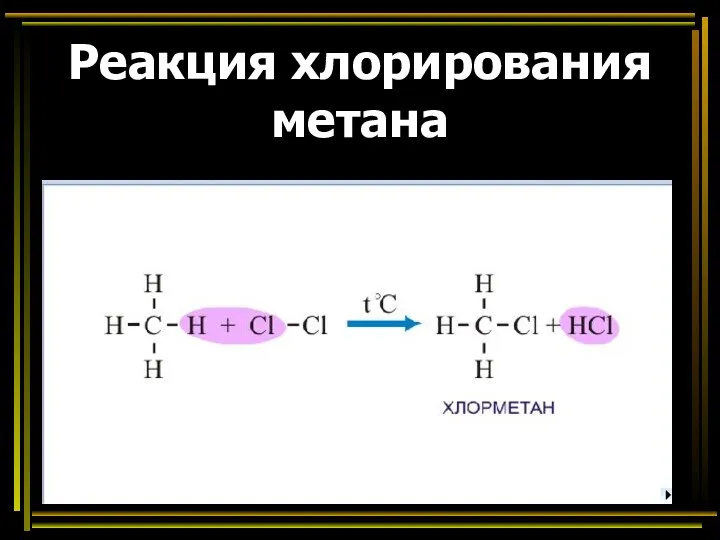
- 34. Реакция хлорирования метана
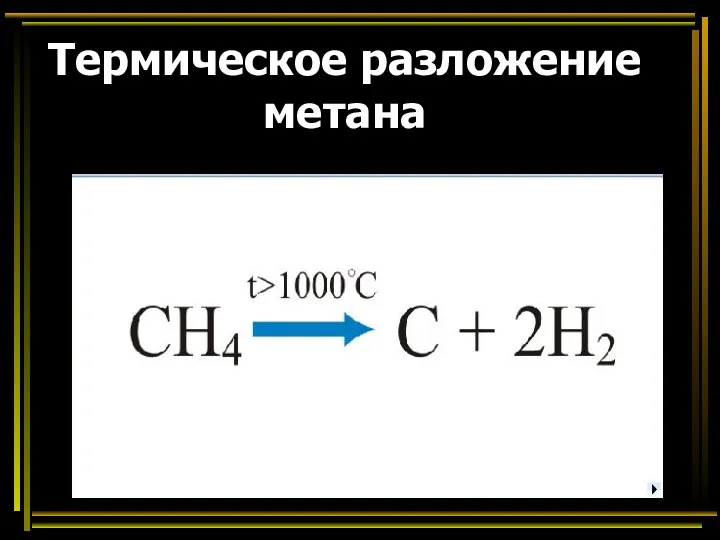
- 35. Термическое разложение метана
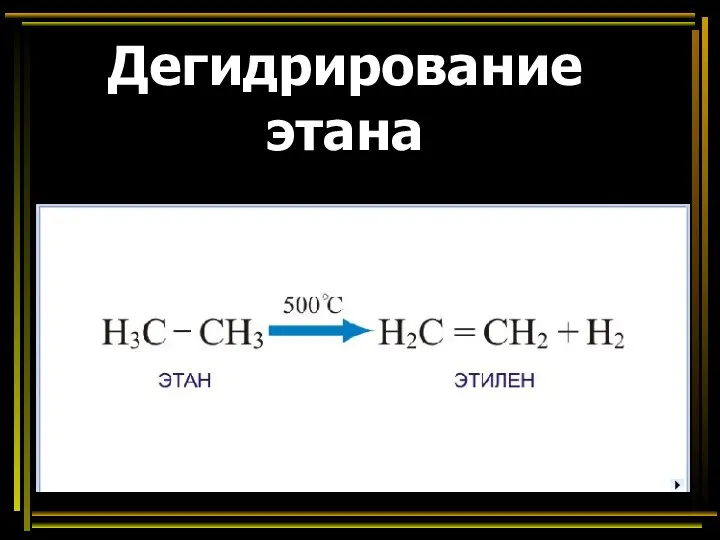
- 36. Дегидрирование этана
- 37. Учёные-химики, которые внесли вклад в изучение углеводородов Владимир Васильевич Марковников (1838-1904) Михаил Иванович Коновалов(1858 – 1906)
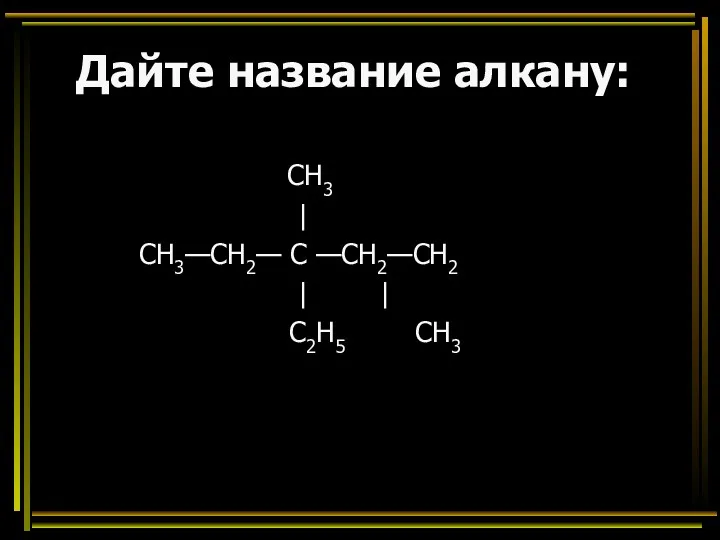
- 38. Дайте название алкану: CH3 | СН3—СН2— С —СН2—СН2 | | C2H5 CH3
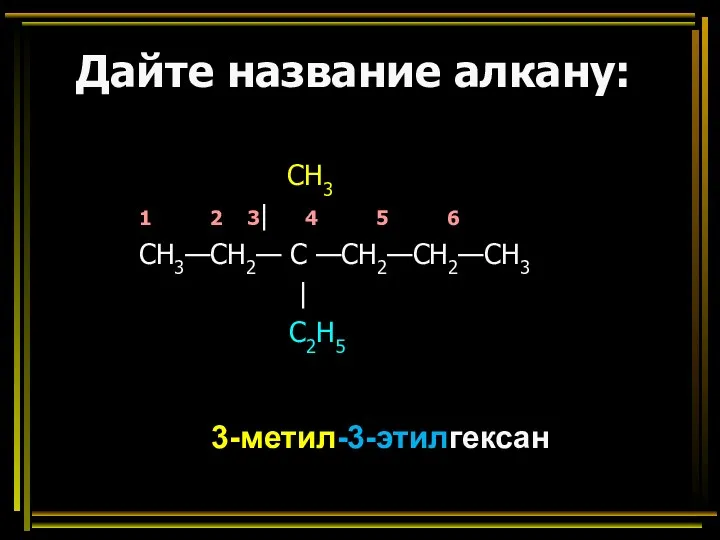
- 39. Дайте название алкану: CH3 1 2 3| 4 5 6 СН3—СН2— С —СН2—СН2—СН3 | C2H5 3-метил-3-этилгексан
- 40. Нефть – источник жидких углеводородов Нефть была известна ещё в античные времена и использовалась в основном
- 41. Нефть: ОПАСНОСТЬ!!! Подсчитано, что 200 тыс. тонн нефти достаточно, чтобы превратить все Балтийское море в биологическую
- 43. Скачать презентацию


























 Общая характеристика халькогенов. Кислород
Общая характеристика халькогенов. Кислород Нанохимия
Нанохимия Фосфор и его соединения. Электронные формулы атома фосфора
Фосфор и его соединения. Электронные формулы атома фосфора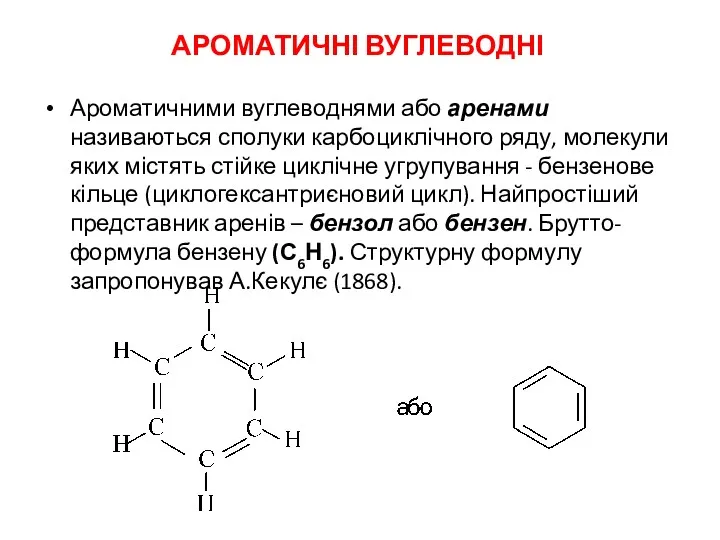 Ароматичні вуглеводні
Ароматичні вуглеводні Гидродинамические свойства полимеров. Полиэлектролиты
Гидродинамические свойства полимеров. Полиэлектролиты Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу
Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу Озон. Значение Озона
Озон. Значение Озона Обзор электродных процессов
Обзор электродных процессов Особенности химического состава клетки
Особенности химического состава клетки Хром. Элемент под № 24
Хром. Элемент под № 24 Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Аминокислоты. Белки
Аминокислоты. Белки Металлические стёкла
Металлические стёкла Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины)
Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины) Кислоты, основания, соли в свете ТЭД
Кислоты, основания, соли в свете ТЭД Практическая работа по разделению смесей
Практическая работа по разделению смесей Свинец
Свинец Кислородные соединения азота
Кислородные соединения азота Буферные растворы
Буферные растворы Основные классы неорганических веществ. Соединения химических элементов
Основные классы неорганических веществ. Соединения химических элементов Резина. Состав и применение резины
Резина. Состав и применение резины Аминокислоты. Понятие аминокислот
Аминокислоты. Понятие аминокислот АЛКАНЫ Строение молекулы метана.
АЛКАНЫ Строение молекулы метана. Растворы. Классификация, способы выражения концентрации, свойства растворов
Растворы. Классификация, способы выражения концентрации, свойства растворов 20230205_okislitelno-vosstanovitelnye_reaktsii
20230205_okislitelno-vosstanovitelnye_reaktsii Хімічні властивості оксидів
Хімічні властивості оксидів Электролиз. Электролизеры
Электролиз. Электролизеры Моделирование структуры биомакромолекул
Моделирование структуры биомакромолекул