Содержание
- 2. 7.1. Кислотность водных растворов и биологических жидкостей. 7.2 Буферные растворы. 7.3 Буферные системы крови. План
- 3. 7.1 Кислотность является важной характеристикой как водных растворов, так и биологических жидкостей. Она определяется соотношением концентраций
- 4. Для характеристики кислотности используется водородный показатель (рН) : рН = - lg[H+] - для слабых электролитов
- 5. Реже для характеристики реакции среды используется гидроксильный показатель (рОН): рОН = - lg[OH-] – для слабых
- 6. Для одного раствора рН + рОН = 14
- 7. Используя уравнение КW = [H+] [OH-] = 10-14, рассчитаем концентрации ионов в нейтральном растворе [H+] =
- 8. В кислой среде: [H+] > [OH-] рН 7 В щелочной среде: [H+] pH > 7, pOH
- 9. Шкала рН [Н+],M pH 1 10-5 10-7 10-9 10-14 0 5 7 9 14 Сильнокислая среда
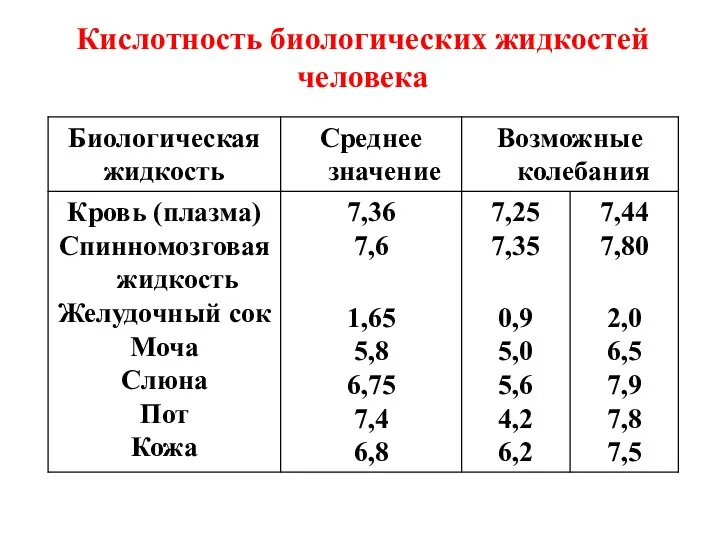
- 10. Кислотность биологических жидкостей человека
- 11. Для биологических жидкостей характерен кислотно-основной гомеостаз (постоянство значений рН), обусловленный действием биологических буферных систем.
- 12. Наиболее опасными видами нарушения кислотно-основного равновесия в крови являются: ацидоз – увеличение кислотности крови, алкалоз –увеличение
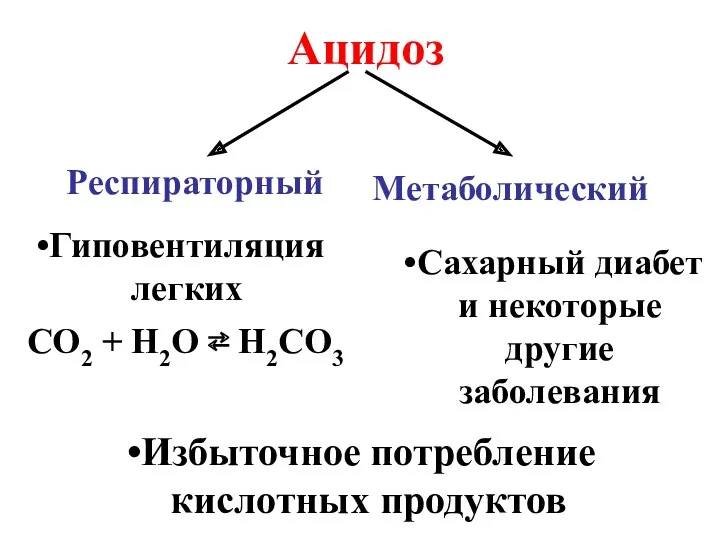
- 13. Ацидоз Респираторный Метаболический Гиповентиляция легких CO2 + H2O ⇄ H2CO3 Сахарный диабет и некоторые другие заболевания
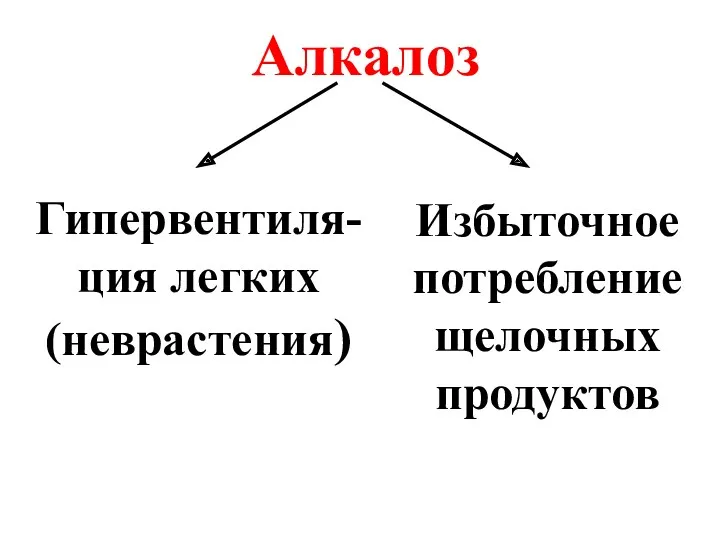
- 14. Алкалоз Гипервентиля-ция легких (неврастения) Избыточное потребление щелочных продуктов
- 15. Опасность изменения рН связана 1) со снижением активности ферментов и гормонов, активных в узком диапазоне рН;
- 16. 2) с изменением осмотического давления биологических жидкостей; 3) с изменением скорости биохимических реакций, катализируемых катионами Н+.
- 17. При изменении рН крови на 0,3 единицы может наступить тяжелое коматозное состояние, а 0,4 единицы -
- 18. Коррекция ацидоза - внутривенное введение 4%-ного раствора NaHCO3: HCO3- + H+ ⇄ H2CO3 Антацидными (гипоцидными) называются
- 19. Коррекция алкалоза- внутривенное введение растворов аскорбиновой кислоты (5% или 15%).
- 20. Повышение кислотности в ротовой полости связано с приемом пищи (особенно сладкой). При этом происходит разрушение зубной
- 21. Методы определения кислотности растворов 1. Кислотно-основное титрование. 2. Кислотно-основные индикаторы.
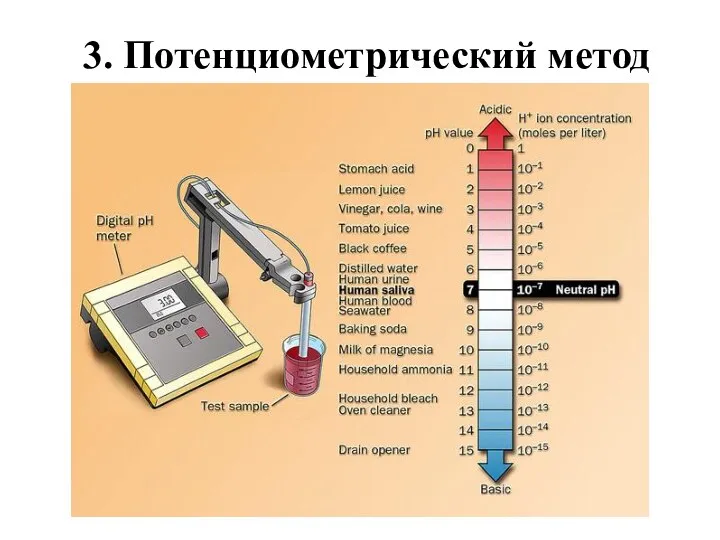
- 22. 3. Потенциометрический метод
- 23. 7.2 Буферными называют растворы, рН которых не изменяется при добавлении небольших количеств кислот или щелочей, а
- 24. Протолитическая теория кислот и оснований Бренстеда-Лоури (1923) объясняет механизм буферного действия. Согласно этой теории, кислота –
- 25. Различают: кислоты–молекулы (CH3COOH), кислоты-катионы (NH4+), кислоты–анионы (H2PO4-)
- 26. Каждая кислота сопряжена со своим основанием. Основание – это акцептор протонов.
- 27. Cопряженные пары кислот и оснований СH3COOH ⇄ CH3COO- + H+ Кислота Сопряженное основание
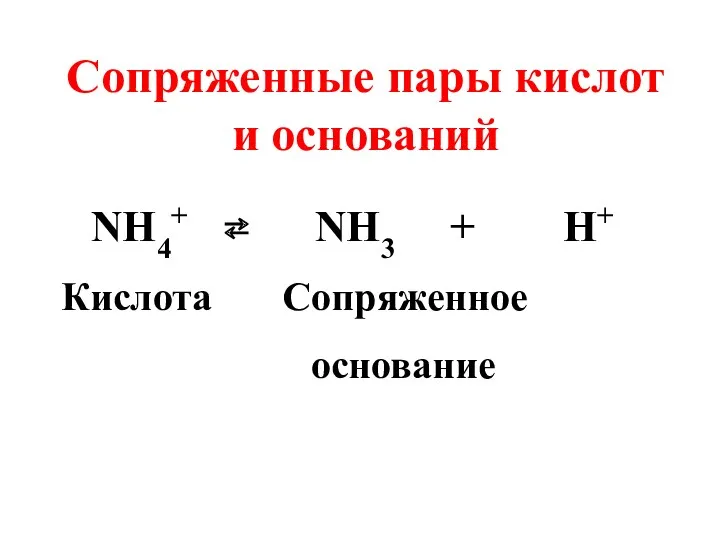
- 28. Cопряженные пары кислот и оснований NH4+ ⇄ NH3 + H+ Кислота Сопряженное основание
- 29. Cопряженные пары кислот и оснований H2PO4- ⇄ HPO42- + H+ Кислота Сопряженное основание
- 30. Буферный раствор содержит кислоту и сопряженное с ней основание. Именно поэтому он способен нейтрализовывать как добавленную
- 31. Классификация буферных растворов Ацетатный буфер: СН3СООН/СН3СООNa Механизм буферного действия НCl + CH3COONa ⇄ CH3COOH + NaCl
- 32. 2) Слабое основание/его соль Аммиачный буфер: NН3/NН4Сl Механизм буферного действия НCl + NH3 ⇄ NH4Cl Нейтрализация
- 33. 3) Две кислые соли Гидрофосфатный буфер : NаН2PO4/Nа2НPO4 Механизм буферного действия НCl + Na2HPO4 ⇄ NaH2PO4+
- 34. 4) кислая соль/средняя соль Карбонатный буфер: NаНСO3/Nа2СO3 Механизм буферного действия НCl + Na2СO3 ⇄ NaHСO3+ NaCl
- 35. Уравнение Гендерсона- Гассельбаха позволяет рассчитать рН буферного раствора: рН =рКа - lg [кислота] [сопряженное основание] _
- 36. Буферная емкость раствора (В, ммоль/л) - это количества сильных кислот или щелочей, при прибавлении которых к
- 37. Сн×V В = ----------------- , |рН - рНо| ×Vбр где Сн - нормальность добавляемых кислот или
- 38. Буферная емкость зависит: от концентрации: чем концентрированнее раствор, тем больше его буферная емкость; 2) от соотношения
- 39. Чем больше буферная емкость раствора, тем эффективнее он поддерживает кислотно - основное равновесие.
- 40. Характеристиками биологических буферных систем являются: Bк – буферная емкость по кислоте, Bщ – буферная емкость по
- 41. В организме человека в спокойном состоянии ежесуточно образуется количество кислоты, эквивалентное 2,5 л HCl (конц).
- 42. 7.3 Из буферных систем организма наибольшей емкостью характеризуются буферные системы крови, которые распределены между эритроцитами и
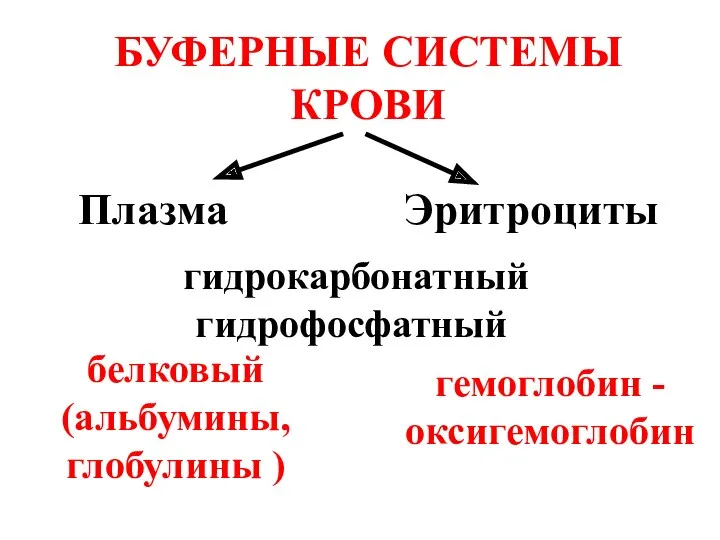
- 43. БУФЕРНЫЕ СИСТЕМЫ КРОВИ Плазма Эритроциты гидрокарбонатный гидрофосфатный белковый (альбумины, глобулины ) гемоглобин - оксигемоглобин
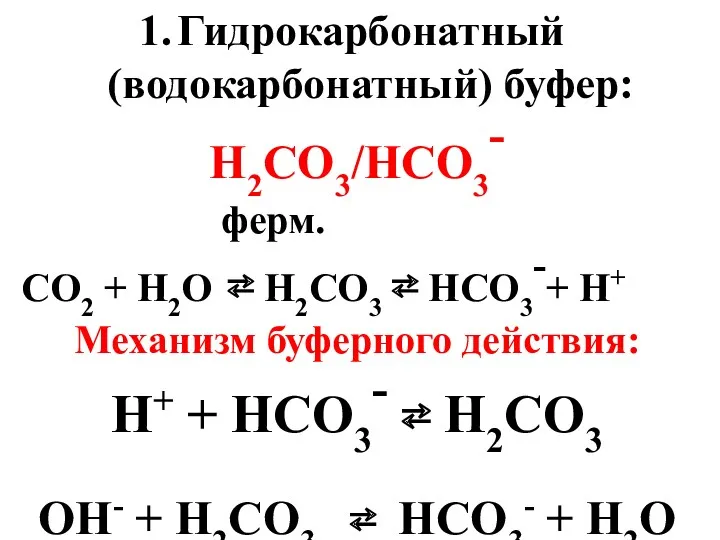
- 44. Гидрокарбонатный (водокарбонатный) буфер: H2CO3/HCO3- ферм. СО2 + Н2О ⇄ Н2СО3 ⇄ НСО3-+ Н+ Механизм буферного действия:
- 45. В крови [HCO3-] 40 [H2CO3] 1 избыток гидрокарбоната создает щелочной резерв крови Вк = 40 ммоль/л;
- 46. Гидрокарбонатный буфер связан со всеми буферными системами вне- и внутри-клеточных жидкостей. Всякие изменения в них сказываются
- 47. Анализируя содержание НСО3- в крови можно диагностировать наличие дыхательных и метаболических нарушений.
- 48. 2. Гидрофосфатная буферная система Н2PO4-/HPO42- Вк = 1-2 ммоль/л; Вщ = 0,5 ммоль/л Низкая буферная емкость
- 49. Однако эта система играет решающую роль в других биологических жидкостях: в моче, соках пищеварительных желез, а
- 50. 3.Гемоглобин-оксигемоглобин: ННb/Нb- ННb - слабая кислота (Ка = 6,37·10-9) Н+ + Нb- ⇄ ННb ОН- +
- 51. HHb + O2⇄ HHbO2 (Ка = 1,17·10-7) HHbO2/ HbO2- H+ + HbO2- ⇄ HHbO2 OH- +
- 52. Буферная система гемоглобин-оксигемоглобин обеспечивает 75% буферной емкости крови.
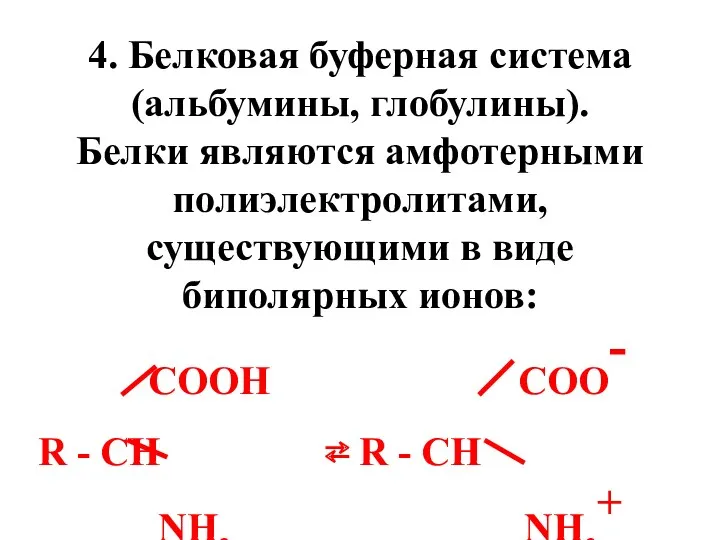
- 53. 4. Белковая буферная система (альбумины, глобулины). Белки являются амфотерными полиэлектролитами, существующими в виде биполярных ионов: COOH
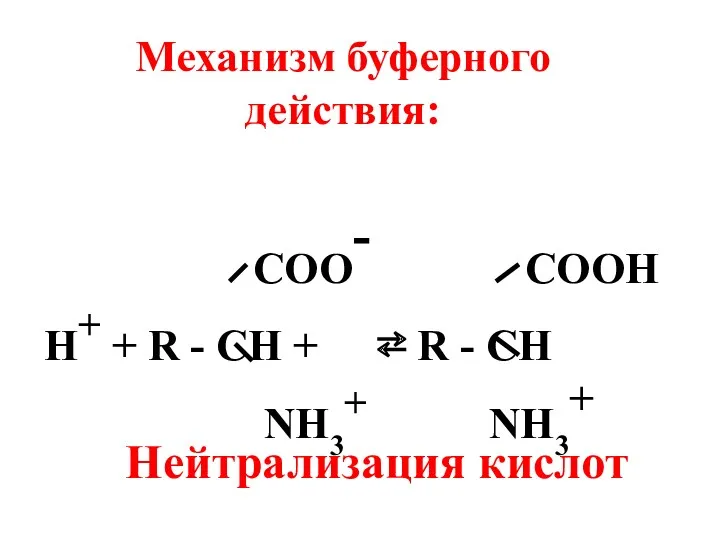
- 54. COO- COOH Н+ + R - CH + ⇄ R - CH NH3+ NH3+ Механизм буферного
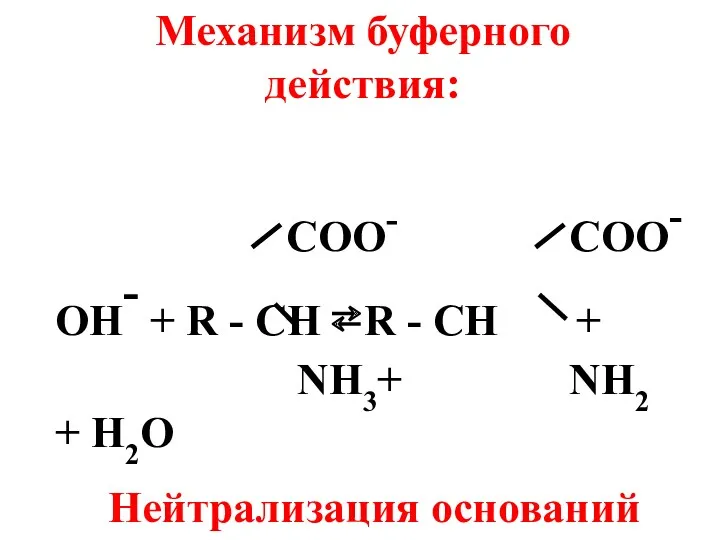
- 55. COO- COO- OH- + R - CH ⇄ R - CH + NH3+ NH2 + H2O
- 56. Вк (альбуминов) = 10 ммоль/л Вк (глобулинов) = 3 ммоль/л Белковые буферы содержатся не только в
- 57. Буферные системы организма обеспечивают кислотно-основной гомеостаз человека.
- 59. Скачать презентацию





![Используя уравнение КW = [H+] [OH-] = 10-14, рассчитаем концентрации](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366964/slide-6.jpg)
![В кислой среде: [H+] > [OH-] рН 7 В щелочной среде: [H+] pH > 7, pOH](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366964/slide-7.jpg)
![Шкала рН [Н+],M pH 1 10-5 10-7 10-9 10-14 0](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366964/slide-8.jpg)




























![В крови [HCO3-] 40 [H2CO3] 1 избыток гидрокарбоната создает щелочной](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366964/slide-44.jpg)





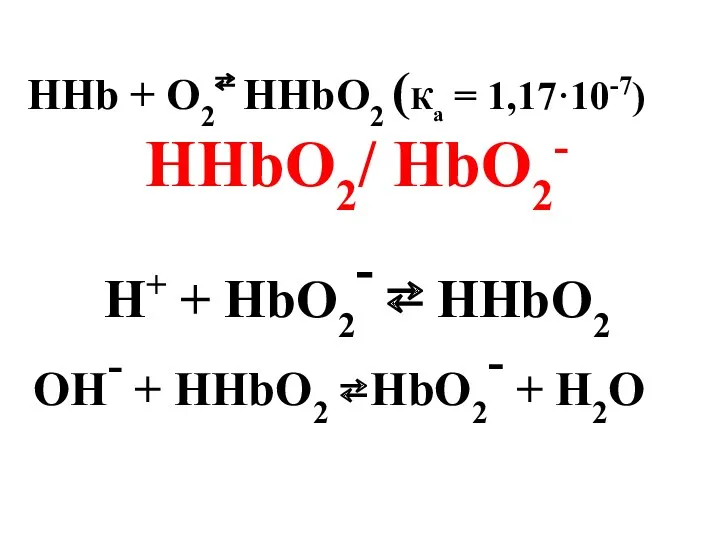



 Азот. Характеристика азота, фосфора (9класс)
Азот. Характеристика азота, фосфора (9класс) Обчислення за хімічними рівняннями відносного виходу продукту реакції
Обчислення за хімічними рівняннями відносного виходу продукту реакції МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс
МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс Тағам қоспалары
Тағам қоспалары Кaрбоновые кислоты
Кaрбоновые кислоты Индикаторные ошибки кислотно-основного титрования
Индикаторные ошибки кислотно-основного титрования Кислотно-основное титрование
Кислотно-основное титрование Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Карбоновые кислоты. Уксусная кислота
Карбоновые кислоты. Уксусная кислота Подгруппа меди. Элементы 11 группы (Cu,Ag,Au)
Подгруппа меди. Элементы 11 группы (Cu,Ag,Au) Кремний и его соединения
Кремний и его соединения Хроматографические методы анализа
Хроматографические методы анализа Магматические горные породы
Магматические горные породы Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Химические свойства спиртов. Химические свойства предельных одноатомных спиртов
Химические свойства спиртов. Химические свойства предельных одноатомных спиртов Чистые вещества и смеси
Чистые вещества и смеси Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Характеристика элементов VIII-В группы. Семейство железа
Характеристика элементов VIII-В группы. Семейство железа Щелочные металлы и их соединения. 9 класс
Щелочные металлы и их соединения. 9 класс Основные интермедиаты в органических реакциях. Часть 1
Основные интермедиаты в органических реакциях. Часть 1 Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление Вуглеводи прості і складні
Вуглеводи прості і складні Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества
Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества Удобрения и их классификация
Удобрения и их классификация Кислоты НСL, H2 O, H2 CO3
Кислоты НСL, H2 O, H2 CO3 Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях АЛКАНЫ Строение молекулы метана.
АЛКАНЫ Строение молекулы метана. Индикаторы. Круговорот воды в природе. Загрязнение природных вод. Охрана и очистка природных вод
Индикаторы. Круговорот воды в природе. Загрязнение природных вод. Охрана и очистка природных вод