Слайд 2

Водородная ошибка возникает, когда недотитрована сильная кислота, перетитровано сильное или слабое
основание
Водородная ошибка – отношение количества ионов водорода n(H+) в конце титрования к первоначально взятому количеству вещества n(X)
n(H+)к.т.
X(H+) = ———— · 100%
n(X)
Слайд 3

n(X) = Сэкв(Х) · V(X)
Сэкв(Х) – молярная концентрация эквивалента первоначально взятого
вещества
V(X) – объем первоначально взятого вещества
n(H+)к.т. = [H+]к.т.· Vк.т.
Vк.т. – объем в конце титрования
Vк.т. = V(X) + V(Т)
Слайд 4
![[H+]к.т.· (V(X) + V(Т)) X(H+) = ——————————— · 100% С(1/z](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-3.jpg)
[H+]к.т.· (V(X) + V(Т))
X(H+) = ——————————— · 100%
С(1/z Х) ·
V(X)
рНк.т. = рТInd
[H+]к.т = 10–рН = 10–рТ
10–рТ · (V(X) + V(Т))
X(H+) = ————————— · 100%
Сэкв(Х) · V(X)
Слайд 5

Гидроксильная ошибка обусловлена наличием гидроксид-ионов в конце титрования и возни-кает, когда
недотитровано сильное основание, перетитрована сильная или слабая кислота
n(OH–)к.т.
X(OH–) = ———— · 100%
n(X)
n(OH–)к.т = [OH–]к.т. · (V(X) + V(Т))
n(X) = Сэкв(Х) · V(X)
[OH–]к.т. · (V(X) + V(Т))
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
Слайд 6
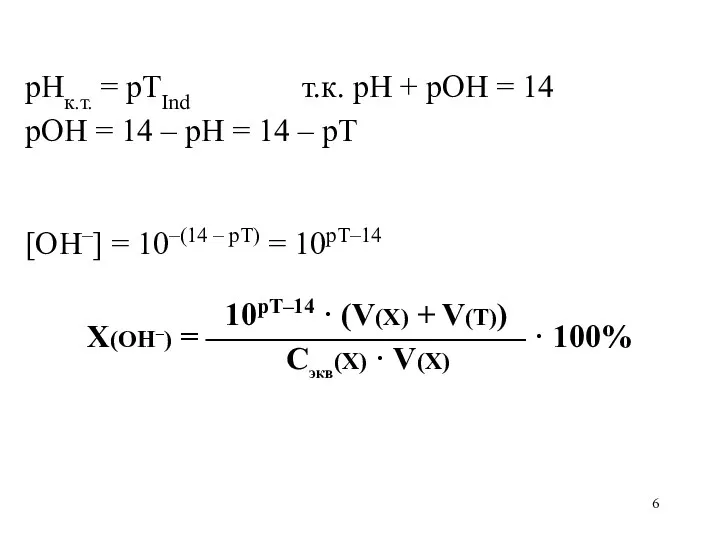
рНк.т. = рТInd т.к. рН + рОН = 14
рОН = 14
– рН = 14 – рТ
[OH–] = 10–(14 – рТ) = 10рТ–14
10рТ–14 · (V(X) + V(Т))
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
Слайд 7

Кислотная ошибка возникает, когда остается недотитрованной слабая кислота
Кислотная ошибка – отношение
концентрации недотитрованной кислоты в конце титрования к ее оттитрованной части
HA + KOH → H2O + KA
[HA]к.т.
X(HA) = ———— · 100%
[A–]к.т.
Оттитрованная часть кислоты будет определяться анионами соли
Слайд 8
![HAк.т. ↔ H+к.т. + A–к.т. [H+]к.т. · [A–]к.т. Kк-ты =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-7.jpg)
HAк.т. ↔ H+к.т. + A–к.т.
[H+]к.т. · [A–]к.т.
Kк-ты
= ———————
[HA]к.т.
[HA]к.т. [H+]к.т.
———= ———
[A–]к.т. Kк-ты
[H+]к.т.
X(HA) = ———— · 100%
Kк-ты
Слайд 9
![рНк.т. = рТInd [H+]к.т = 10–рН = 10–рТ Kк-ты =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-8.jpg)
рНк.т. = рТInd
[H+]к.т = 10–рН = 10–рТ Kк-ты = 10–рК
10–рТ
X(HA)
= ———— · 100%
10–рКк-ты
X(HA) =10рКк-ты–рТ · 100%
Слайд 10

Основная ошибка возникает, когда остается недотитрованным слабое основание
Основная ошибка – отношение
концентрации неоттитрованного основания в конце титрования к его оттитрованной части
[BOH]к.т.
X(BOH) = ———— · 100%
[B+]к.т.
Слайд 11
![Аналогично с кислотной ошибкой можно показать [BOH]к.т. [OH–]к.т. ————— =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-10.jpg)
Аналогично с кислотной ошибкой можно показать
[BOH]к.т. [OH–]к.т.
————— =
—————
[B+]к.т. Kосн
[OH–]к.т.
X(BOH) = ———— · 100%
Kосн
Т.к. [OH–]к.т. = 10рТ–14 Kосн = 10–рКосн
Слайд 12
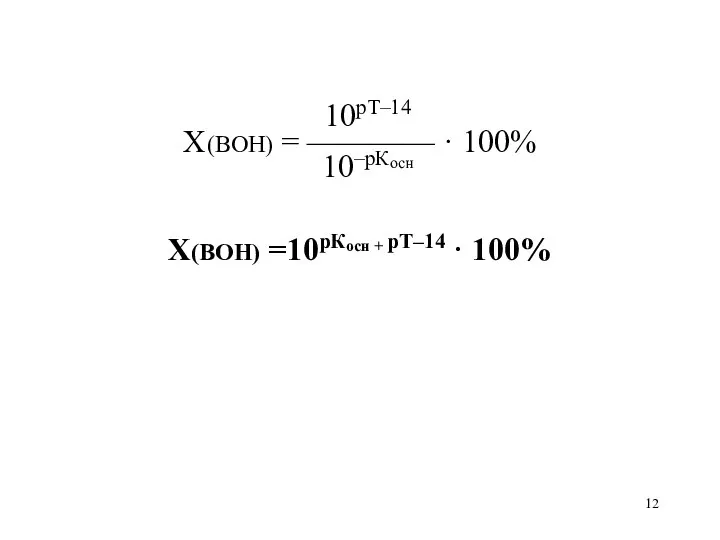
10рТ–14
X(BOH) = ———— · 100%
10–рКосн
X(BOH) =10рКосн + рТ–14 ·
100%
Слайд 13

Вычислить ошибку титрования 0,2 н. раствора HCl 0,2 н. раствором NaOH
с индикатором метиловым оранжевым.
рТ(м/о) = 4 ⇒ ошибка водородная
10–рТ · (V(X) + V(Т))
X(H+) = ————————— · 100%
Сэкв(Х) · V(X)
10–4 · (10 + 10)
X(H+) = ——————— · 100 = 0,1%
0,2 · 10
Индикаторная ошибка должна быть ≤ 0,1%
Слайд 14

Вычислить индикаторную ошибку титрования 0,2 н. раствора HCl 0,2 н. раствором
NaOH с индикатором фенолфталеином
рТ(ф/ф) = 9 ⇒ ошибка гидроксильная
10рТ–14 · (V(X) + V(Т))
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
109–14 · (10 + 10)
X(OH–) = ——————— · 100 = 0,01 %
0,2 · 10
Слайд 15

Вычислить ошибку титрования 0,1 н. раствора муравьиной кислоты 0,1 н. раствором
силь-ного основания с индикатором метиловым красным
рТ(м/к) = 5 рК(HCOOH) = 3,76
рНт.э. = 7 + ½ рКк-ты + ½ lg Cсоли = 8,38
Раствор недотитрован ⇒ ошибка кислотная
Слайд 16

X(HA) =10рКк-ты–рТ · 100%
X(HA) =103,76–5 · 100 = 5,7 %
Индикатор использовать
нельзя.


![[H+]к.т.· (V(X) + V(Т)) X(H+) = ——————————— · 100% С(1/z](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-3.jpg)

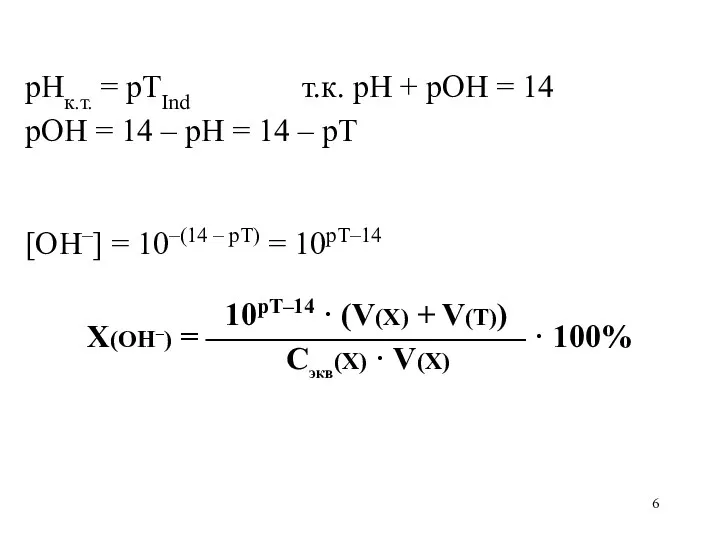

![HAк.т. ↔ H+к.т. + A–к.т. [H+]к.т. · [A–]к.т. Kк-ты =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-7.jpg)
![рНк.т. = рТInd [H+]к.т = 10–рН = 10–рТ Kк-ты =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-8.jpg)

![Аналогично с кислотной ошибкой можно показать [BOH]к.т. [OH–]к.т. ————— =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/362205/slide-10.jpg)




 Ковалентний зв’язок, його утворення
Ковалентний зв’язок, його утворення Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Неметаллы. Элементы V группы
Неметаллы. Элементы V группы Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Как трудно быть особенной…
Как трудно быть особенной… Агрегатні стани речовини
Агрегатні стани речовини Масс-Спектроскопия
Масс-Спектроскопия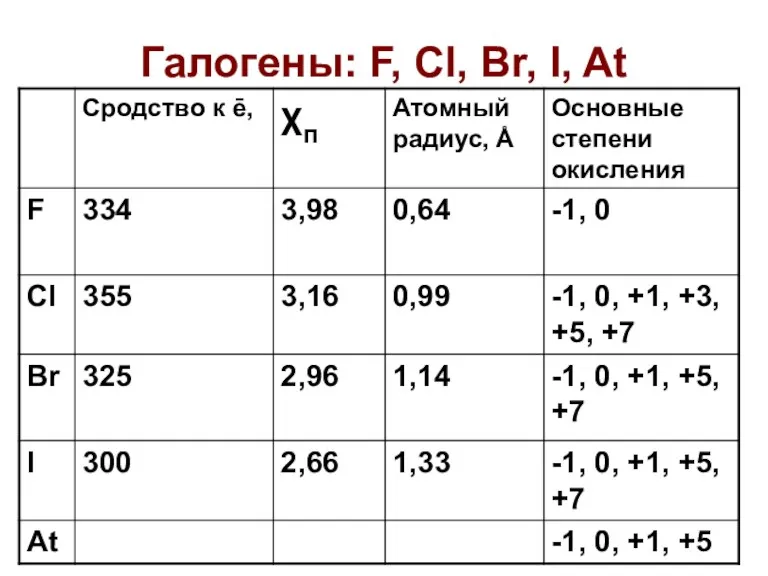 Галогены: F, Cl, Br, I, At
Галогены: F, Cl, Br, I, At Простые вещества – неметаллы. Аллотропия
Простые вещества – неметаллы. Аллотропия Кисень та хімічні властивості кисню. 7 клас
Кисень та хімічні властивості кисню. 7 клас Массовая доля химического элемента
Массовая доля химического элемента Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Дисперсные системы: общая характеристика и классификация
Дисперсные системы: общая характеристика и классификация Сернистый газ. Сернистая кислота и её соли
Сернистый газ. Сернистая кислота и её соли Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Оксид фосфора(V). Ортофосфорная кислота и ее соли. Минеральные удобрения
Оксид фосфора(V). Ортофосфорная кислота и ее соли. Минеральные удобрения Багатоатомні насичені спирти. Фізичні та хімічні властивості
Багатоатомні насичені спирти. Фізичні та хімічні властивості Теория электролитической диссоциации
Теория электролитической диссоциации Алкены. Пропилен (пропен)
Алкены. Пропилен (пропен) Гидролиз солей
Гидролиз солей Ионоселективные электроды
Ионоселективные электроды Определение нефтепродуктов в воде с использованием Флюората-02-5М
Определение нефтепродуктов в воде с использованием Флюората-02-5М Тест по неорганической химии
Тест по неорганической химии Аммиак. 9 класс
Аммиак. 9 класс Железо и его свойства
Железо и его свойства Свойства природного газа
Свойства природного газа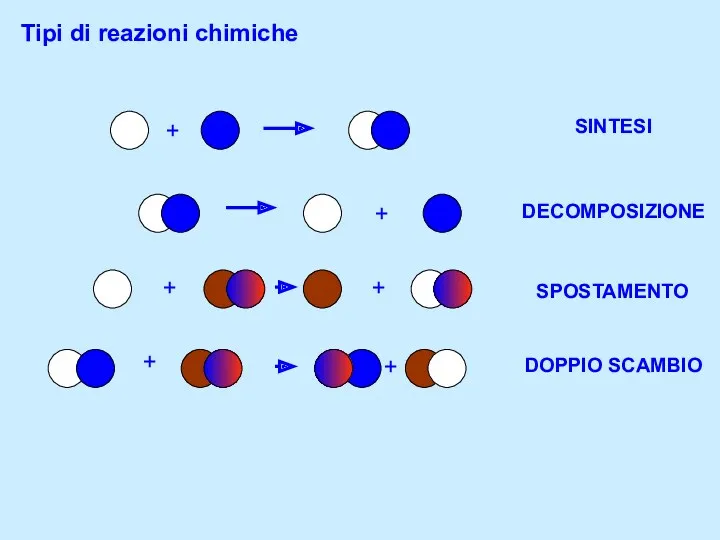 Tipi di reazioni chimiche
Tipi di reazioni chimiche Второй закон термодинамики. Биоэнергетика
Второй закон термодинамики. Биоэнергетика