Содержание
- 2. Мыла – это натриевые или калиевые соли высших карбоновых кислот: пальмитиновой, стеариновой, олеиновой, лауриновой. Что такое
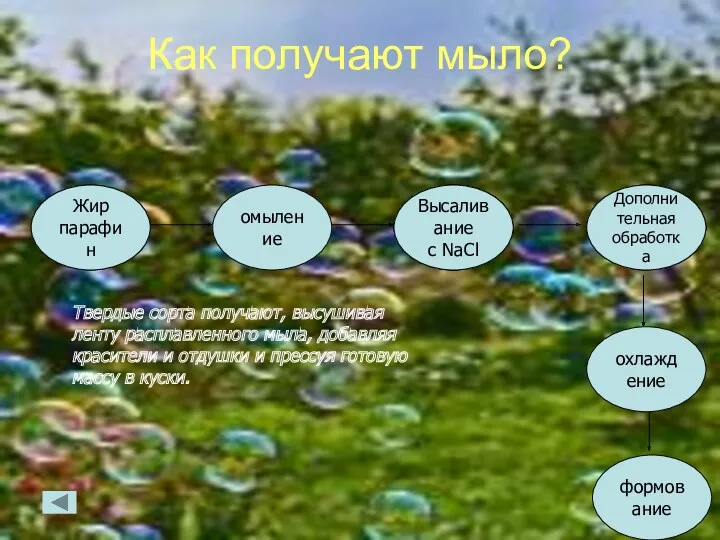
- 3. Как получают мыло? Жир парафин омыление Жир парафин Высаливание с NaCl Высаливание с NaCl Высаливание с
- 4. Омыление. В результате омыления образуется ядровое мыло из которого изготавливают хозяйственное и туалетное мыло. С3Н5(С13Н35СОО)3+3NaOH 3C17H35
- 5. Хозяйственное мыло. Твердые хозяйственные мыла в зависимости от сорта содержат 40-72% основного вещества, 0,1-0,2% свободной щелочи,
- 6. Туалетное мыло. Получают путем дополнительной обработки ядрового мыла с добавлением: красителей, антисептиков, талька, соды, каолина, душистых
- 7. Моющее действие мыла. Молекулы мыла прикрепляются к мицоле(грязный жир) и удаляет ее.
- 8. Недостатки мыла. Не отстирывает в жесткой воде. Мало пенится.
- 9. Синтетические моющие средства. Синтетические моющие средства - это натриевые соли кислых сложных эфиров высших спиртов и
- 10. Получение СМС. R-CH2-OH + H-O-SO2-OH=R-CH2-O-SO2-OH + H2O R-CH2-O-SO2-OH + NaOH=R-CH2-O-SO2-ONa + H2O
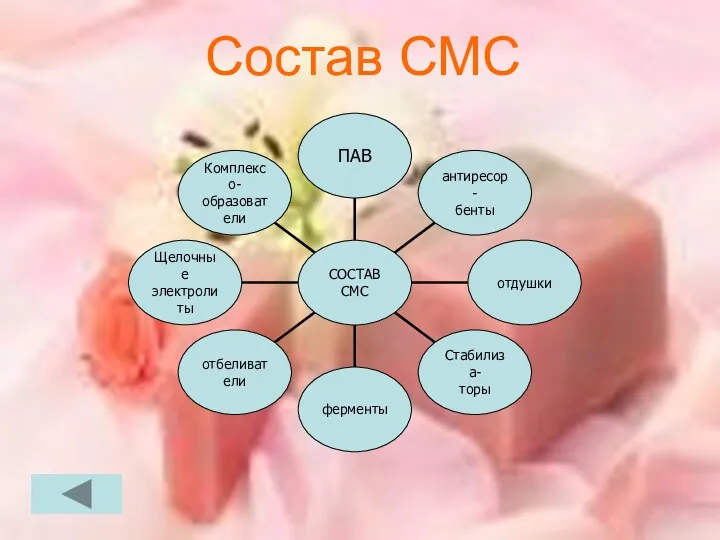
- 11. Состав СМС
- 12. ДЛЯ ЧЕГО НУЖНЫ СОСТАВНЫЕ ЧАСТИ СМС. Катионоактивные ПАВ-обладает, кромеиоющего, еще и дезинфицирующим действием. Неионогенные ПАВ образуют
- 13. 3. Щелочное отбеливание(процесс гидролиза)-это реакция обменного разложения веществ водой. Рассмотрим подробнее гидролиз слабой кислоты-Na2CO3 –карбонат натрия.
- 14. 4.отбеливатели-для удаления цветных загрязнений, оставщихся после стирки, и отбеливания. 5.отдушки-впринципе не имеет отношение к стирке, а
- 15. Вывод: Вообще говоря, для стирки можно использовать разные средства: в каких-то случаях подойдет и мыло, и
- 17. Скачать презентацию












 Инструментальные методы исследования органических веществ
Инструментальные методы исследования органических веществ III А – топтың элементтері
III А – топтың элементтері Удивительные свойства воды
Удивительные свойства воды Гидролиз солей (11 класс)
Гидролиз солей (11 класс) Кристаллизация. Структура жидких металлов
Кристаллизация. Структура жидких металлов Глюкоза. Хімічні властивості глюкози. Сахароза, гідроліз
Глюкоза. Хімічні властивості глюкози. Сахароза, гідроліз Алкены. Строение алкенов, характерные типы химических реакций
Алкены. Строение алкенов, характерные типы химических реакций Кремнийдің құрамы, құрылысы және қасиеттері
Кремнийдің құрамы, құрылысы және қасиеттері Защита от коррозии каменных и бетонных строительных материалов и конструкций
Защита от коррозии каменных и бетонных строительных материалов и конструкций Химиялық элемент оттегі
Химиялық элемент оттегі Теплота горения
Теплота горения Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Фенолдар, аминдер, альдегидтер
Фенолдар, аминдер, альдегидтер СФ- И ЯМР-ИССЛЕДОВАНИЕ РЕДОКС-ПРОЦЕССОВ В СИСТЕМЕ Со(II)-ЭДТА-H2O2
СФ- И ЯМР-ИССЛЕДОВАНИЕ РЕДОКС-ПРОЦЕССОВ В СИСТЕМЕ Со(II)-ЭДТА-H2O2 Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Некоторые d-элементы
Некоторые d-элементы Пенообразование в растворах поверхностно-активных веществ. Лекция 13
Пенообразование в растворах поверхностно-активных веществ. Лекция 13 Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Неоднородные системы, их классификация, методы разделения. Лекция 4
Неоднородные системы, их классификация, методы разделения. Лекция 4 Химические свойства солей
Химические свойства солей Хімічні явища, їх ознаки
Хімічні явища, їх ознаки Особенности органических веществ. Классификация органических соединений. 9 класс
Особенности органических веществ. Классификация органических соединений. 9 класс Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла
Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла Алюминий. Определите элемент
Алюминий. Определите элемент 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft 20231028_kislorod
20231028_kislorod Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов