Содержание
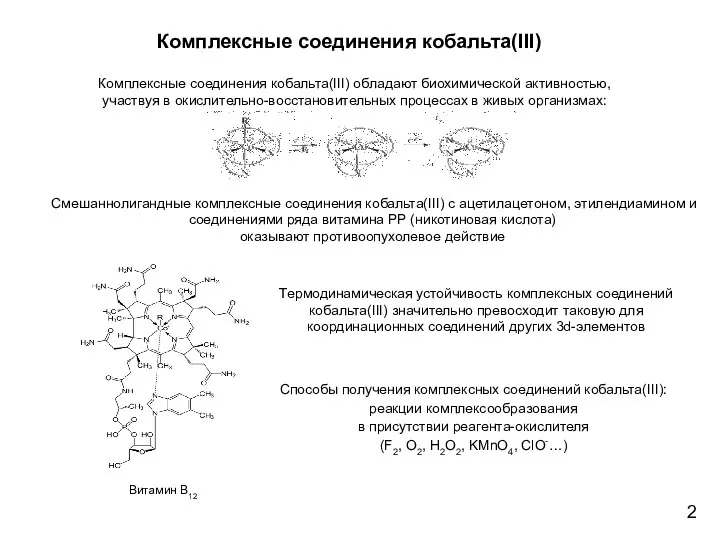
- 2. Комплексные соединения кобальта(III) Комплексные соединения кобальта(III) обладают биохимической активностью, участвуя в окислительно-восстановительных процессах в живых организмах:
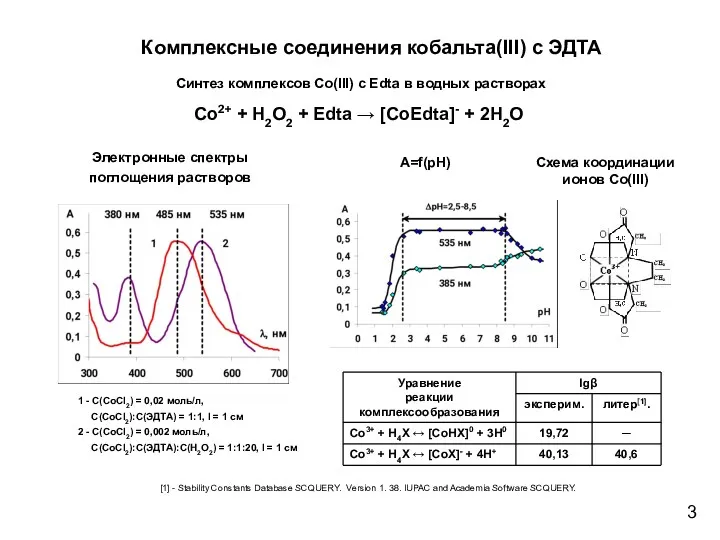
- 3. Комплексные соединения кобальта(III) с ЭДТА Co2+ + H2O2 + Edta → [CoEdta]- + 2H2O Синтез комплексов
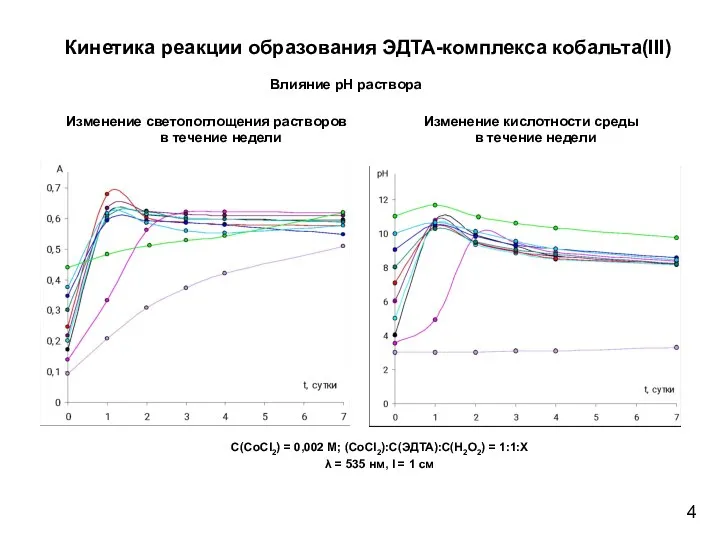
- 4. Кинетика реакции образования ЭДТА-комплекса кобальта(III) Влияние рН раствора Изменение кислотности среды в течение недели Изменение светопоглощения
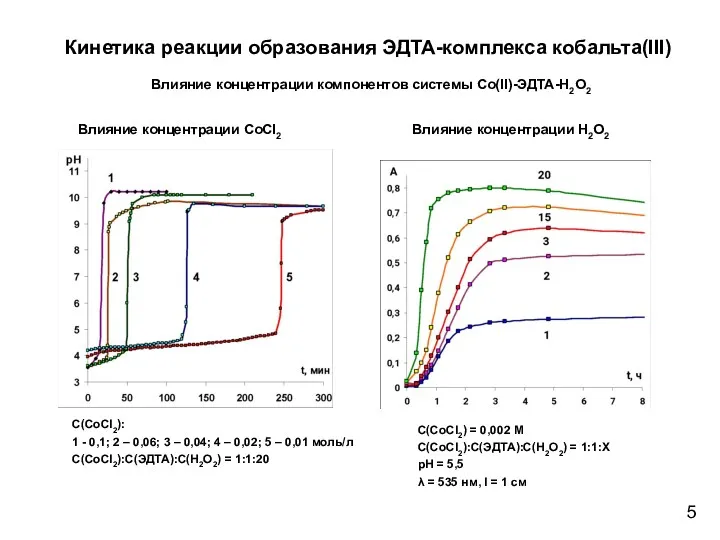
- 5. Кинетика реакции образования ЭДТА-комплекса кобальта(III) Влияние концентрации компонентов системы Co(II)-ЭДТА-Н2О2 Влияние концентрации CoСl2 Влияние концентрации H2O2
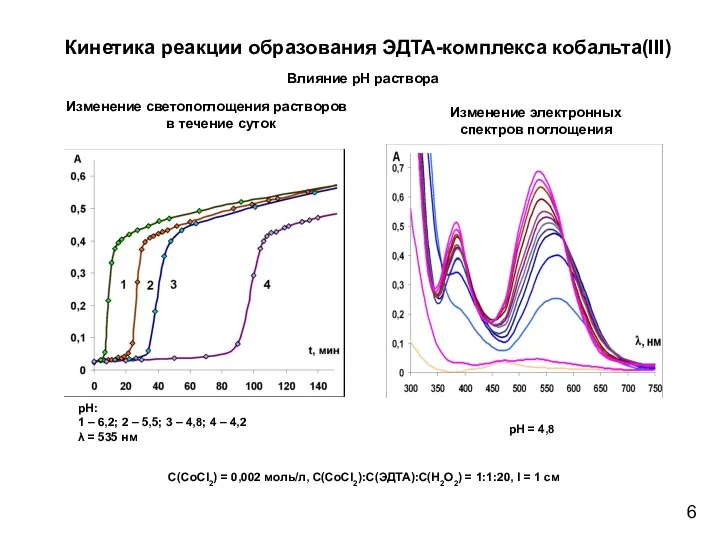
- 6. Кинетика реакции образования ЭДТА-комплекса кобальта(III) Влияние рН раствора Изменение электронных спектров поглощения Изменение светопоглощения растворов в
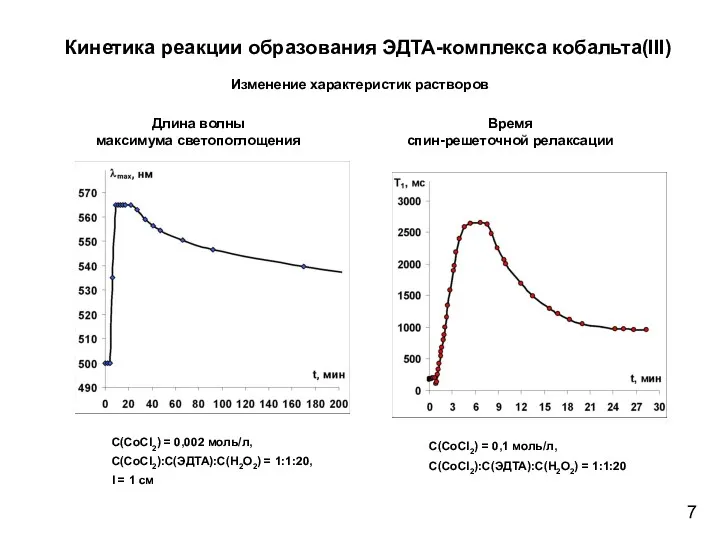
- 7. Кинетика реакции образования ЭДТА-комплекса кобальта(III) Изменение характеристик растворов Время спин-решеточной релаксации Длина волны максимума светопоглощения С(СoCl2)
- 8. Co2+ + ЭДТА4- → [CoЭДТА]2- [CoЭДТА]2- + H2O2 → [CoЭДТА]- + 2OH- 2H2O2 O2 + 2H2O
- 10. Скачать презентацию
![Co2+ + ЭДТА4- → [CoЭДТА]2- [CoЭДТА]2- + H2O2 → [CoЭДТА]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/311886/slide-7.jpg)
 Полимеры, их классификации и способы получения
Полимеры, их классификации и способы получения Эластомеры (резины)
Эластомеры (резины) Щелочные металлы
Щелочные металлы Закон сохранения массы вещества
Закон сохранения массы вещества Применение жиров
Применение жиров Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях Инструментальные методы исследования органических веществ
Инструментальные методы исследования органических веществ B-окисление жирных кислот и кетогенез
B-окисление жирных кислот и кетогенез Коллигативные свойства растворов
Коллигативные свойства растворов Аквамарин
Аквамарин Химия в повседневной жизни человека
Химия в повседневной жизни человека Кластер Химические реакции
Кластер Химические реакции Геохимия изотопов стабильных элементов
Геохимия изотопов стабильных элементов Обобщающий урок по теме Металлы
Обобщающий урок по теме Металлы Теоретичні основи неорганічного синтезу
Теоретичні основи неорганічного синтезу Высокомолекулярные соединения и супрамолекулярные структуры. Синтез полимеров (Лекция 1)
Высокомолекулярные соединения и супрамолекулярные структуры. Синтез полимеров (Лекция 1) Топливо. Загрязнения воздуха, способы его предотвращения. Химия. 8 класс
Топливо. Загрязнения воздуха, способы его предотвращения. Химия. 8 класс Нурахмет А Защита ДП
Нурахмет А Защита ДП Амины
Амины Гидрокарбонат натрия NaHCO₃
Гидрокарбонат натрия NaHCO₃ Химические методы выявления потожировых следов
Химические методы выявления потожировых следов Переработка тяжелых нефтей, битумов и нефтяных остатков
Переработка тяжелых нефтей, битумов и нефтяных остатков Теория электролитической диссоциации
Теория электролитической диссоциации Спектроскопия лазерных кристаллов
Спектроскопия лазерных кристаллов Тепло- и массообменные процессы при синтезе Фишера-Тропша
Тепло- и массообменные процессы при синтезе Фишера-Тропша Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Белоктар. Биохимиясы
Белоктар. Биохимиясы Электролиз: его применение
Электролиз: его применение