Содержание
- 2. Методи неорганічного синтезу по класах синтезованих сполук (синтез оксидів, гідроксидів, гідридів і т.д.) по типах хімічних
- 3. Реакції у водному розчині окисно-відновні, у тому числі, що перебігають при електролізі обміну з'єднання (комплексоутворення)
- 4. Перебіг у водному розчині реакцій, що використовуються для синтезу певних речовин, може ускладнювати: окиснення та відновлення
- 5. РЕАКЦІЇ У ВОДНОМУ РОЗЧИНІ Загальні особливості реакцій у водному розчині та фактори, що їх ускладнюють Ва2+(р)
- 6. Напівреакція відновлення водню: Напівреакція окиснення кисню:
- 7. Ці процеси обмежують термодинамічну стійкість речовин у водному розчині. У нейтральному розчині (pH = 7) вода
- 8. Кисень має досить сильну окисну здатність: рН = 0, О2 + 4Н+ + 4ē = 2Н2О,
- 9. Перебіг реакцій у розчині може ускладнюватися також процесом комплексоутворення, наприклад, кількісний перебіг реакцій Hg2+(p) + 2I–(р)
- 10. Реакції утворення важкорозчинних речовин з розчинних Реакції утворення важкорозчинних речовин, не ускладнені гідролізом. Реакції утворення важкорозчинних
- 11. Реакції утворення важкорозчинних речовин, не ускладнені гідролізом Наприклад, осади, отримані за обмінними реакціями Ag+(p) + I–(р)
- 12. Реакції утворення важкорозчинних речовин, ускладнені гідролізом Якщо розчинність дуже мала, гідроліз практично не йде, як, наприклад,
- 13. Спільний гідроліз у цьому випадку може привести до утворення важкорозчинних основних солей і навіть гідроксидів металів.
- 14. Zn2+(p) + (p) xZn(OH)2 · yZnCO3(т) + H2CO3 + Н2О ⇄ НCO3- + ОН– Кгідр≈ 10–4
- 15. Реакції утворення важкорозчинних речовин у результаті гідролізу Найчастіше цим шляхом одержують гідроксиди кремнію і металів, таких,
- 16. Реакції утворення важкорозчинних гідроксидів Для осадження важкорозчинних гідроксидів металів використовується реакція лужного осадження: Меn+(р) + ОН–
- 17. Реакції утворення металів Можливість перебігу реакції утворення металів теоретично оцінюється з урахуванням потенціалів систем Меn+/Ме, 2Н+/Н2
- 18. Реакції утворення металів Добре відомим прикладом реакцій розглянутого типу є реакція "срібного дзеркала". Іони срібла можуть
- 19. Реакції утворення важкорозчинних сполук у ході взаємодії газів з розчинами Використання реакцій такого типу неможливо для
- 20. Реакції утворення легкорозчинних речовин Умова необоротного перебігу таких реакцій – це утворення малодисоційованого основного продукту або
- 21. Реакції утворення комплексних сполук Cu2+(p) + 4NH3(p) = [Cu(NH3)4]2+(p), Кнест = 2·10–13, Co3+(p) + 6NH3(p) =
- 22. РЕАКЦІЇ В НЕВОДНИХ РОЗЧИНАХ Діапазон температур рідкого стану ряду неорганічних розчинників становить: У спиртовому розчині за
- 23. Неводні розчинники можна розділити на кілька груп: До першої з них можна віднести неполярні та слабкополярні
- 24. Розчинники із сильно вираженою іонізуючою здатністю одночасно схильні до самоіонізації. Це характерно для багатьох неорганічних сполук:
- 25. Для синтезу деяких координаційних сполук використовуються розчинники, молекули яких здатні виступати в ролі лигандів. У цьому
- 26. У рідкому HF і за його участю перебігають реакції обміну: NaCl(т) + НF(ж) = НС1(г) +
- 27. РЕАКЦІЇ У ТВЕРДІЙ ФАЗІ Реакції за участю твердих речовин досить різноманітні за типами і умовами їх
- 28. РЕАКЦІЇ У ТВЕРДІЙ ФАЗІ В твердій фазі перебігають наступні реакції: реакції взаємодії твердої і газоподібної, двох
- 29. Вплив ступеню гомогенності реакційної суміші, дисперсності реагентів і впорядкованості їх структури на швидкість реакції можна проілюструвати
- 30. РЕАКЦІЇ У ТВЕРДІЙ ФАЗІ У неорганічному синтезі для отримання багатьох твердих речовин, зокрема оксидів і особливо
- 31. РЕАКЦІЇ ЗА УЧАСТЮ ГАЗІВ Практичне застосування у отриманні та синтезі знаходять хімічні транспортні реакції, що перебігають
- 32. Прикладом транспортної реакції, використовуваної в неорганічному синтезі, може служити реакція отримання крупнокристалічного сульфіду цинку, що перебігає
- 34. Скачать презентацию
 Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною
Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною Энергоресурсы и их использование
Энергоресурсы и их использование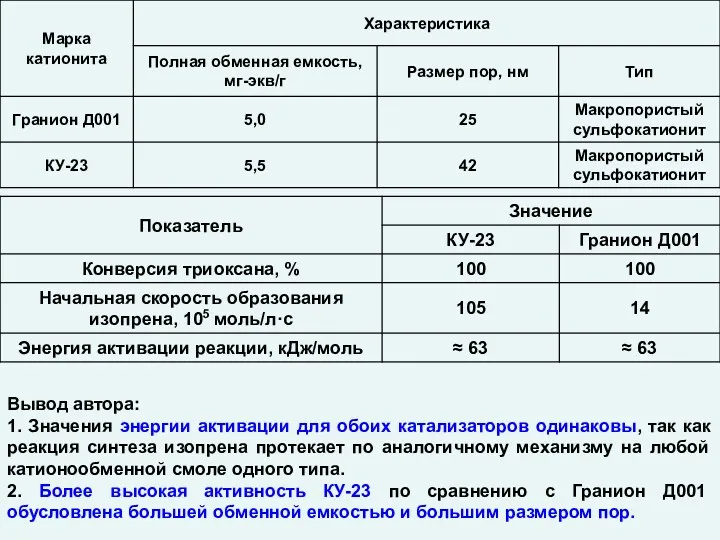 Катализ. Гетерогенные катализаторы
Катализ. Гетерогенные катализаторы Композиционные материалы: углепластик, стеклопластик
Композиционные материалы: углепластик, стеклопластик Реакции ионного обмена
Реакции ионного обмена Дизельное топливо
Дизельное топливо Кристалічний і аморфний стани твердих речовин
Кристалічний і аморфний стани твердих речовин Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Каучук
Каучук Как разгадать химический кроссворд
Как разгадать химический кроссворд Органические производные титана со связями Ti-O-C. Получение и свойства. Полимеры на их основе
Органические производные титана со связями Ti-O-C. Получение и свойства. Полимеры на их основе Кристаллические решетки
Кристаллические решетки Неметаллы – простые вещества
Неметаллы – простые вещества Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Ртуть. Использование ртути
Ртуть. Использование ртути Химическая промышленность
Химическая промышленность Электролитическая диссоциация
Электролитическая диссоциация Углерод. Аллотропные модификации углерода
Углерод. Аллотропные модификации углерода Electrolytes. Reactions in Aqueous Solutions
Electrolytes. Reactions in Aqueous Solutions Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Изомерия в органической химии. Изомеры
Изомерия в органической химии. Изомеры Методы окислительно-восстановительного и комплексонометри-ческого титрования
Методы окислительно-восстановительного и комплексонометри-ческого титрования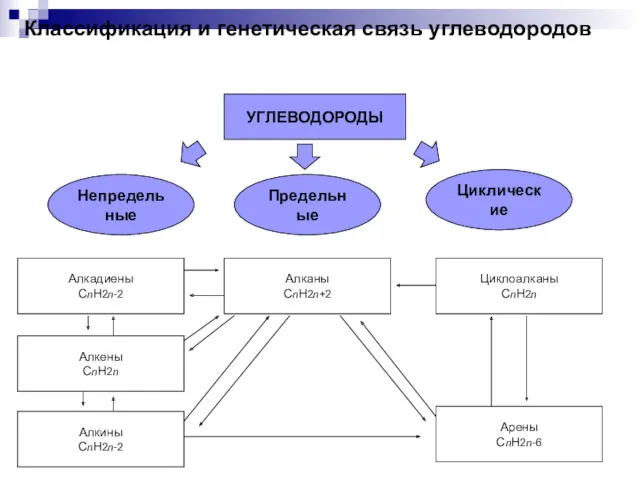 Классификация и генетическая связь углеводородов
Классификация и генетическая связь углеводородов Метод окислительно-восстановительного титрования
Метод окислительно-восстановительного титрования Реакции солей в растворе. Гидролиз солей. Водородный показатель рН
Реакции солей в растворе. Гидролиз солей. Водородный показатель рН Полифункциональные органические соединения
Полифункциональные органические соединения Кислородсодержащие органические соединения. 9 класс
Кислородсодержащие органические соединения. 9 класс