Слайд 2

Титан
Титан – элемент главной подгруппы IV группы. Его электронная формула следующая:
+22Ti
1s2|2s22p6|3s23p63d2|4s2
Электроотрицательность – 1,54 (шкала Полинга)
Как и у многих других d-элементов, в атоме титана Ti подвижными являются не только электроны наружного энергетического уровня, но и два электрона d-подуровня. Поэтому титан в соединениях проявляет степени окисления: +2, +4, +3
Слайд 3

Производные ортотитановой кислоты
В качестве производных ортотитановой кислоты выступают ее эфиры.
Взаимодействие алкоголятов
спиртов с тетрахлоридом титана:
Метод имеет ряд недостатков: выходы в этой реакции небольшие, скорость реакции низкая, трудно отделять осадок хлорида натрия, используются только те спирты, которые образуют алкоголяты.
Слайд 4

Получение в промышленности
В промышленности получают при взаимодействии тетрахлорида титана с органическими
спиртами в присутствии акцептора выделяющегося хлороводорода:
В качестве акцепторов предложено использовать жидкий или газообразный аммиак, формамид или диметилформамид, пиридин.
Слайд 5

Эфиры ортотитановой кислоты способны к реакции переэтерификации:
Тетрахлорид титана реагирует с алкиленоксидами
в среде органических растворителей:
Алкокси- и арилоксититанаты могут быть получены взаимодействием сульфида титана со спиртом или фенолом:
Обработка натрий- или калийтитангексафторида алкогалятами Mg, Ca, Al :
, где М=Mg, Ca; n=2 или М=Al; n=3
Слайд 6

Химические свойства
Гидролиз эфиров ортотитановой кислоты:
Комплекс распадается на спирт и оксиэфир, который
выделить не удается, так как он немедленно конденсируется, образуя титанооксановую связь:
Слайд 7

Получение олигомерных ортотитанатов при помощи термической конденсации ортотитанов:
Реакциями алкоголиза или переэтерификацией
можно получать эфиры с другими эфирными группами:
Взаимодействие ортотитанатов с галогенангидридами кислот:
Слайд 8

Реакции ортотитанатов с органическими кислотами или их ангидридами приводят к получению
ацильных производных. Достаточно легко происходит образование моно- и диацилатов, дальнейшее замещение осуществить трудно, так как образующиеся ацилаты неустойчивы и легко конденсируются с образованием титанооксановых связей:
Слайд 9

Внутренние комплексы титана (хелаты)
Атом титана обладает способностью образовывать координационные связи с
увеличением координационного числа до шести. Если в органическом радикале, связанном с атомом титана эфирной связью, имеются атомы X с неподеленной парой электронов, то возможно образование внутренних комплексных связей:
Слайд 10

Химические свойства
Ацетилацетон является β-дикетоном, склонным к кетоенольной таутомерии:
В енольной форме он
взаимодействует с ортоэфирами титана:
Слайд 11
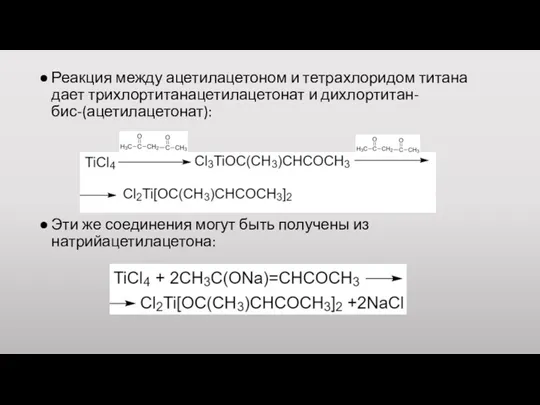
Реакция между ацетилацетоном и тетрахлоридом титана дает трихлортитанацетилацетонат и дихлортитан-бис-(ацетилацетонат):
Эти же
соединения могут быть получены из натрийацетилацетона:
Слайд 12
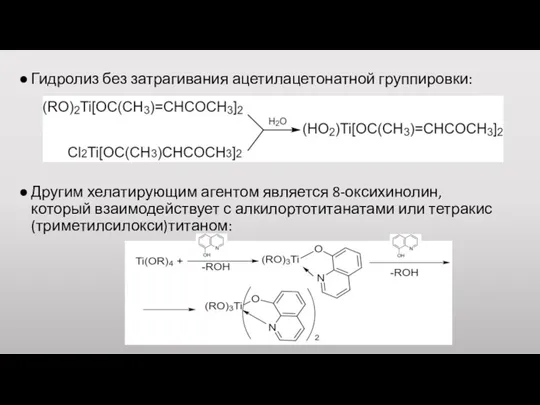
Гидролиз без затрагивания ацетилацетонатной группировки:
Другим хелатирующим агентом является 8-оксихинолин, который взаимодействует
с алкилортотитанатами или тетракис(триметилсилокси)титаном:











 Массовая доля растворенного вещества в растворе
Массовая доля растворенного вещества в растворе Способы производства железоуглеродистых сплавов
Способы производства железоуглеродистых сплавов Суспензии: получение, свойства
Суспензии: получение, свойства Соли (12 класс)
Соли (12 класс) Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Химические опасности. Нитраты
Химические опасности. Нитраты Lipid metabolism
Lipid metabolism Контроль результатов обучения химии
Контроль результатов обучения химии Галогены. Строение атомов и молекул галогенов
Галогены. Строение атомов и молекул галогенов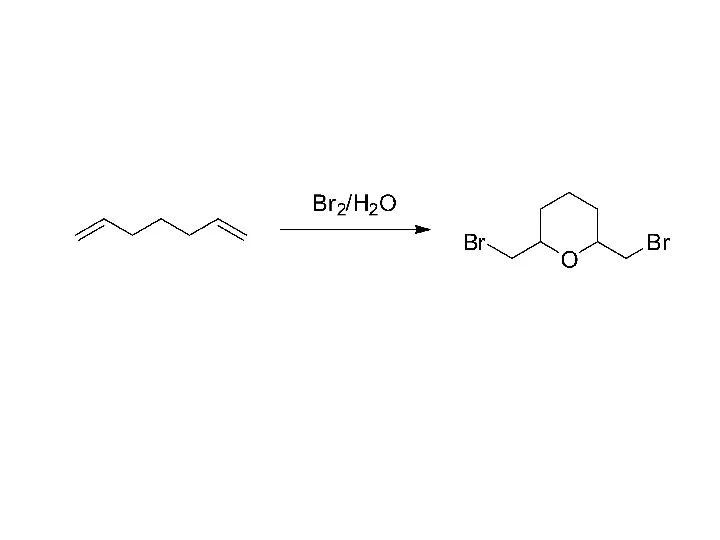 Превращение (S)-бутанол-2 в другие соединения
Превращение (S)-бутанол-2 в другие соединения Три состояния вещества
Три состояния вещества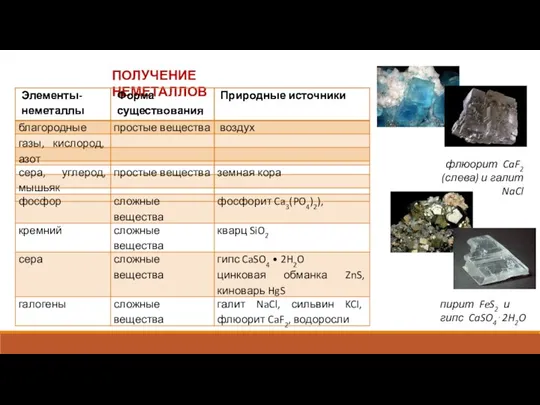 Получение неметаллов
Получение неметаллов Липолиз. Обмен кетоновых тел
Липолиз. Обмен кетоновых тел Алюминий. Определите элемент
Алюминий. Определите элемент Оксид кальция (СаО)
Оксид кальция (СаО) Chemical reactions and heat. (Chapter 1)
Chemical reactions and heat. (Chapter 1) Натрий алкилсульфонаттарын алу. №4 лекция
Натрий алкилсульфонаттарын алу. №4 лекция Растворы. Основные понятия и определения
Растворы. Основные понятия и определения Игра - викторина
Игра - викторина Лекция 2 Периодический закон
Лекция 2 Периодический закон Techniques for preparation of gaseous samples with a desired concentration of analyte
Techniques for preparation of gaseous samples with a desired concentration of analyte Химия в повседневной жизни человека
Химия в повседневной жизни человека Предмет органической химии
Предмет органической химии Полимеры, их классификации и способы получения
Полимеры, их классификации и способы получения Атом құрылысы
Атом құрылысы Химический элемент - водород
Химический элемент - водород Plastic is one of the challenges of the 21st century
Plastic is one of the challenges of the 21st century Періодична система хімічних елементів
Періодична система хімічних елементів