Слайд 2

Тесты
А 4 . В каком ряду химические элементы расположены в порядке
увеличения их атомного радиуса?
1) Na, Mg, Al 2) Al, Mg, Na 3) K, Na, Li 4) Mg, Be, Ca
А 5 . Металл, обладающий самой высокой электропроводностью, - это
1) железо 2) медь 3) серебро 4) алюминий
А 6 . Самый тугоплавкий металл – это:
хром 2) медь 3) вольфрам 4) железо
А7
В каком ряду химические элементы расположены в порядке ослабления металлических свойств?
1) Li, K, Rb 2) Al, Mg, K 3) Ca, Mg, Li 4) K, Ca, Be
А8 Самый легкоплавкий металл – это:
1) цезий 2) ртуть 3) алюминий 4) железо
Составьте уравнения химических реакций согласно схеме:
Ca ---- CaO ---- Ca(OH)2 ----- CaCO3 ----- CaCl2
Слайд 3

Тесты
А9 В каком ряду химические элементы расположены в порядке увеличения их
атомного радиуса?
Na, Mg, Al 2) Al, Mg, Na
3) K, Na, Li 4) Mg, Be, Ca
А10 Металл, обладающий самой высокой пластичностью, - это:
1) золото 2) медь
3) серебро 4) алюминий
Составьте уравнения химических реакций согласно схеме:
Ca ---- CaO ---- Ca(OH)2 ----- CaCO3 ----- CaCl2
Слайд 4

Ответы
1Б ;2 Б; 3В;4-2;5-3;6-3;7-4; 8-2;9-2;10-1
Слайд 5

Слайд 6
Слайд 7

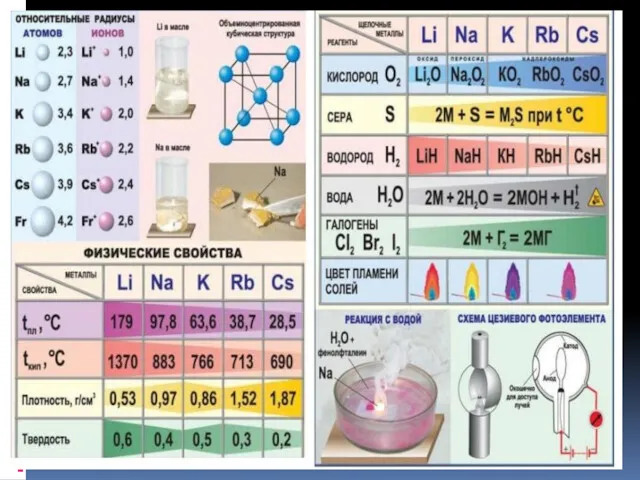
Взаимодействие с простыми веществами-неметаллами
1. Металлы взаимодействуют с кислородом, образуя оксиды.
Металл + кислород → оксид.
Реакция щелочных металлов с кислородом:
4Li + O2 → 2Li2O (оксид лития)
2Na + O2 → Na2O2 ( пероксид натрия)
K + O2 → KO2 (надпероксид калия)
Слайд 8

Щелочные металлы:
2. В реакциях щелочных металлов с другими неметаллами образуются бинарные
соединения:
2Li + Cl2 → 2LiCl (галогениды)
2Na + S → Na2S (сульфиды)
2Na + H2 → 2NaH (гидриды)
6Li + N2 → 2Li3N (нитриды)
2Li + 2C → Li2C2 (карбиды)
Слайд 9

Опыт 1
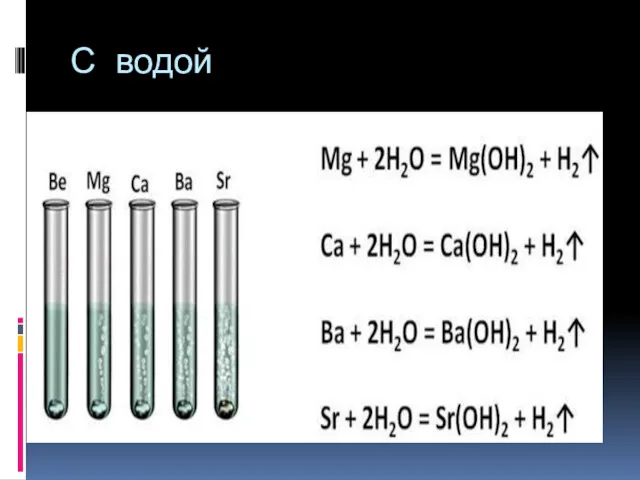
2 Li + 2 H2O = 2 LiOH + H2
2 Na + 2 H2O = 2 NaOH + H2
2 K + 2 H2O = 2
KOH + H2
Кусочек натрия помещаем на поверхность воды. Попадая в воду, натрий плавится и начинает быстро двигаться по поверхности воды, подгоняемый пузырьками выделяющегося водорода. Кусочек натрия уменьшается на глазах. В процессе реакции также образуется щелочь - гидроксид натрия. С калием нужно обращаться очень осторожно. На воздухе он может самовозгораться. Кусочек калия поместим в чашку Петри с водой. Калий так энергично реагирует с водой, что выделяющийся в реакции водород загорается. В целях безопасности чашку Петри следует накрыть стеклянной пластинкой. Из трех щелочных металлов наиболее активным является калий.
Слайд 10

Щелочные металлы
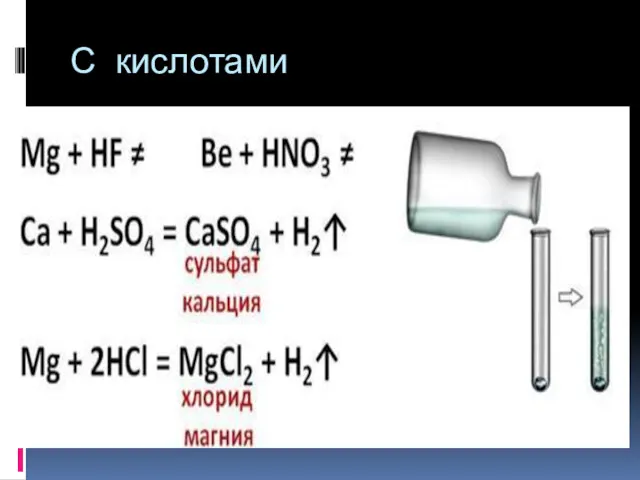
3. Реакция щелочных металлов с кислотами
(проводят редко, идет конкурирующая реакция
с водой):
2Na + 2HCl → 2NaCl + H2
4. Взаимодействие щелочных металлов с аммиаком
(образуется амид натрия):
2Li + 2NH3 = 2LiNH2 + H2
5. Взаимодействие щелочных металлов со спиртами и фенолами, которые проявляют в данном случае кислотные свойства:
2Na + 2C2H5OH = 2C2H5ONa + H2;
2K + 2C6H5OH = 2C6H5OK + H2;
Слайд 11

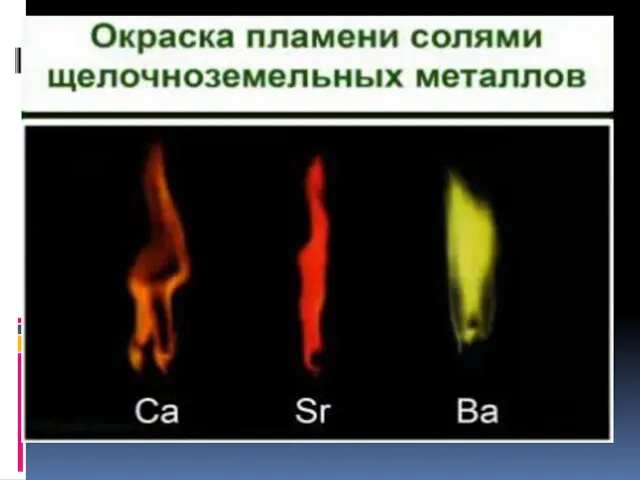
6. Качественная реакция на катионы щелочных металлов — окрашивание пламени в
следующие цвета:
Li+ – карминово-красный
Na+ – желтый
K+, Rb+ и Cs+ – фиолетовый
Слайд 12

Слайд 13

Щелочноземельные металлы
Реакция с кислородом.
Все металлы образуют оксиды RO, барий-пероксид – BaO2:
Ba +
O2 ® BaO2
В атмосфере кислорода магний вспыхивает ослепительным белым пламенем.При горении магния выделяются ультрафиолетовые лучи.
Продукт горения магния – белый порошкообразный оксид.
2Mg + O2= 2MgO
Слайд 14

Слайд 15
Слайд 16
Слайд 17
Слайд 18

Слайд 19

Слайд 20

Слайд 21

Слайд 22

Реакция железа с кислотами
Слайд 23

Задание
Напишите три уравнения реакций железа с разбавленной азотной кислотой, в которых
продуктом восстановления кислоты будет соответственно N2, NO, NH4NO3. Для расстановки коэффициентов в уравнениях химических реакций используйте метод электронного баланса. Определите окислитель и восстановитель в этих реакциях.
Слайд 24

Слайд 25

Слайд 26
Слайд 27

Задание 2
Методом электронного баланса определите коэффициенты в уравнении реакции, схема которого:
Какой ион проявляет в этой реакции окислительные свойства?
Слайд 28

Слайд 29

Задание 3
Можно ли получить водород при взаимодействии свинца с раствором серной
кислоты?
Ответ
По правилу, которое гласит, что металлы, стоящие в ряду напряжения левее водорода, вытесняют его из растворов кислот, водород при реакции свинца с раствором серной кислоты должен получиться. Но данное правило соблюдается, если в реакции металла с кислотой образуется растворимая соль, a PbSO4 — нерастворимая соль. Поэтому в случае свинца и серной кислоты правило не действует и, следовательно, водород нельзя получить при взаимодействии свинца с раствором серной кислоты.
Слайд 30

Задание 4
Как можно получить из пирита FeS2 железо и серную кислоту?
Запишите уравнения реакций.





























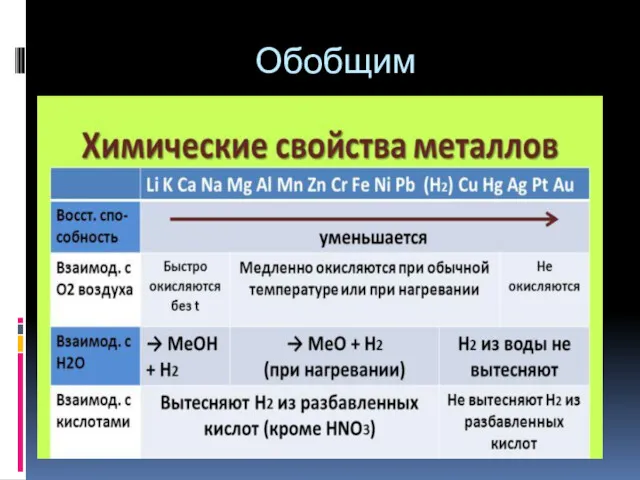
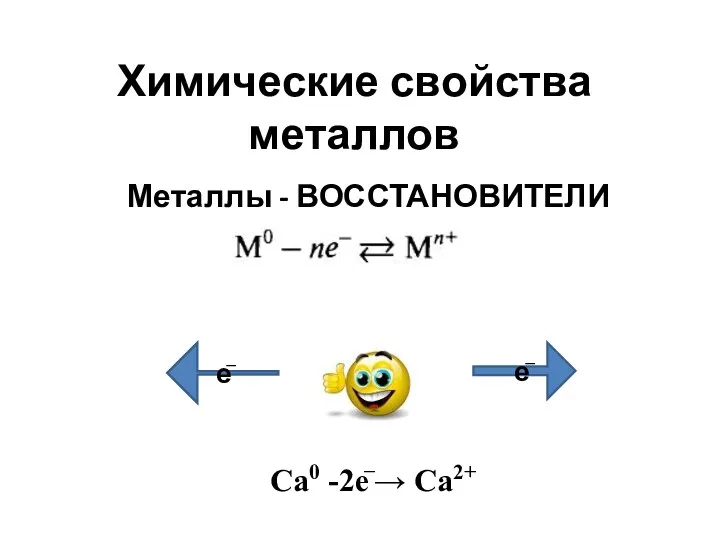 Химические свойства металлов
Химические свойства металлов Основные физико-химические процессы очистки воды. Опыт исследования коагулянтов и флокулянтов
Основные физико-химические процессы очистки воды. Опыт исследования коагулянтов и флокулянтов Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Кремний и его соединения
Кремний и его соединения Экспериментальные методы измерения изотерм адсорбции. Лекция 4
Экспериментальные методы измерения изотерм адсорбции. Лекция 4 Строение атома
Строение атома Явления, происходящие с веществами
Явления, происходящие с веществами Химические свойства оксидов
Химические свойства оксидов Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Общие свойства металлов
Общие свойства металлов Гидролиз неорганических соединений
Гидролиз неорганических соединений Биохимия нуклеиновых кислот
Биохимия нуклеиновых кислот Магматические формации
Магматические формации Аминокислоты. Химические свойства
Аминокислоты. Химические свойства Тіршілік гетерофункционалды қосылыстар
Тіршілік гетерофункционалды қосылыстар Минералы. Классификация
Минералы. Классификация Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Крекинг нефти
Крекинг нефти Химический факультет
Химический факультет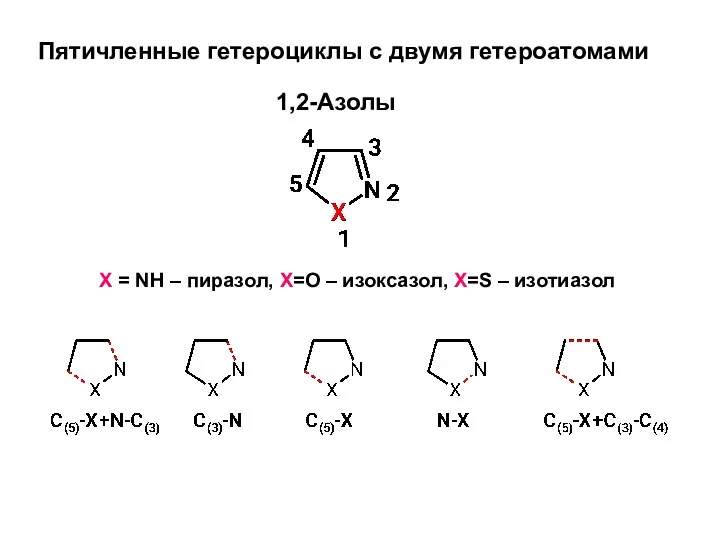 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами Контроль результатов обучения химии
Контроль результатов обучения химии Нуклеозиды. Нуклеиновые кислоты
Нуклеозиды. Нуклеиновые кислоты Кислотные дожди
Кислотные дожди Кислоты. Классификация кислот по строению кислотного остатка
Кислоты. Классификация кислот по строению кислотного остатка Этот многоликий цинк
Этот многоликий цинк Алюминий
Алюминий Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості (10 клас)
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості (10 клас) Смазочные материалы. Моторные масла
Смазочные материалы. Моторные масла