Содержание
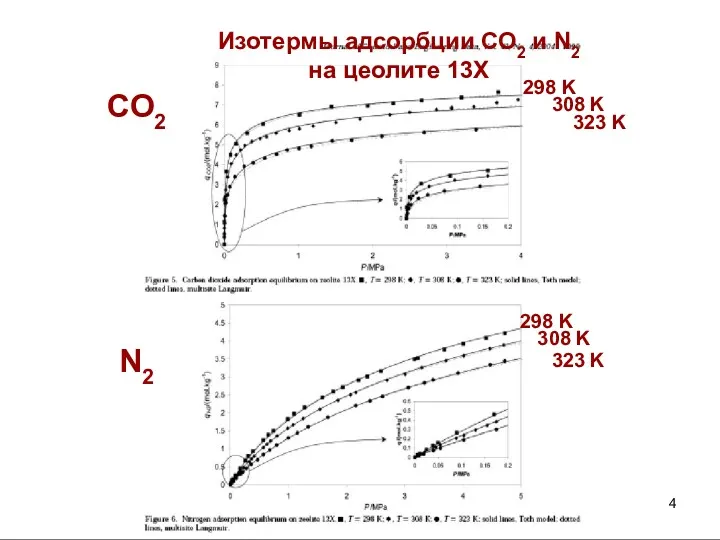
- 2. Величина адсорбции а = f(P,T,Σξi), где Р - давление (или концентрация) адсорбтива G; Т- температура, ξi-
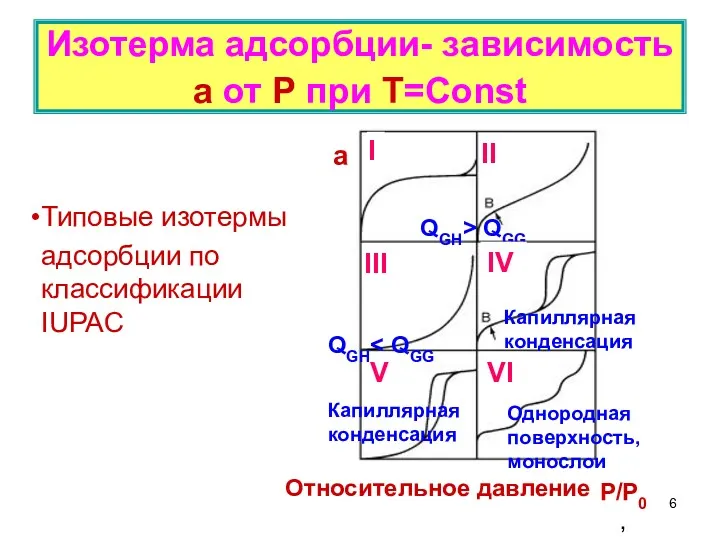
- 3. Изотерма адсорбции – зависимость а = a(P) при T = const; Изобара адсорбции – зависимость а
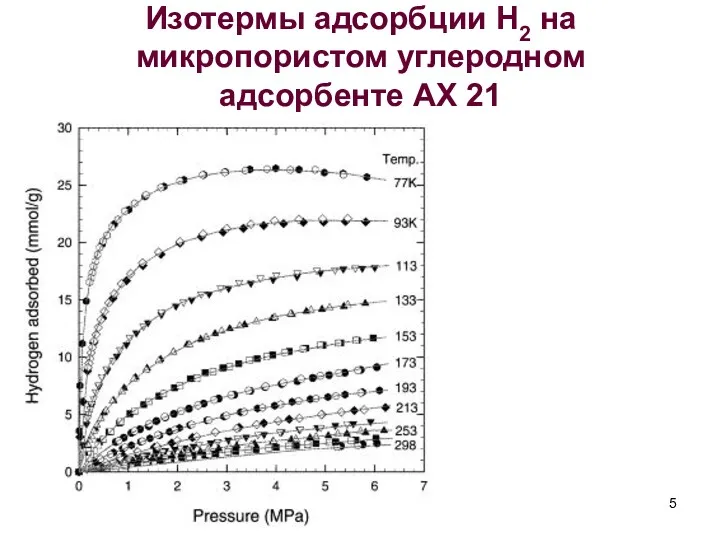
- 5. Изотермы адсорбции Н2 на микропористом углеродном адсорбенте АХ 21
- 6. Изотерма адсорбции- зависимость а от Р при Т=Const Типовые изотермы адсорбции по классификации IUPAC
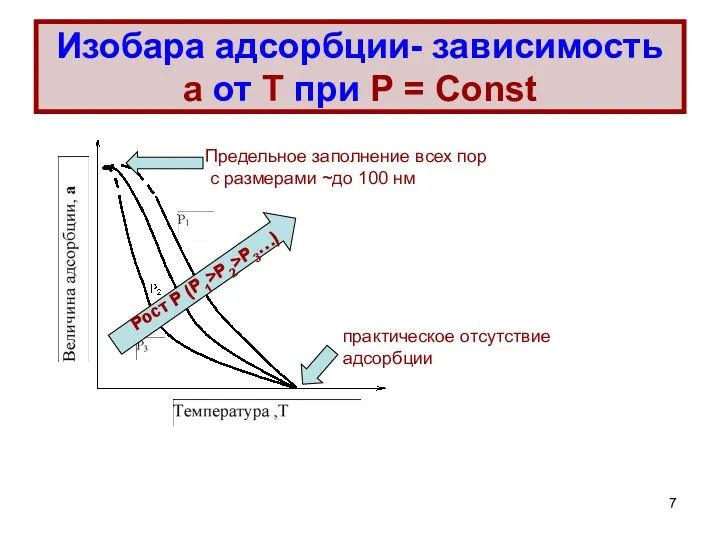
- 7. Изобара адсорбции- зависимость а от Т при Р = Const
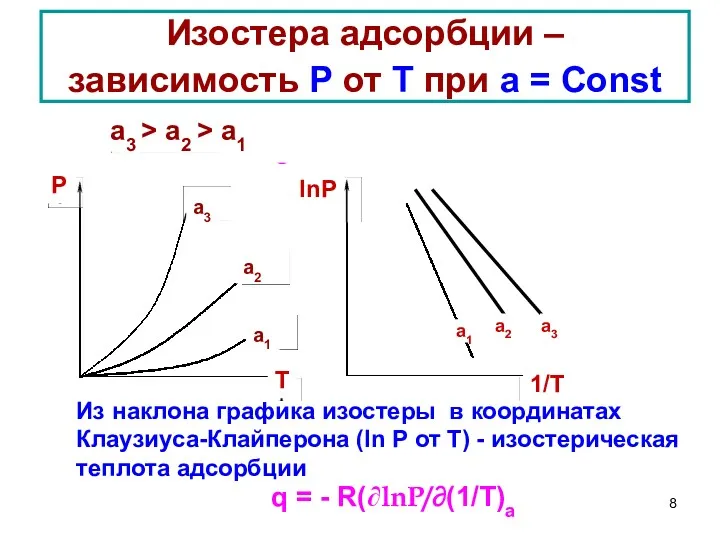
- 8. Изостера адсорбции – зависимость Р от Т при а = Const q = - R(∂lnP/∂(1/T)a
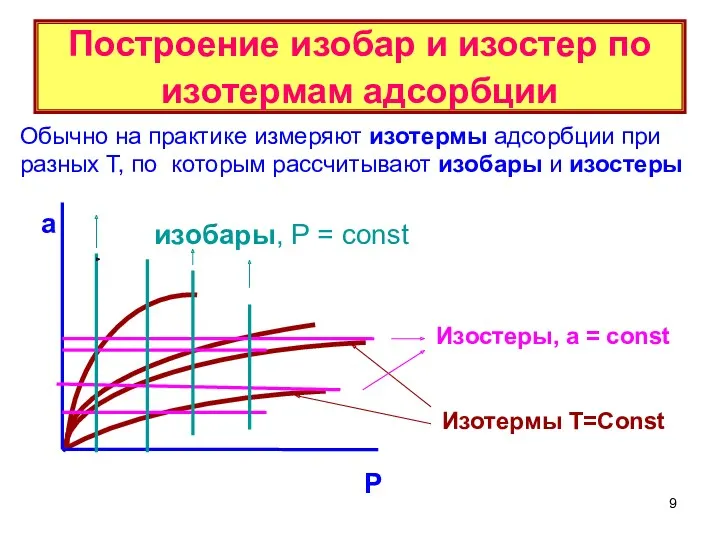
- 9. Построение изобар и изостер по изотермам адсорбции Обычно на практике измеряют изотермы адсорбции при разных Т,
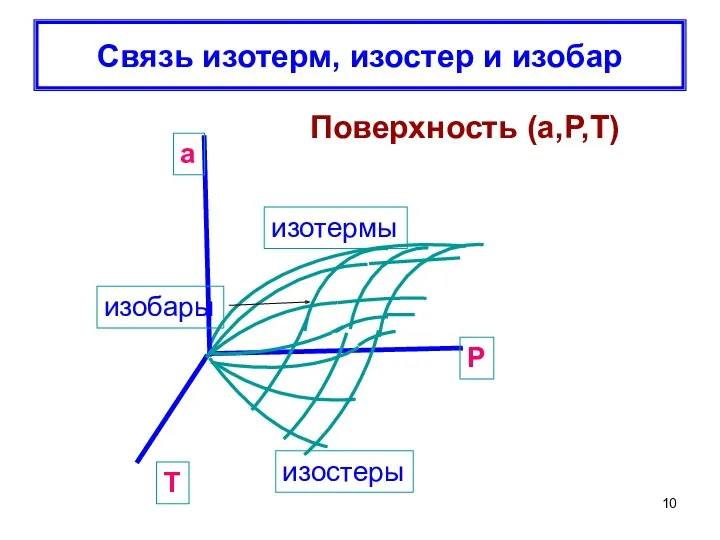
- 10. Связь изотерм, изостер и изобар Поверхность (а,Р,Т)
- 11. Связь изотерм, изостер и изобар Принимая, что при ξi = Const зависимость a(P,T) – непрерывная независимая
- 12. Равновесные величины адсорбции В общем случае равновесные величины адсорбции а могут быть измерены по: Изменению массы
- 13. Необходимые условия для корректного измерения адсорбции газов и паров Измерения адсорбции проводятся после: очистки системы от
- 14. изотерма адсорбции Адсорбционная ветвь изотермы измеряется путем последовательного напуска порций адсорбтива с возрастающим давлением Р. Десорбционная
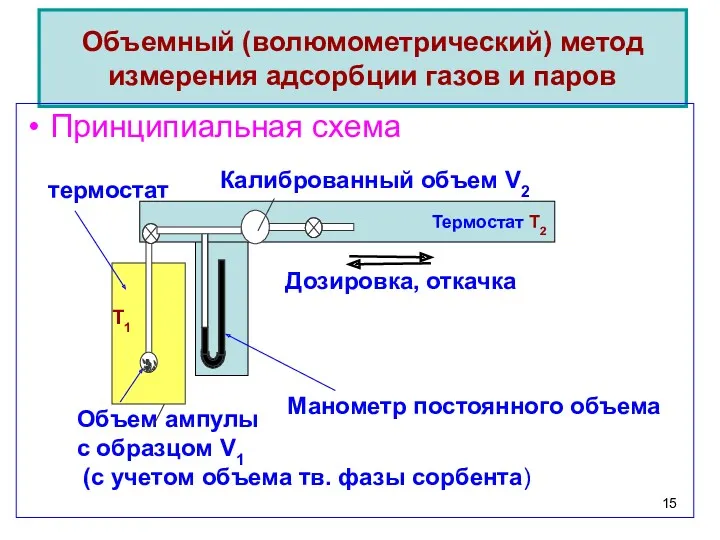
- 15. Объемный (волюмометрический) метод измерения адсорбции газов и паров Принципиальная схема
- 16. Расчеты адсорбции - через изменение числа молей адсорбтива в объеме Δm = (P1- Р2)Vа/RT Объемный (волюмометрический)
- 17. ASAP-2020 Micromeritics
- 18. ASAP-2420 Micromeritics
- 19. Теплота адсорбции q Дает прямую информацию об энергии связи и природе адсорбционного взаимодействия, отражает энергетическую сторону
- 20. Изостерическая теплота адсорбции qст Из общих уравнений т/д поверхностных явлений следует применимость уравнения Клаузиуса-Клайперона при условии
- 21. Теплота адсорбции q Дифференциальная теплота адсорбции qкал, измеряе-мая на калориметре при введении малых порций адсорбата, определяется
- 23. Скачать презентацию












 Элементы V группы главной подгруппы
Элементы V группы главной подгруппы Свойства алкадиенов и их получение
Свойства алкадиенов и их получение Алкены. Этилен
Алкены. Этилен Природные источники углеводородов
Природные источники углеводородов Адсорбция
Адсорбция Формы минералов и их агрегатов
Формы минералов и их агрегатов Азотсодержащие органические соединения. Аминокислоты (часть 2)
Азотсодержащие органические соединения. Аминокислоты (часть 2) Основные классы неорганических соединений
Основные классы неорганических соединений Химические элементы IV группы главной подгруппы
Химические элементы IV группы главной подгруппы Трифенилметановые красители
Трифенилметановые красители Азотсодержащие органические соединения
Азотсодержащие органические соединения Гидролиз солей. Лекция №9
Гидролиз солей. Лекция №9 Жесткость воды
Жесткость воды Азо-, диазосоединения
Азо-, диазосоединения Вода. Практическая работа
Вода. Практическая работа Природные источники углеводородов
Природные источники углеводородов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Основные понятия химии
Основные понятия химии Хімічні явища в побуті
Хімічні явища в побуті Анилин. Строение. Физические и химические свойства
Анилин. Строение. Физические и химические свойства Каменный уголь
Каменный уголь Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Углерод. Положение в периодической системе и строение атома
Углерод. Положение в периодической системе и строение атома Коррозия металлов и способы ее устранения
Коррозия металлов и способы ее устранения Физические свойства карбоновых кислот. Общие химические свойства неорганических и органических кислот. 10 класс
Физические свойства карбоновых кислот. Общие химические свойства неорганических и органических кислот. 10 класс Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве
Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве Супрамолекулярний контроль для дослідження реакційної здатності та каталізу
Супрамолекулярний контроль для дослідження реакційної здатності та каталізу Химические свойства алкенов
Химические свойства алкенов