Содержание
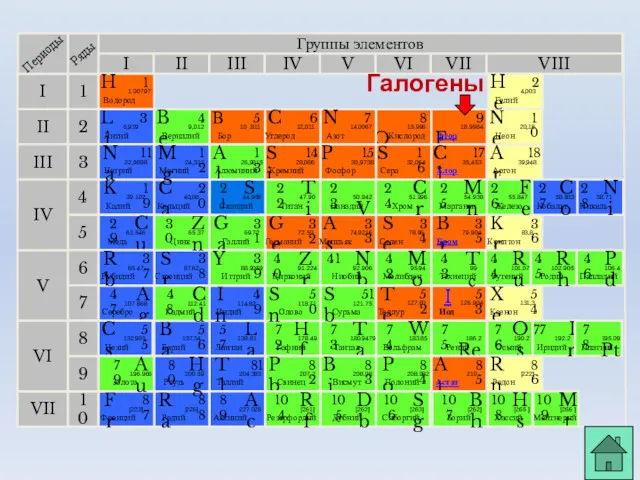
- 3. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 4. Общая характеристика К элементам V группы, главной подгруппы относятся азот N, фосфор P, мышьяк As, сурьма
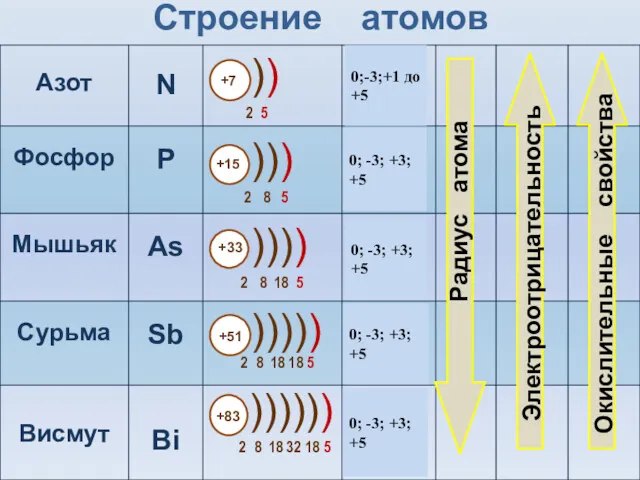
- 5. Строение атомов 0;-3;+1 до +5 0; -3; +3; +5 0; -3; +3; +5 0; -3; +3;
- 6. Общая характеристика nS2nP3 – строение внешнего энергетического уровня На внешнем уровне 5 электронов Увеличивается количество энергетических
- 7. Высшая степень окисления в соединениях равна +5; низшая степень окисления равна —3 (кроме Sb и Bi).
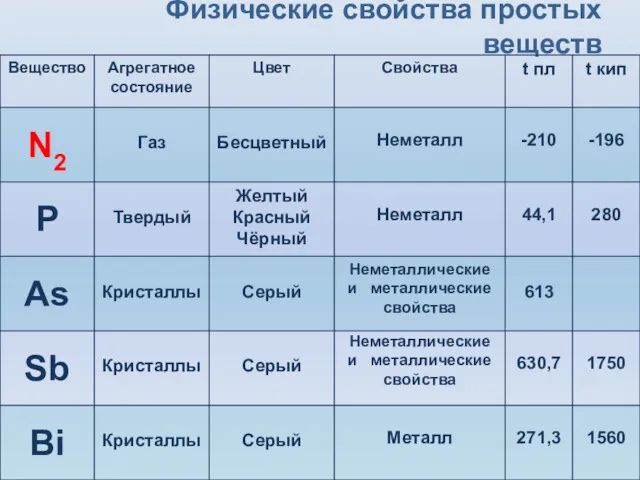
- 8. Физические свойства простых веществ
- 9. Первые два элемента (азот и фосфор) являются типичными неметаллами, мышьяк уже проявляет признаки металличности, значительно усиливающиеся
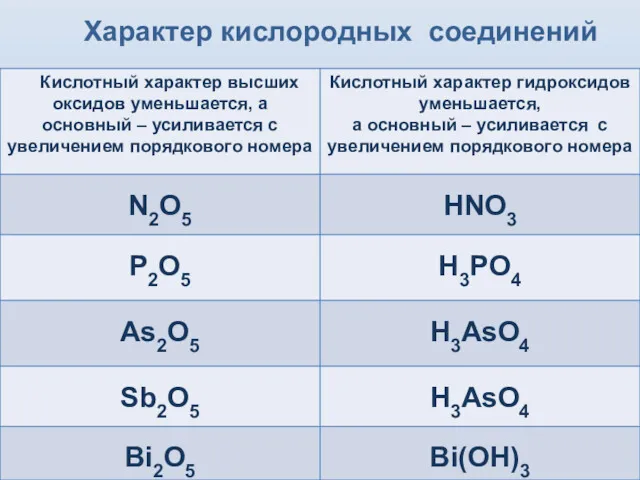
- 10. Характер кислородных соединений
- 11. Из истории открытия азота Впервые азот был открыт английским ученым Д.Резерфордом в 1772 г. Его свойства
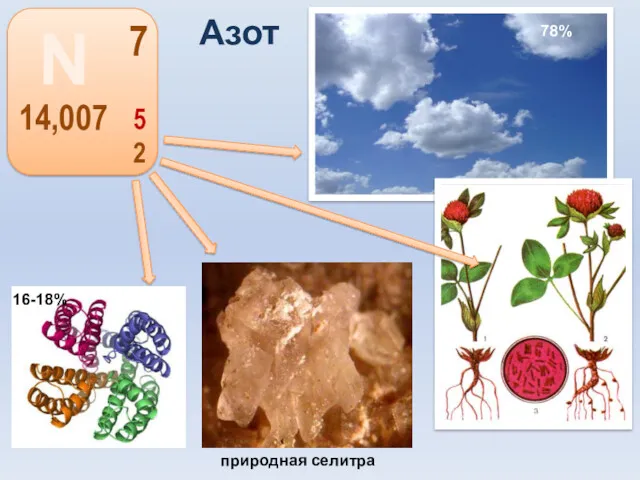
- 12. Азот
- 13. Значение азота Азот- жизненно важный элемент. Все основные части клеток организма построены из белковых молекул, в
- 14. В природе основная часть азота находится в свободном состоянии (N2). Из неорганических соединений азота только натриевая
- 15. Фосфор
- 16. Мышьяк Мышьяк — редкий элемент. содержание в земной коре 1,7·10-4% по массе может встречаться в самородном
- 17. Сурьма Природная сурьма является смесью двух изотопов: 121Sb (57,36 %) и 123Sb (42,64 %) Напоминая внешним
- 19. Скачать презентацию










 Соединения химических элементов. Урок-игра. 8 класс
Соединения химических элементов. Урок-игра. 8 класс Комплексонометрия – метод количественного титриметрического анализа
Комплексонометрия – метод количественного титриметрического анализа Экстракционные методы выделения продуктов микробиологического синтеза
Экстракционные методы выделения продуктов микробиологического синтеза Химическая связь
Химическая связь Общая характеристика и источники сырья производств основного органического и нефтехимического синтеза. Лекция № 5-6
Общая характеристика и источники сырья производств основного органического и нефтехимического синтеза. Лекция № 5-6 большая стирка
большая стирка Алкадиены. Гомологический ряд, номенклатура и изомерия
Алкадиены. Гомологический ряд, номенклатура и изомерия Химическая связь
Химическая связь Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату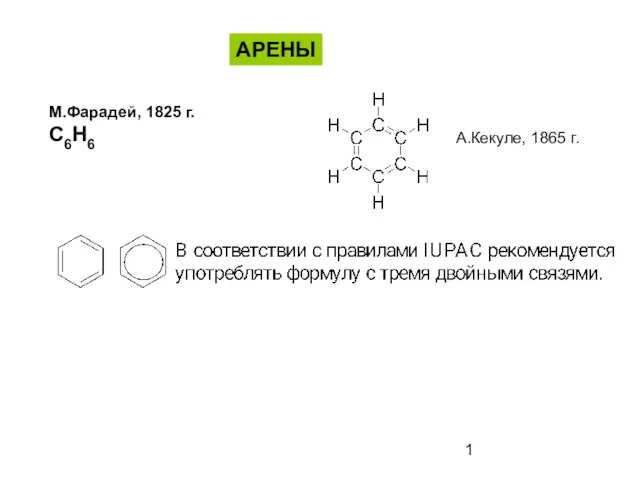 Ароматические соединения - арены
Ароматические соединения - арены Водородная связь
Водородная связь Электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей
Электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей Атомный и ионный радиусы. Принципы шаровых упаковок
Атомный и ионный радиусы. Принципы шаровых упаковок Азот и его соединения
Азот и его соединения Технология оптического стекла
Технология оптического стекла Современная химия. (Лекция 6)
Современная химия. (Лекция 6) Электрохимические процессы
Электрохимические процессы Простые вещества
Простые вещества Кислород
Кислород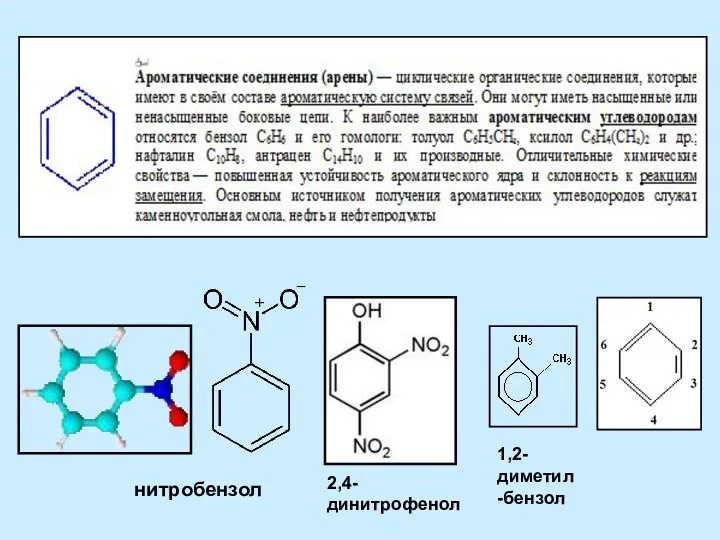 Ароматические соединения (арены)
Ароматические соединения (арены) Алкалоидтар
Алкалоидтар Лекция 2. Строение атома и Периодический закон Д.И. Менделеева
Лекция 2. Строение атома и Периодический закон Д.И. Менделеева Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Общая характеристика твердого, жидкого и газообразного видов топлива
Общая характеристика твердого, жидкого и газообразного видов топлива Химия в строительстве
Химия в строительстве Кислотные и основные свойства органических соединений
Кислотные и основные свойства органических соединений Углерод
Углерод