Электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей презентация
Содержание
- 2. Электролиты – это вещества, водные растворы которых проводят электрический ток Проверка электропроводности раствора: Электропроводность раствора хлорида
- 3. Электролиты в водном растворе или расплаве распадаются на ионы Неэлектролиты в водном растворе или расплаве не
- 4. Катионы – это положительно заряженные ионы АНОД КАТОД + + + - - - + -
- 5. Электролитическая диссоциация – это распад электролита на ионы Кислоты – это электролиты, которые в водном растворе
- 6. Электролитическая диссоциация – это распад электролита на ионы Основания – это электролиты, которые в водном растворе
- 8. Скачать презентацию
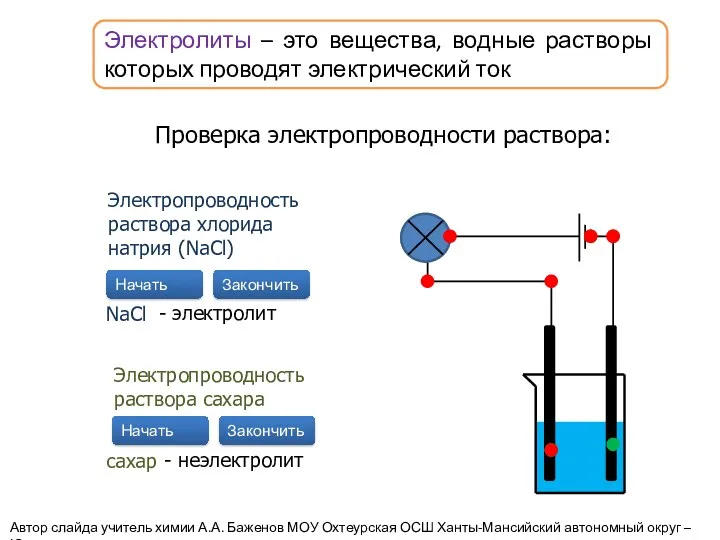
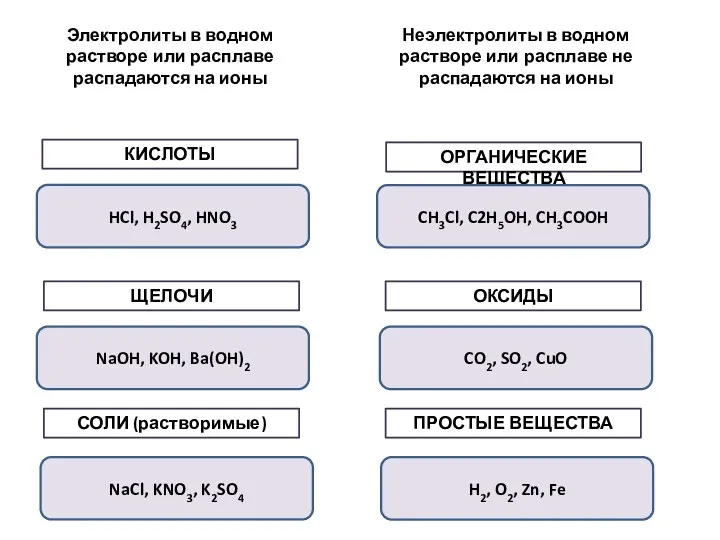
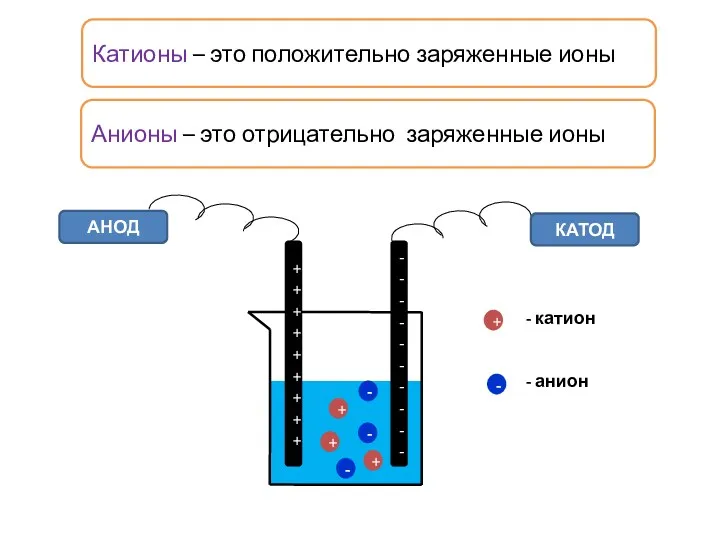
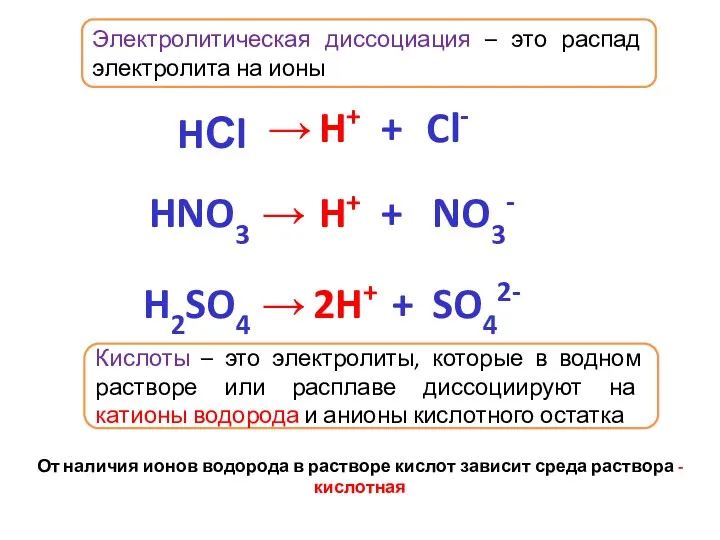
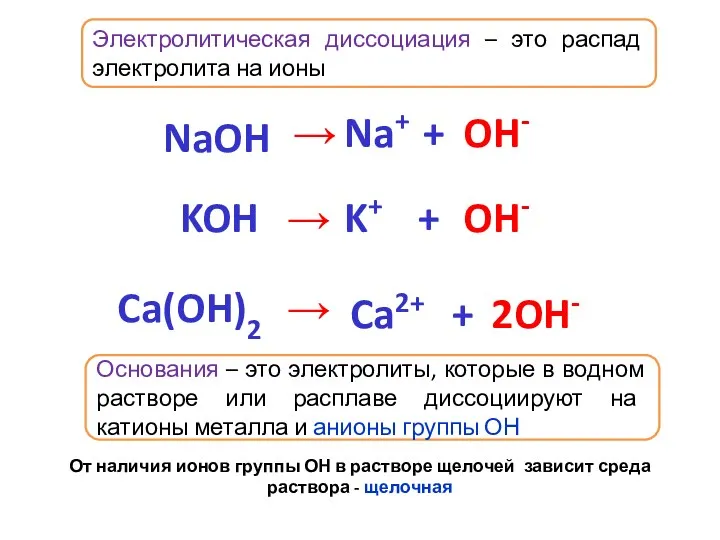
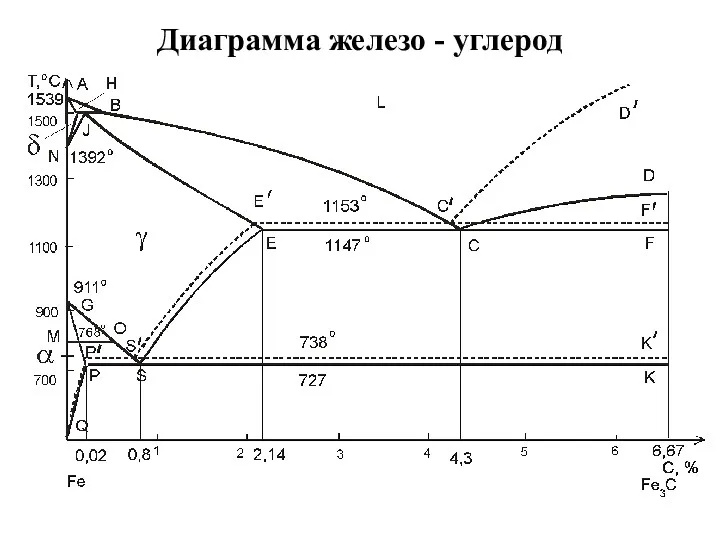 Диаграмма железо - углерод
Диаграмма железо - углерод Соли. Определение солей
Соли. Определение солей Месторождения турмалина
Месторождения турмалина Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс
Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс Алюминий IIIА топ элементі
Алюминий IIIА топ элементі Расчеты по химическим уравнениям. 8 класс
Расчеты по химическим уравнениям. 8 класс Катализ. Классификация каталитических процессов. Механизм действия катализаторов
Катализ. Классификация каталитических процессов. Механизм действия катализаторов Титриметрический метод анализа
Титриметрический метод анализа Періодична система Д.І.Менделєєва
Періодична система Д.І.Менделєєва Металдар мен бейметалдардың салыстырмалы сипаттамасы
Металдар мен бейметалдардың салыстырмалы сипаттамасы Знаки химических элементов
Знаки химических элементов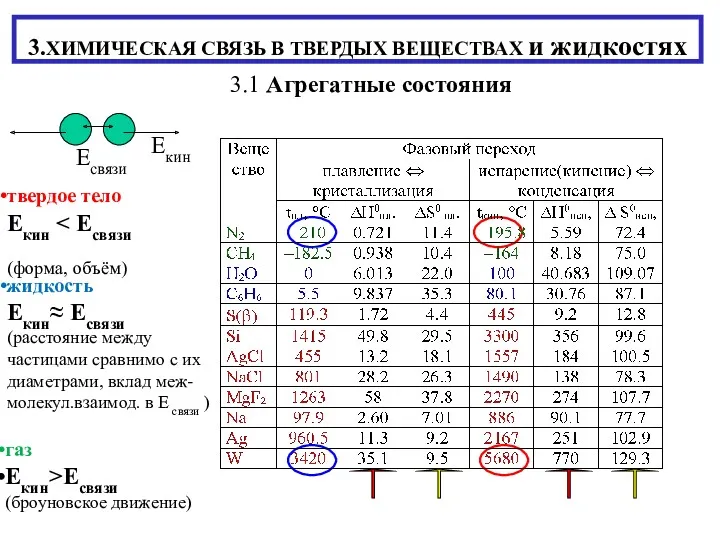 Химическая связь в твердых веществах и жидкостях
Химическая связь в твердых веществах и жидкостях Щелочные металлы
Щелочные металлы Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Задачи, включаемые в задание 33 тестов ЕГЭ
Задачи, включаемые в задание 33 тестов ЕГЭ Аллотропия
Аллотропия Ионная химическая связь
Ионная химическая связь Электролитическая диссоциация
Электролитическая диссоциация Розділ 3. Теорія комплексних сполук. Комплексні сполуки
Розділ 3. Теорія комплексних сполук. Комплексні сполуки Равновесные электрохимические системы
Равновесные электрохимические системы Мінеральні добрива
Мінеральні добрива Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды Классификация химических элементов. 8 класс
Классификация химических элементов. 8 класс Титриметрический анализ. Сущность титриметрического анализа
Титриметрический анализ. Сущность титриметрического анализа Липиды
Липиды Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Вода. Химические и физические свойства
Вода. Химические и физические свойства Разделение углеводородных газов
Разделение углеводородных газов