Содержание
- 2. Химия - наука о веществах, их свойствах, взаимных превращениях, и процессах, их сопровождающих Химия - наука
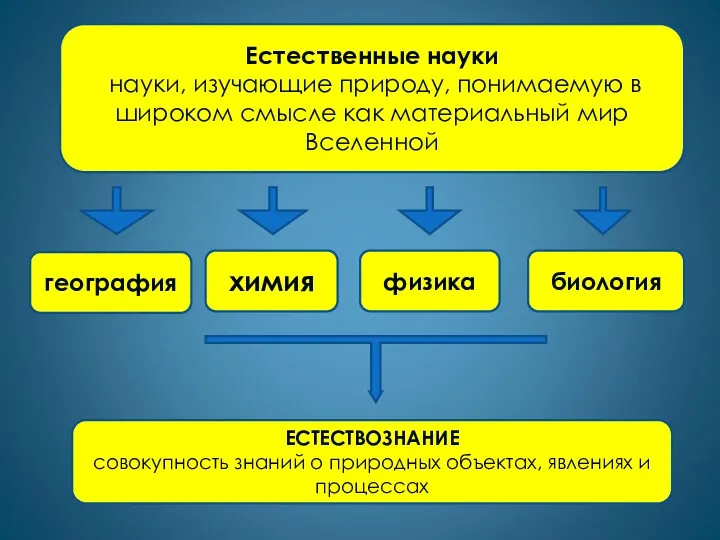
- 3. Естественные науки науки, изучающие природу, понимаемую в широком смысле как материальный мир Вселенной физика химия география
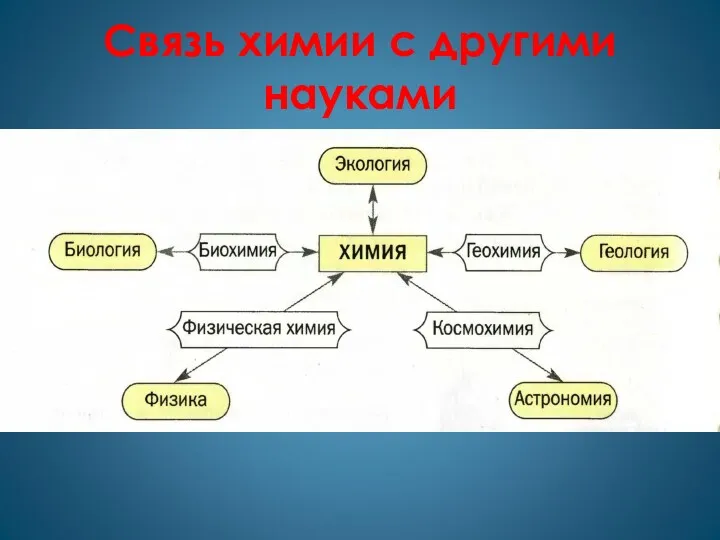
- 4. Связь химии с другими науками
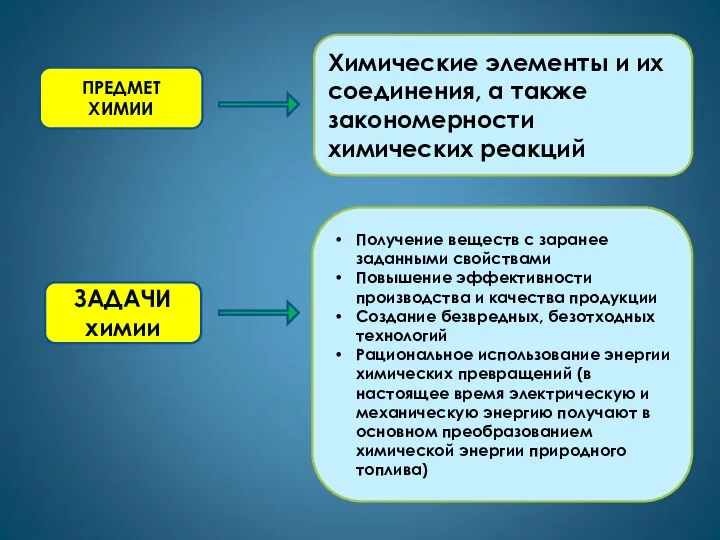
- 5. Химические элементы и их соединения, а также закономерности химических реакций ПРЕДМЕТ ХИМИИ Получение веществ с заранее
- 6. Вещество - то, из чего состоят физические тела. Вещество состоит из элементарных частиц (электронов, протонов, нейтронов
- 7. Молекула - наименьшая частица вещества, обладающая его химическими свойствами. Атом - наименьшая частица химического элемента, сохраняющая
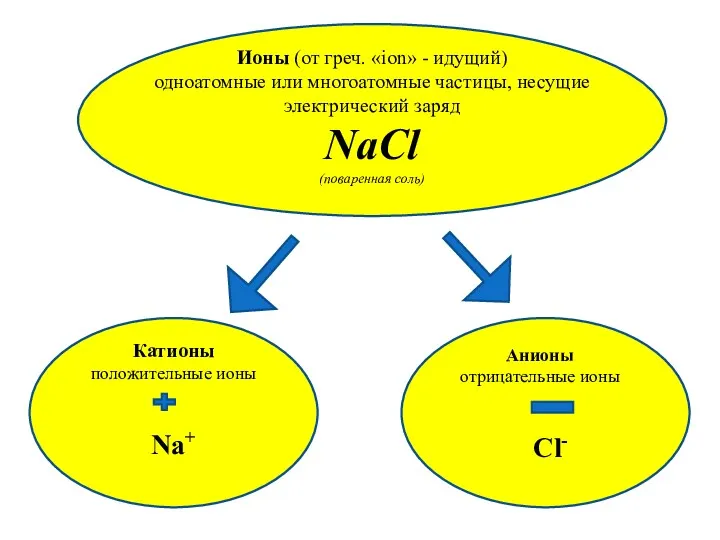
- 8. Ионы (от греч. «ion» - идущий) одноатомные или многоатомные частицы, несущие электрический заряд NaCl (поваренная соль)
- 9. Относительная атомная масса (Аг) - масса одного атома, выраженная в атомных единицах массы (а.е.м.). Показывает, во
- 10. Валентность (от лат. «valentia» - сила) - способность атома присоединять или замещать определенное число других атомов
- 11. Степень окисления (с.о.) - условный заряд атома данного элемента в соединении, вычисленный, исходя из предположения, что
- 12. Понятие валентности можно считать родственным такой характеристике, как степень окисления. Тем не менее, обе эти характеристики
- 13. Важнейшей количественной единицей в химии является величина, называемая молем. Моль - количество вещества, содержащее столько молекул,
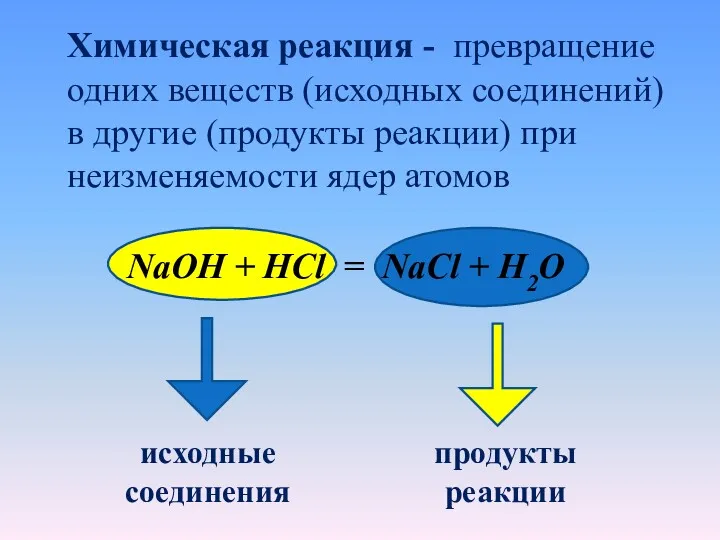
- 15. Химическая реакция - превращение одних веществ (исходных соединений) в другие (продукты реакции) при неизменяемости ядер атомов
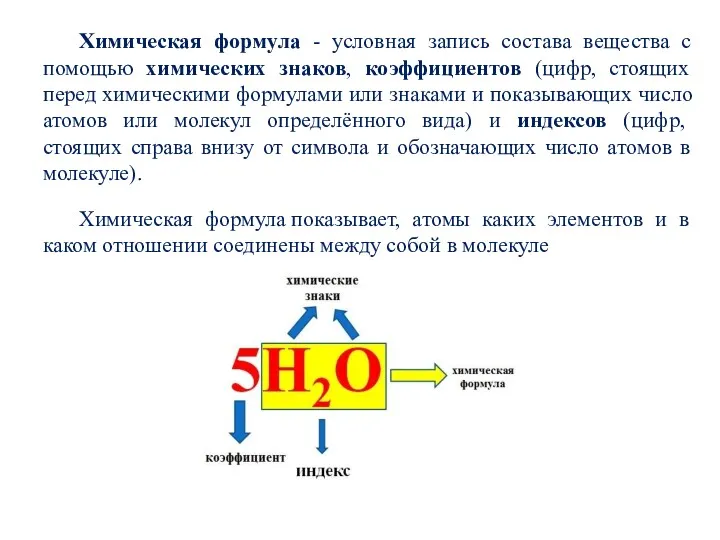
- 16. Химическая формула - условная запись состава вещества с помощью химических знаков, коэффициентов (цифр, стоящих перед химическими
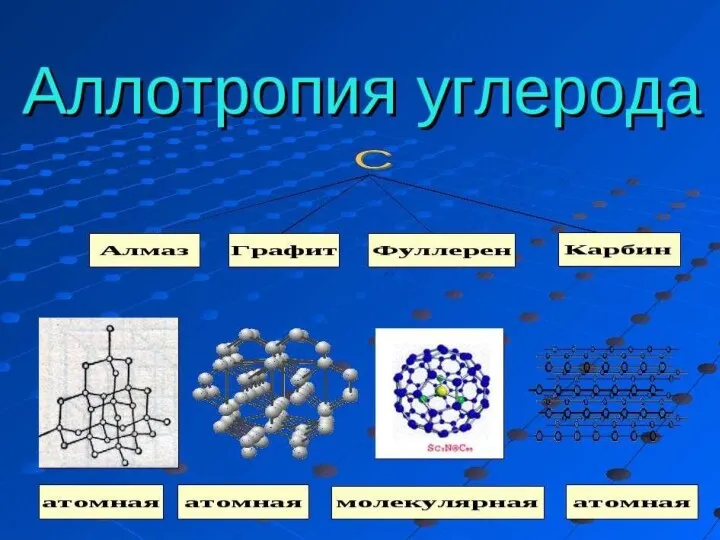
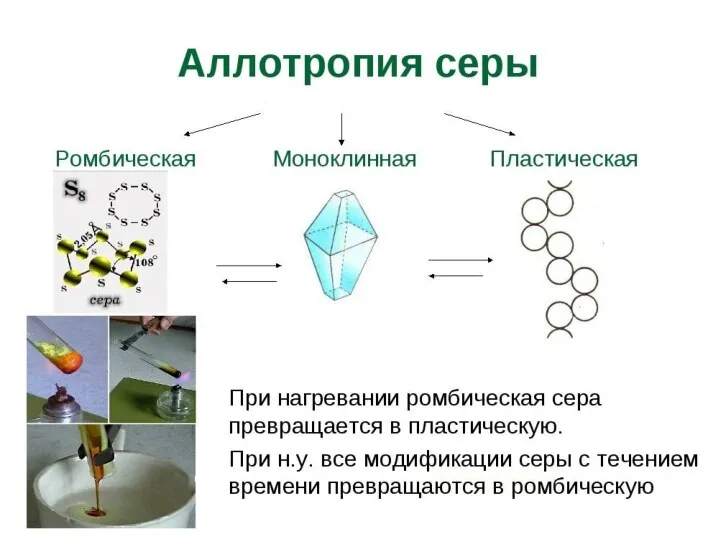
- 17. Аллотропия (от др.греч.(от др.греч. αλλος - «другой», τροπος - «поворот, свойство») - существование одного и того
- 21. Основные законы химии:
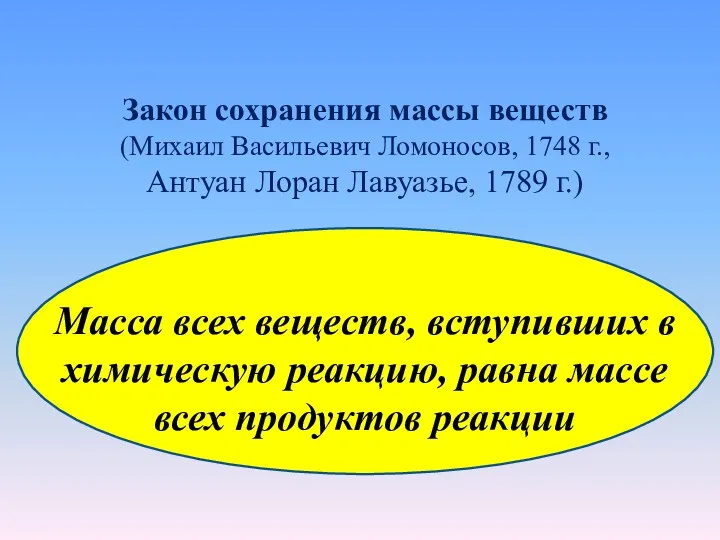
- 22. Закон сохранения массы веществ (Михаил Васильевич Ломоносов, 1748 г., Антуан Лоран Лавуазье, 1789 г.) Масса всех
- 23. Закон постоянства состава (Жозеф Луи Пруст,1808 г.) Все индивидуальные химические вещества имеют постоянный качественный и количественный
- 25. Скачать презентацию













 Емтихан сұрақтары
Емтихан сұрақтары Железо. Соединения железа
Железо. Соединения железа Решение упражнений по теме: Углеводы
Решение упражнений по теме: Углеводы Метаболизм углеводов
Метаболизм углеводов Определите положение в ПСХЭ элементов
Определите положение в ПСХЭ элементов Классификация минералов в соответствии с систематикой, утвержденной IMA
Классификация минералов в соответствии с систематикой, утвержденной IMA Теория электролитической диссоциации
Теория электролитической диссоциации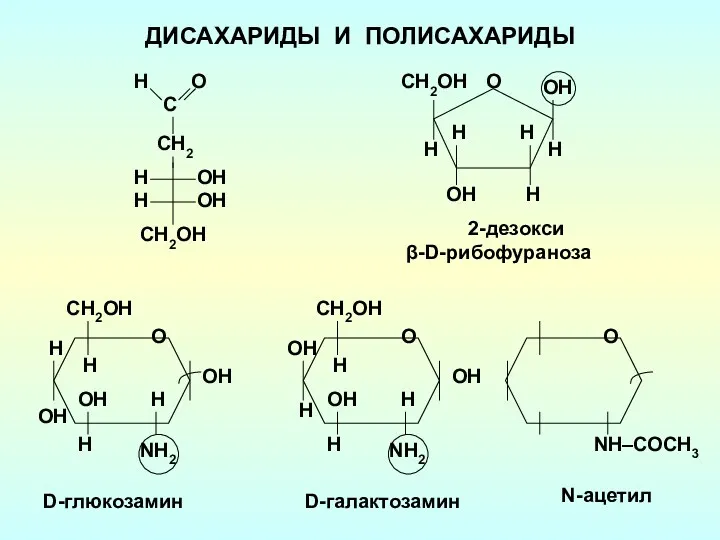 Дисахариды и полисахариды
Дисахариды и полисахариды Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2)
Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2) Классификация химических реакций по механизму реакции
Классификация химических реакций по механизму реакции Качественные реакции
Качественные реакции Фосфор и его соединения
Фосфор и его соединения Технологии создания и обработки кристаллических материалов
Технологии создания и обработки кристаллических материалов Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Двовимірний ямр. Приклади
Двовимірний ямр. Приклади Алканы
Алканы Углеводороды
Углеводороды Валентные возможности атомов химических элементов
Валентные возможности атомов химических элементов Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Кaрбоновые кислоты
Кaрбоновые кислоты Карбоновые кислоты. (Лекция 6.3)
Карбоновые кислоты. (Лекция 6.3) Серная кислота. ОХТ, лекция №7
Серная кислота. ОХТ, лекция №7 Предмет химии. Вещества
Предмет химии. Вещества Нефть и способы её переработки
Нефть и способы её переработки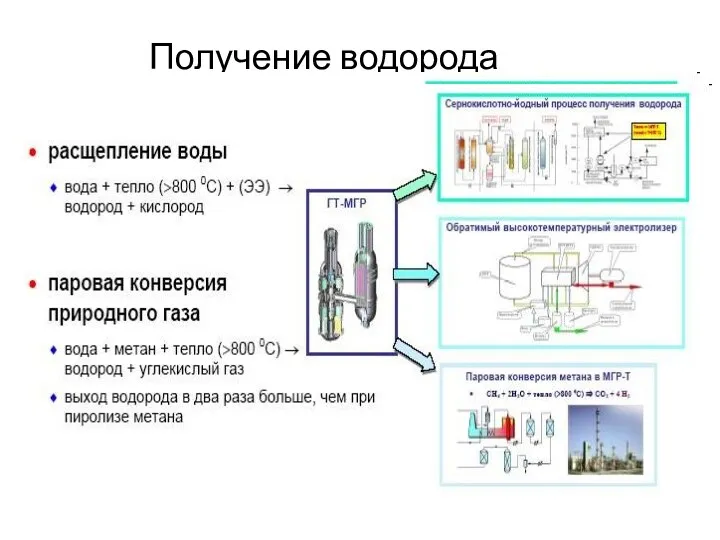 Получение водорода
Получение водорода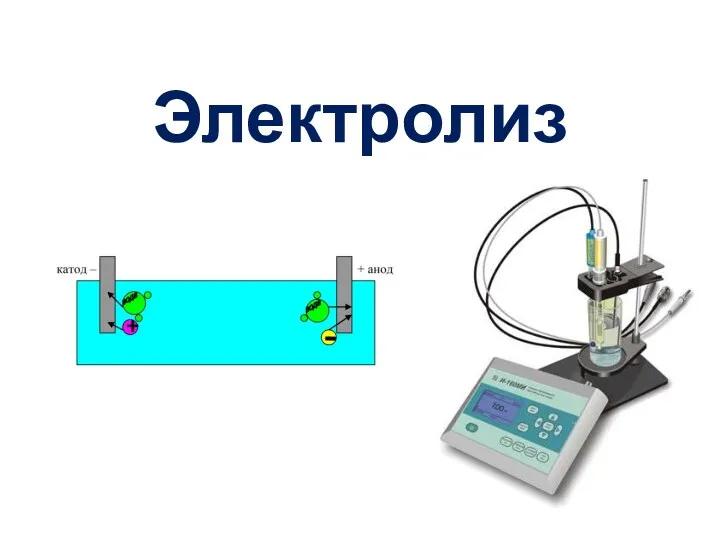 Электролиз – ОВ процесс
Электролиз – ОВ процесс Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу
Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу Материальный баланс химического реактора. Лекция № 3
Материальный баланс химического реактора. Лекция № 3