Покрытия: виды, принципы создания, свойства, применение. Получение покрытий золь-гель методом. Супергидрофобные покрытия презентация
Содержание
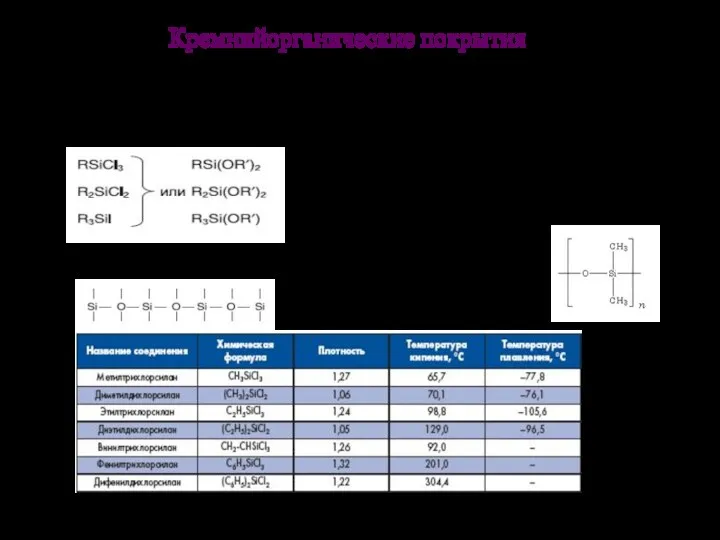
- 3. Кремнийорганические покрытия Кремнийорганические или полиорганосилоксановые смолы – ВМС, образ-ся в результате превращения различных мономерных соединений Si,
- 4. При гидролизе алкоксисоединений кремния расщепляются связи Si – ОR с образованием силанолов Si – ОН, которые
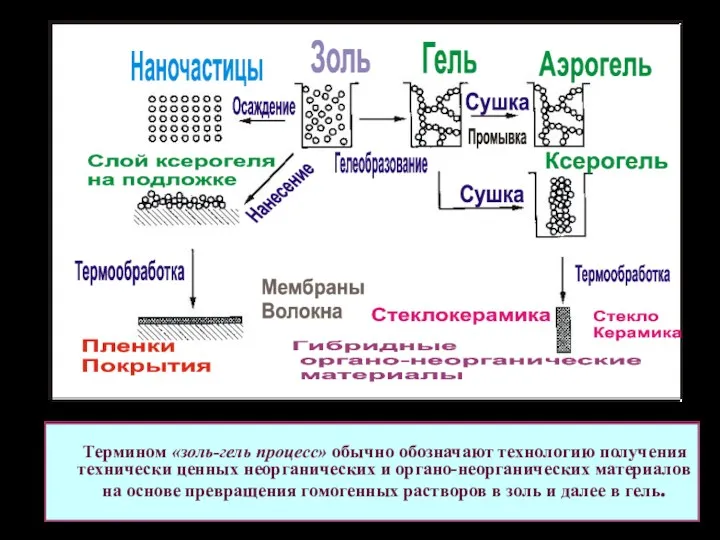
- 5. Термином «золь-гель процесс» обычно обозначают технологию получения технически ценных неорганических и органо-неорганических материалов на основе превращения
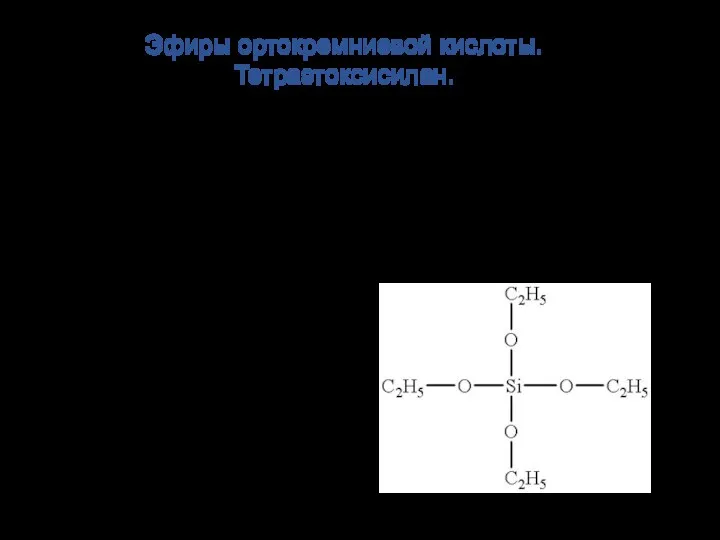
- 6. Эфиры ортокремниевой кислоты. Тетраэтоксисилан. Эфиры ортокремниевой кислоты и их производные ( -алкокси (арокси) силаны Si(OR)4 и
- 7. При гидролизе алкоксисоединений кремния расщепляются связи Si – ОR с образованием силанолов Si – ОН, которые
- 8. Нанесение покрытий 1.Предварительная обработка поверхности подложки: - Удаление посторонних веществ (механическая и химическая очистка). - Создание
- 9. Свойства и тестирование покрытий Механические свойства Оценка адгезионной прочности – метод решетчатого надреза. Твердость (испытание с
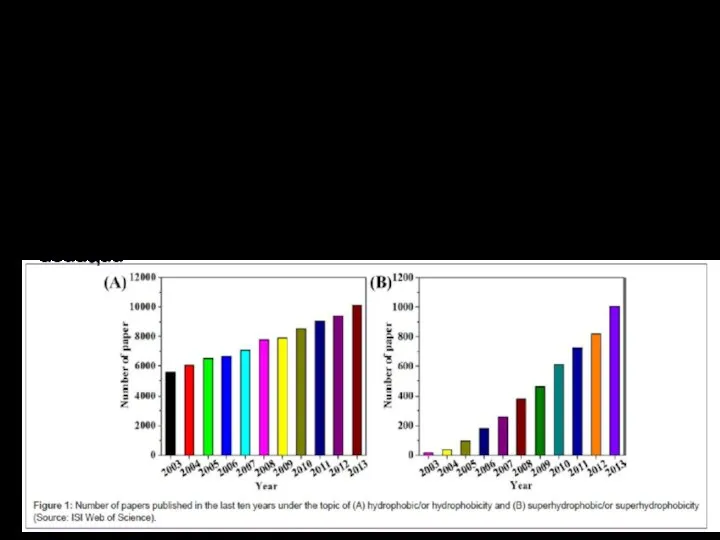
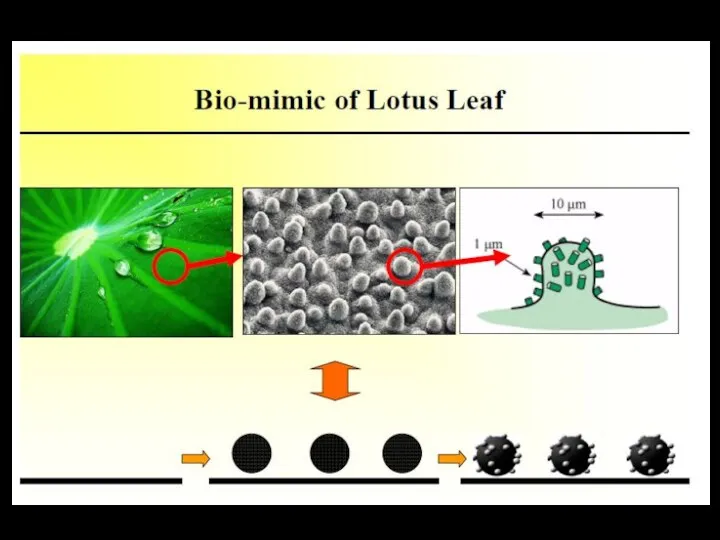
- 10. Формирование супергидрофобных покрытий золь-гель методом Neinhuis C, Barthlott W: Characterization and distribution of waterrepellent, self-cleaning plant
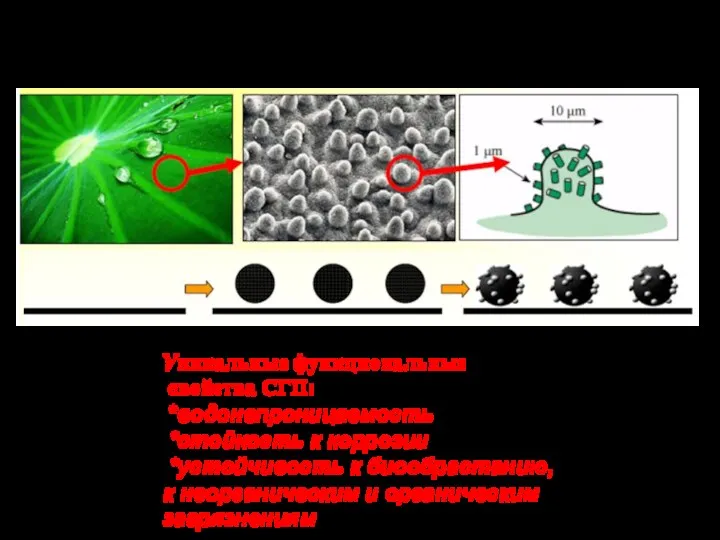
- 11. Естественные гидрофобные поверхности Поверхность многих растений и мех животных обладают водоотталкивающими свойствами. Уникальные функциональные свойства СГП:
- 12. - Супергидрофобизующая обработка зданий из стекла и бетона позволяет существенно снизить остроту проблемы очистки стекол и
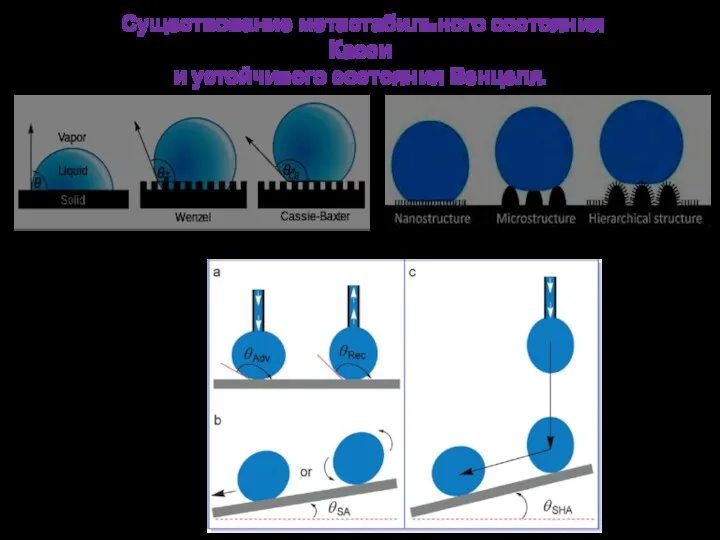
- 14. Существование метастабильного состояния Касси и устойчивого состояния Венцеля.
- 15. Методы позволяющие получать гидрофобные механически и химически устойчивые поверхности Плазменное электролитическое оксидирование (г/ф покрытия на Мg
- 16. Cупергидрофобные покрытия Определенная топология поверхности Неупорядоченный рельеф (золь-гель синтез) Литографические методы (электронное, ионное травление), темплатный синтез
- 17. Нанесение покрытий полученных золь-гель методом 1.Предварительная обработка поверхности подложки: - Удаление посторонних веществ (механическая и химическая
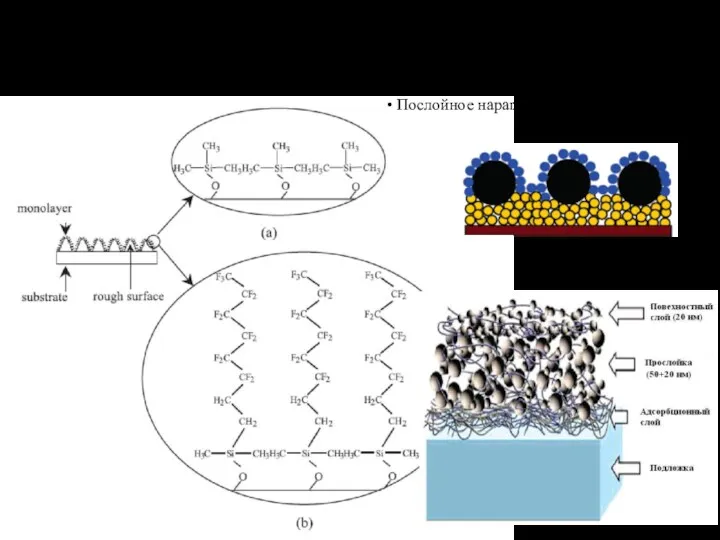
- 19. Методы создания супергидрофобной поверхности • Привитые поверхностные соединения • Коллоидные ансамбли • Послойное наращивание
- 20. Химическое модифицирование поверхности Носитель – конформационно-жесткое, ненабухающее твердое тело; Поверхностный слой – функциональные группы или адсорбционные
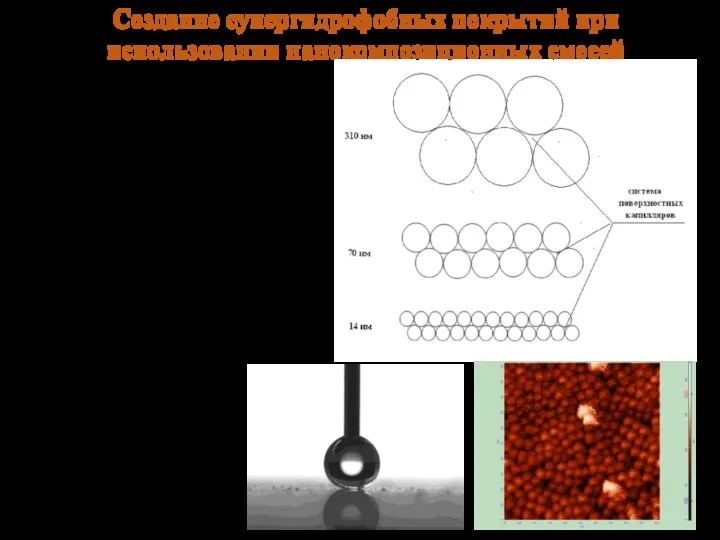
- 22. Создание супергидрофобных покрытий при использовании нанокомпозиционных смесей • Формирование нанорельефа происходит за счет адсорбции наночастиц SiO2;
- 23. Использование бимодального распределения частиц для формирования супергидрофобного нанослоя • Первый сорбционный слой наночастиц служит матрицей для
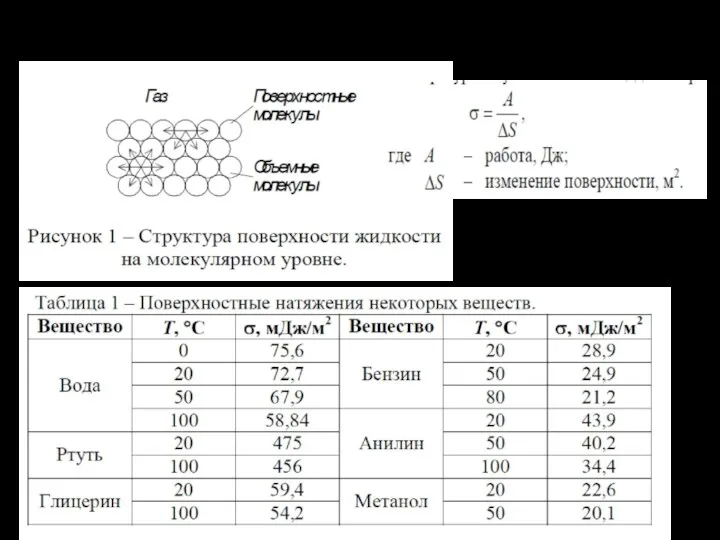
- 24. Поверхностное натяжение
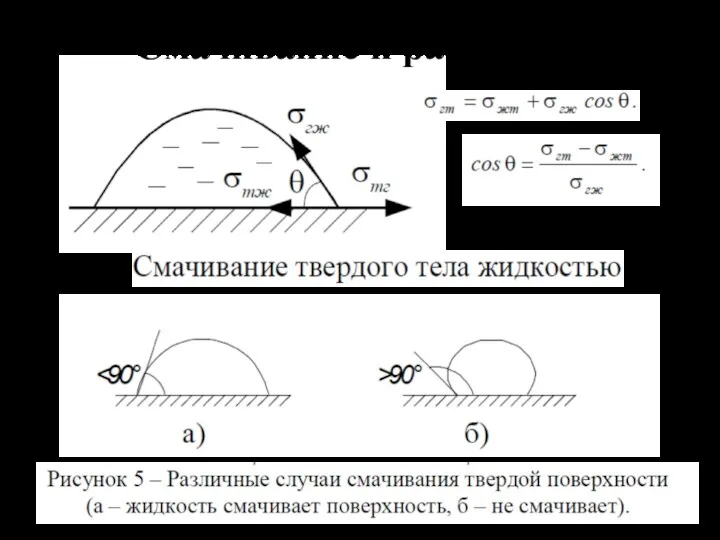
- 25. Смачивание и растекание
- 26. при θ= 00 Cos θ = 1.0 Wa /Wk = 1.0 (полное смачивание), 900 > θ
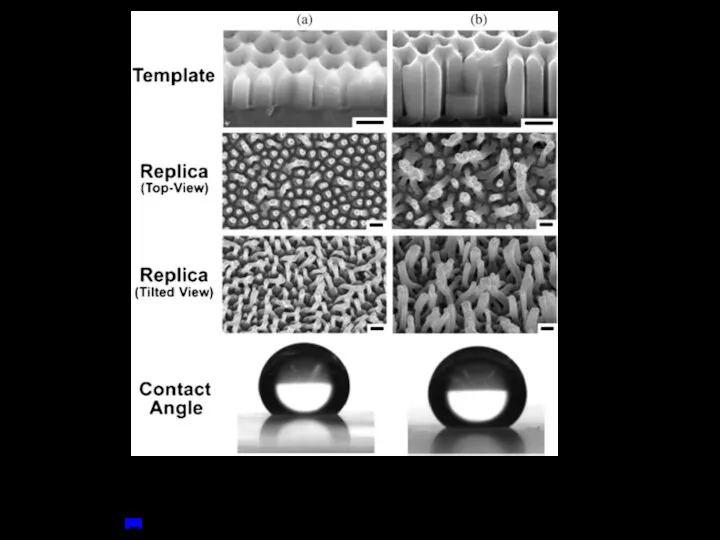
- 27. FE-SEM images of AAO templates anodized at the second anodization for 10 min (a) and 20
- 31. Связь С — F В зависимости от числа атомов F в молекуле ФС условно разделяют -
- 34. Скачать презентацию



















 Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Магия кристаллов
Магия кристаллов Пластмаси. Види пластмас. (11 клас)
Пластмаси. Види пластмас. (11 клас) Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ Производство полимеров
Производство полимеров Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте
Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте Геохимия гидротермального процесса
Геохимия гидротермального процесса Защита металлоконструкций от коррозии
Защита металлоконструкций от коррозии Химия металлов: влияние металлов на организм человека
Химия металлов: влияние металлов на организм человека Типы химических реакций
Типы химических реакций Органическая химия
Органическая химия Химия титанорганических соединений
Химия титанорганических соединений Соли и их свойства
Соли и их свойства Соединения серы
Соединения серы Химическая связь
Химическая связь Нанотехнологии в школьном образовании. Семинар учителей химии
Нанотехнологии в школьном образовании. Семинар учителей химии Генетическая связь между классами веществ
Генетическая связь между классами веществ Беломорская соль, проектная работа
Беломорская соль, проектная работа Химические свойства спиртов
Химические свойства спиртов Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Значение органической химии в жизни человека
Значение органической химии в жизни человека Классификация химических реакций
Классификация химических реакций Полезные геологические химические соединения. Получение меди из малахита
Полезные геологические химические соединения. Получение меди из малахита Механическая смесь и растворы
Механическая смесь и растворы Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений
Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений Применение солей
Применение солей Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс