Слайд 2

РЕМОНТ
Считается, что человек был знаком с действием перебродивших фруктов не менее
чем за 8000 лет до нашей эры.
Археологические находки свидетельствуют, что в Китае производились спиртосодержащие напитки из риса, мёда, винограда и других фруктов в 6500 - 7000 гг. до н. э.
Впервые спирт из вина получили в VI—VII веках арабские химики; способ получения спирта содержится в записях персидского алхимика АР-Рази.
В Европе этиловый спирт был получен из продуктов брожения в XI—XII веке, в Италии
Слайд 3
РЕМОНТ
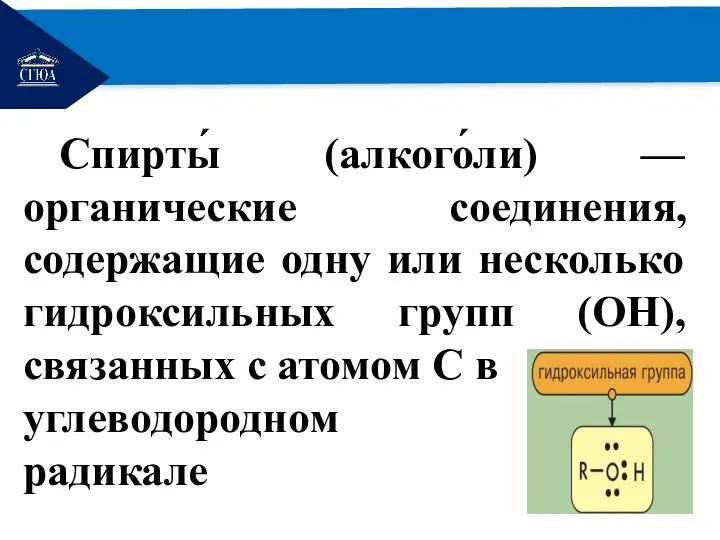
Спирты́ (алкого́ли) — органические соединения, содержащие одну или несколько гидроксильных групп
(OH), связанных с атомом С в
углеводородном
радикале
Слайд 4

РЕМОНТ
По номенклатуре ИЮПАК
названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол», положение
которого указывается арабской цифрой.
Слайд 5

РЕМОНТ
Классификация спиртов
Слайд 6
РЕМОНТ
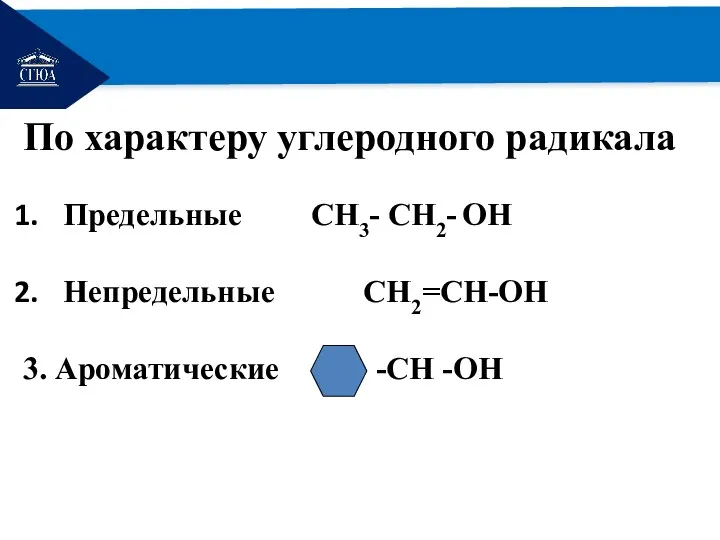
По характеру углеродного радикала
Предельные CH3- CH2- OH
Непредельные CH2=CH-OH
3. Ароматические -СН
-ОН
Слайд 7

РЕМОНТ
По количеству гидроксильных групп
1. Одноатомные СН3-CH2-ОН
2. Многоатомные СН2-СН2
| |
ОН ОН
СН2-СН-СН2
| | |
ОН ОН ОН
СН2-СН-СН-CH-CH-СН2
| | | | | |
ОН ОН ОН ОН OH OH
Слайд 8
РЕМОНТ
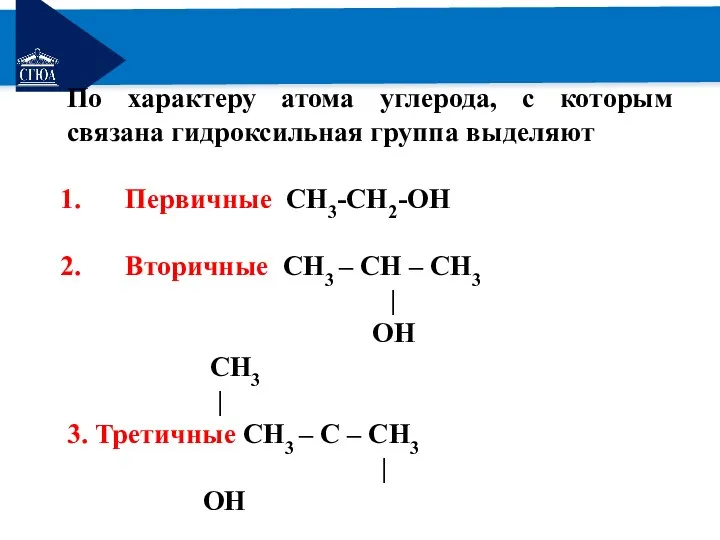
По характеру атома углерода, с которым связана гидроксильная группа выделяют
Первичные
СН3-СН2-ОН
Вторичные СН3 – СН – СН3
|
OH
СН3
|
3. Третичные СН3 – С – СН3
|
OH
Слайд 9

РЕМОНТ
Предельные одноатомные спирты (алканолы)
- органические соединения, в молекулах которых
алкильный радикал (CnH2n+1) связан с гидроксильной группой
Общая формула Cn H 2n+1OH
Слайд 10
РЕМОНТ
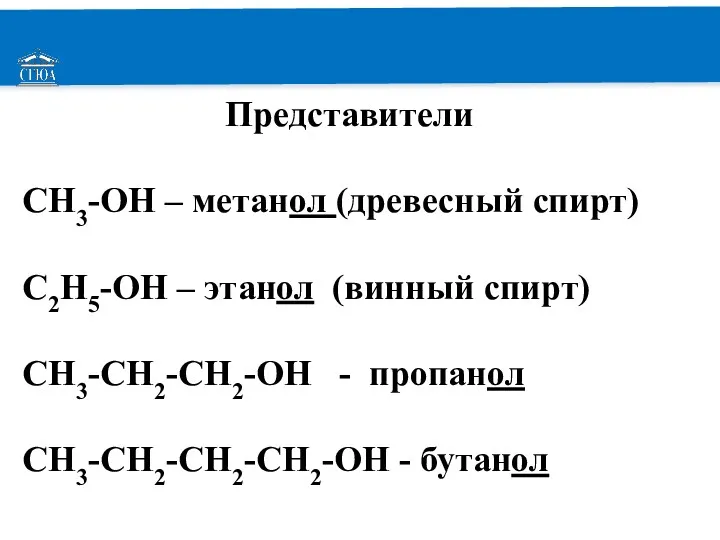
Представители
CH3-OH – метанол (древесный спирт)
C2H5-OH – этанол (винный спирт)
СН3-СН2-СН2-ОН - пропанол
СН3-СН2-СН2-СН2-ОН
- бутанол
Слайд 11
РЕМОНТ
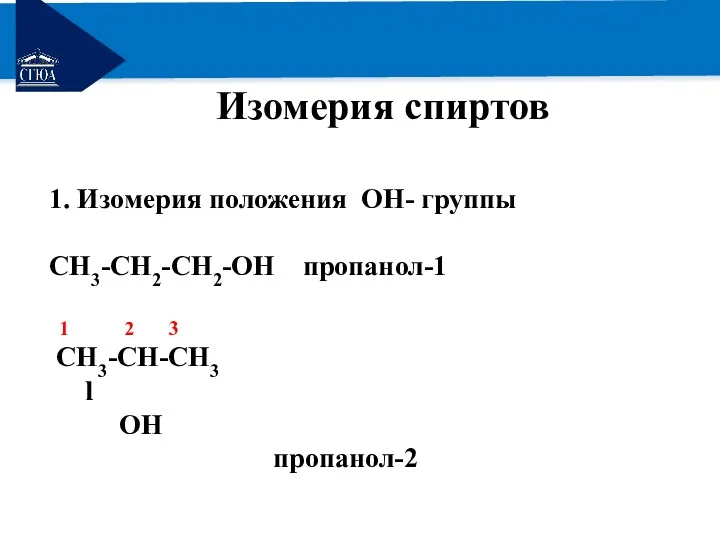
Изомерия спиртов
1. Изомерия положения OH- группы
CH3-CH2-CH2-OH пропанол-1
1 2 3
CH3-CH-CH3
l
OH
пропанол-2
Слайд 12

РЕМОНТ
Изомерия спиртов
2. Изомерия углеродного скелета
CH3-CH2-CH2-CH2-OH Бутанол
3 2 1
CH3-CH-CH2-OH
l
CH3
2 - метилпропанол
Слайд 13

РЕМОНТ
Физические свойства спиртов
Все алканолы легче воды, бесцветны, жидкие имеют резкий
запах, твердые запаха не имеют. Метанол, этанол и пропанол неограниченно растворяются в воде, с увеличением числа углеродных атомов растворимость алканолов в воде уменьшается, высшие спирты не растворяются в воде.
Метанол — сильный яд нервного и сердечно-сосудистого действия; поражает органы зрения вплоть до полной слепоты. В больших дозах (30 г и более) вызывает смерть.
Этанол - его употребление приводит к нарушению важнейших функций организма, тяжелому поражению органов и систем.
Слайд 14

РЕМОНТ
Химические свойства спиртов
Слайд 15

РЕМОНТ
1.Спирты как слабые кислоты реагируют со щелочными металлами:
С2Н5ОН + Na
→ C2H5ONa + H2
алкоголят натрия
Слайд 16

РЕМОНТ
2. Как слабые основания реагируют с сильными кислотами:
Н2SO4
С2Н5ОН + НСl
Слайд 17

РЕМОНТ
3. Окисление
a) Горение:
C2H5OH+ 3O2 → 2CO2+3H2O + Q
б) Окисление спиртов
оксидом меди до альдегидов:
Слайд 18
РЕМОНТ
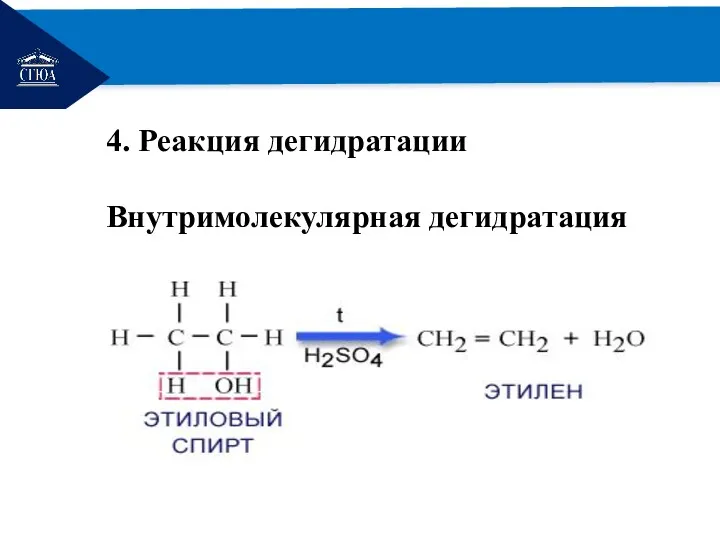
4. Реакция дегидратации
Внутримолекулярная дегидратация
Слайд 19
РЕМОНТ
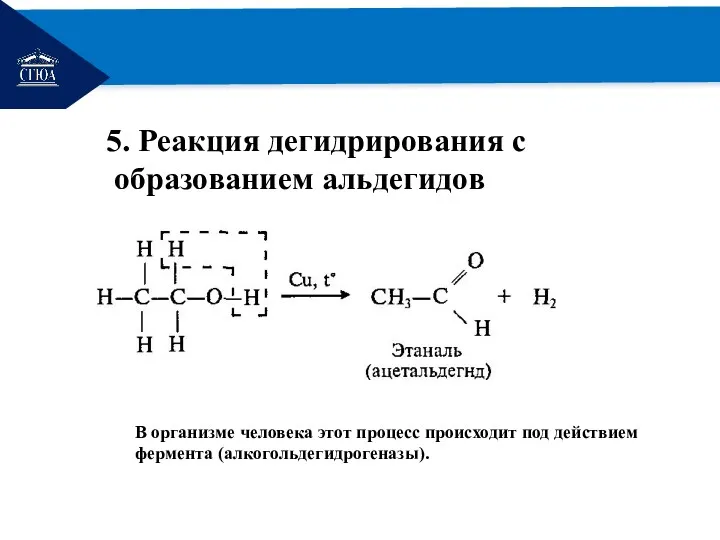
5. Реакция дегидрирования с
образованием альдегидов
В организме человека этот процесс происходит
под действием фермента (алкогольдегидрогеназы).
Слайд 20

РЕМОНТ
6. Дегидрирование и дегидратация -реакция Лебедева
2С2Н5ОН →СН2=СН-СН=СН2+2Н2О+Н2
Этанол
бутадиен -1,3
Слайд 21

РЕМОНТ
7. Этерификация – реакция между спиртами и кислотами с
образованием сложных эфиров
Слайд 22
РЕМОНТ
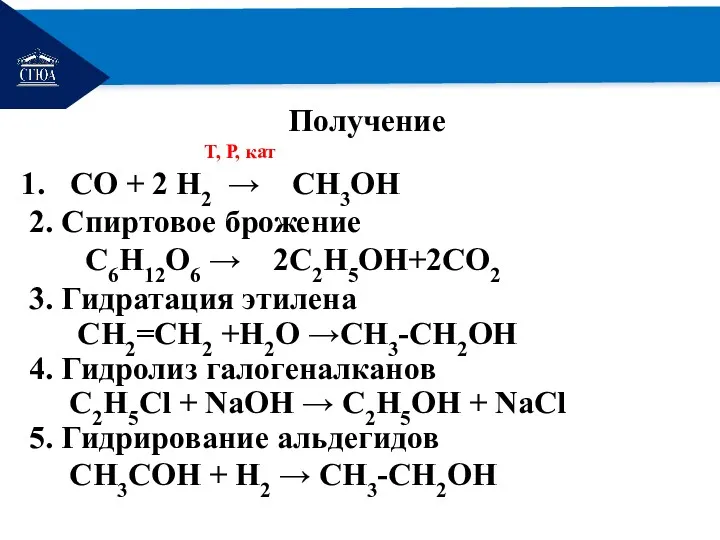
Получение
Т, Р, кат
СО + 2 Н2 → СН3ОН
2.
Спиртовое брожение
C6H12O6 → 2С2Н5OH+2CO2
3. Гидратация этилена
СН2=СН2 +Н2О →СН3-СН2ОН
4. Гидролиз галогеналканов
C2H5Cl + NaOH → C2H5OH + NaCl 5. Гидрирование альдегидов
CH3СОН + Н2 → СН3-СН2ОН
Слайд 23

РЕМОНТ
Применение
1. производство уксусной кислоты и алкогольных напитков, лаков, сложных
эфиров, синтетических каучуков;
2. косметика и парфюмерия;
3. медицинские препараты;
4. топливо.
Слайд 24

РЕМОНТ
Многоатомные спирты
Слайд 25

РЕМОНТ
Этандиол (этиленгликоль) -сиропообразная жидкость
сладкого вкуса, без запаха,
ядовит. Смертельная
доза для человека - 50-150 мл.
Хорошо смешивается с водой и спиртом, гигроскопичен.
Компонент автомобильных антифризов и незамерзающих жидкостей.
Применяется для получения лавсана.
Слайд 26

РЕМОНТ
Пропантриол – глицерин
Сиропообразная, гигроскопичная,
сладкая на вкус жидкость.
Неограниченно растворим
в воде.
С азотной кислотой с образует нитроглицерин.
С карбоновыми кислотами образует жиры и масла.
Не ядовит.
Слайд 27

РЕМОНТ
Применение глицерина
В производстве взрывчатых веществ и сосудорасширяющего лекарства (нитроглицерина), пластмасс .
В
текстильной и кожевенной промышленности.
Как пищевая добавка E422.
Входит в состав кремов, помад, зубных паст, моющих средств, предотвращая их от высыхания и способствуя увлажнению и смягчению кожи
Слайд 28
РЕМОНТ
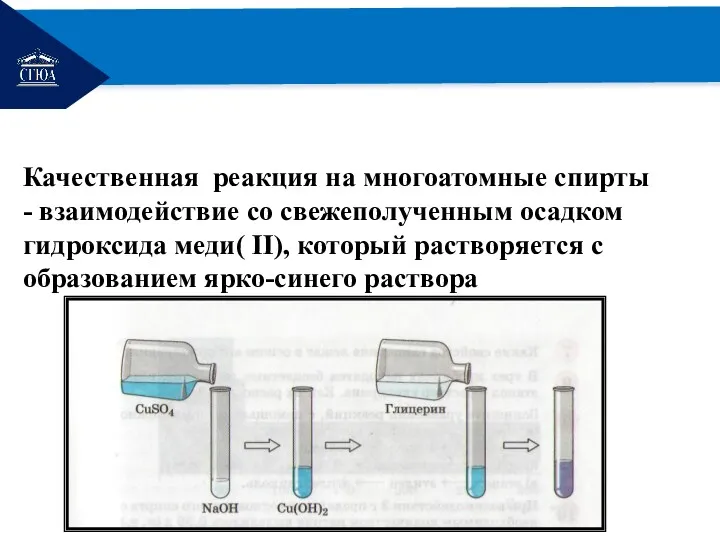
Качественная реакция на многоатомные спирты
- взаимодействие со свежеполученным осадком гидроксида
меди( II), который растворяется с образованием ярко-синего раствора



























 Удивительные свойства воды
Удивительные свойства воды Electronică aplicată. (Curs 2)
Electronică aplicată. (Curs 2) Пространственное строение органических соединений. (Лекция 2)
Пространственное строение органических соединений. (Лекция 2) 20230416_urok_na_20.02.2023
20230416_urok_na_20.02.2023 Неізогіпсичні перетворення функціональних груп. Реакції окиснення
Неізогіпсичні перетворення функціональних груп. Реакції окиснення Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Электронная конфигурация К. Классификация химических элементов. 8 класс
Электронная конфигурация К. Классификация химических элементов. 8 класс Спирты. Физические и химические свойства
Спирты. Физические и химические свойства Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування
Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування 20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii
20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Типовые процессы технологии неорганических веществ. (Тема 3)
Типовые процессы технологии неорганических веществ. (Тема 3) ЕГЭ Химия. Задание №5
ЕГЭ Химия. Задание №5 Изучение строения и свойств глюкозы
Изучение строения и свойств глюкозы Железо и его соединения
Железо и его соединения Химические превращения веществ
Химические превращения веществ Белки. Функции белков
Белки. Функции белков Високомолекулярні сполуки. Полімери
Високомолекулярні сполуки. Полімери Простые спектры 1Н ЯМР
Простые спектры 1Н ЯМР Значення хімічних процесів у природі
Значення хімічних процесів у природі Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас Реакции ионного обмена
Реакции ионного обмена Жиры. Мыла. 10 класс
Жиры. Мыла. 10 класс Группа редкоземельных элементов
Группа редкоземельных элементов Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі
Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі Железо
Железо Crystallography. Part 4: Crystal Forms Twinning
Crystallography. Part 4: Crystal Forms Twinning Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)