Содержание
- 2. Строение атомного ядра Например, в ядро атома гелия входят 2 электрона, а его ядро состоит из
- 3. Электрон Электрон (от др.-греч. ἤλεκτρον - янтарь) - стабильная, отрицательно заряженная элементарная частица, одна из основных
- 4. Электрон Электроны вращаются вокруг ядра, словно планеты вокруг Солнца. Они удерживаются на орбите кулоновской силой. Если
- 5. Атом - квантовая система, т.е. система микрочастиц, поведение которых описывается законами квантовой механики. Согласно законам, энергетическое
- 6. Квантовые числа Орбитальное квантовое число характеризует форму орбит (они могут быть как круговыми, так и эллиптическими).
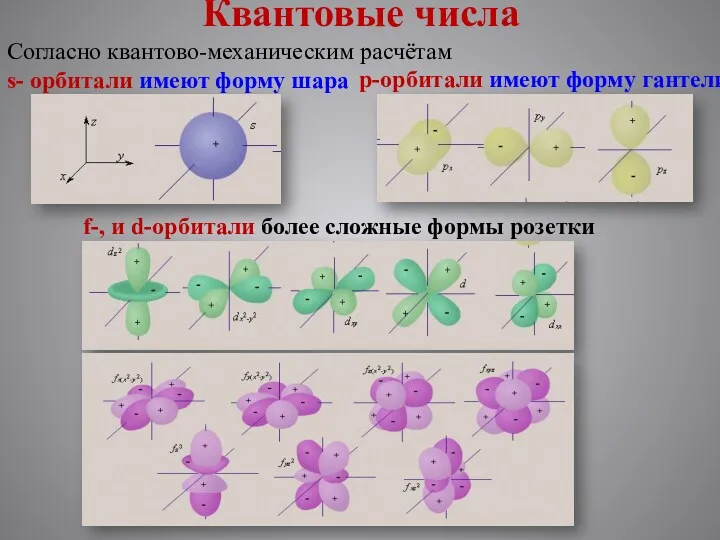
- 7. Квантовые числа Согласно квантово-механическим расчётам s- орбитали имеют форму шара p-орбитали имеют форму гантели f-, и
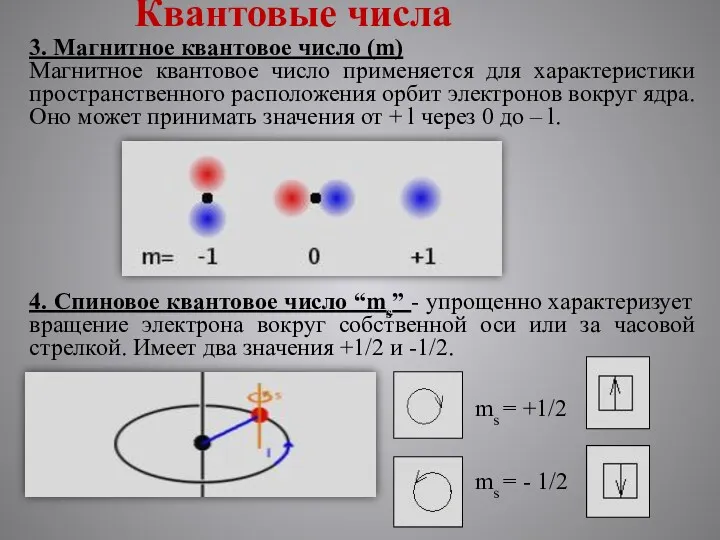
- 8. Квантовые числа 3. Магнитное квантовое число (m) Магнитное квантовое число применяется для характеристики пространственного расположения орбит
- 9. Принципы заполнения атомных орбиталей Распределение электронов в атоме, находящемся в основном состоянии определяется зарядом ядра. При
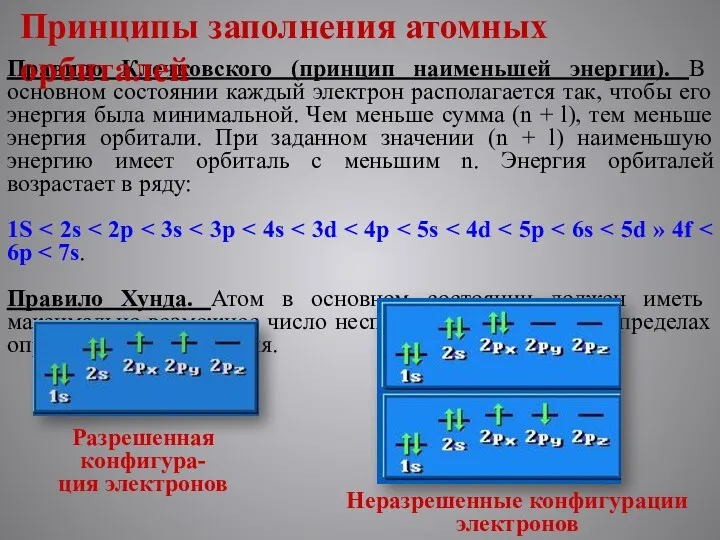
- 10. Правило Клечковского (принцип наименьшей энергии). В основном состоянии каждый электрон располагается так, чтобы его энергия была
- 11. Полная электронная формула элемента Запись, отражающая распределение электронов в атоме химического элемента по энергетическим уровням и
- 12. Открытие периодического закона Д. И. Менделеева Открытие периодического закона и разработка периодической системы химических элементов Д.
- 13. Открытие периодического закона Д. И. Менделеева Однако, несмотря на огромную значимость такого вывода, периодический закон и
- 14. Периодический закон Д. И. Менделеева В основу Периодического закона Д.И. Менделеев положил атомные массы (ранее -
- 15. В связи с открытием закона Мозле современная формулировка периодического закона следующая: Свойство элементов, а так же
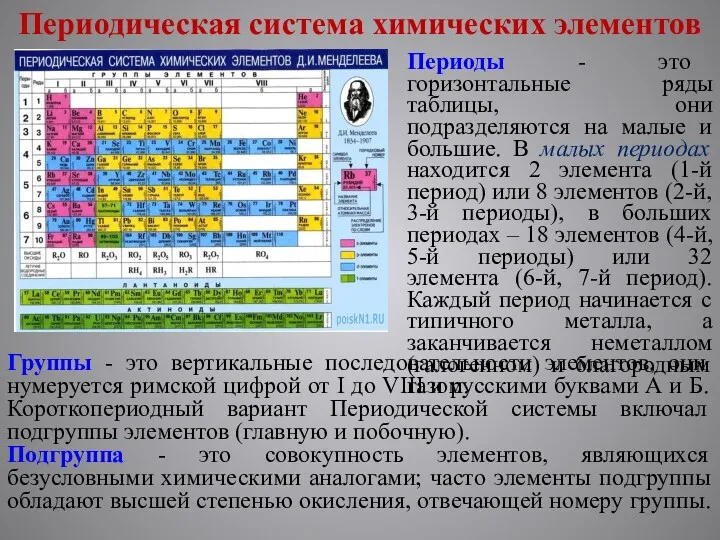
- 16. Периодическая система химических элементов На основе Периодического закона Д. И. Менделеев создал Периодическую систему химических элементов,
- 17. Группы - это вертикальные последовательности элементов, они нумеруется римской цифрой от I до VIII и русскими
- 18. Периодическая система химических элементов В А-группах химические свойства элементов могут меняться в широком диапазоне от неметаллических
- 19. Периодическая система химических элементов Форма Периодической системы, которую предложил Д. И. Менделеева, называлась короткопериодной или классической.
- 21. Скачать презентацию














 Цветные металлы и сплавы
Цветные металлы и сплавы Массовая доля вещества в растворе
Массовая доля вещества в растворе Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2)
Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2) Анилин. Строение. Физические и химические свойства
Анилин. Строение. Физические и химические свойства Технология промышленных газов
Технология промышленных газов Химия вокруг нас
Химия вокруг нас Непредельные, ненасыщенные, ацетиленовые алкины
Непредельные, ненасыщенные, ацетиленовые алкины Перегонка с водяным паром
Перегонка с водяным паром Липиды. Классификация липидов
Липиды. Классификация липидов Основания. Номенклатура оснований
Основания. Номенклатура оснований Химические свойства металлов
Химические свойства металлов Процесс в химическом реакторе
Процесс в химическом реакторе Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Гидроксиды. Основания: способы получения
Гидроксиды. Основания: способы получения Спирты
Спирты Кондуктометрия и кондуктометрическое титрование
Кондуктометрия и кондуктометрическое титрование Тяжелые металлы
Тяжелые металлы Горение жидкостей
Горение жидкостей Определение фосфатов, железа, хлоридов
Определение фосфатов, железа, хлоридов Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья Металлическая связь
Металлическая связь Химический состав воздуха
Химический состав воздуха Сладкая жизнь. Проектно-исследовательская работа
Сладкая жизнь. Проектно-исследовательская работа Хімічні явища в побуті
Хімічні явища в побуті Кристаллы. Кристаллические вещества
Кристаллы. Кристаллические вещества Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)