Урок 19. Практична робота №1. Реакції йонного обміну між електролітами у водних розчинах презентация
Содержание
- 2. Мета: - дослідити умови перебігу реакцій йонного обміну ; - навчитися складати повні йонні та скорочені
- 3. Реакції йонного обміну відбуваються до кінця в трьох випадках: якщо утворюється осад якщо виділяється газ якщо
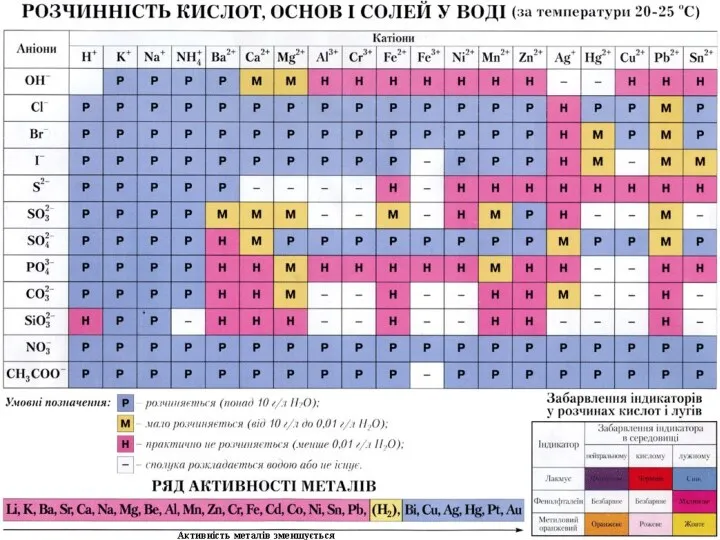
- 4. Обладнання: таблиця розчинності солей, кислот і основ; пробірки, штатив; реактиви: розчини - MgCI2; AgNO3; Na2CO3; CuSO4
- 5. Хід роботи: Завдання 1. Повторити правила техніки безпеки при роботі з реактивами
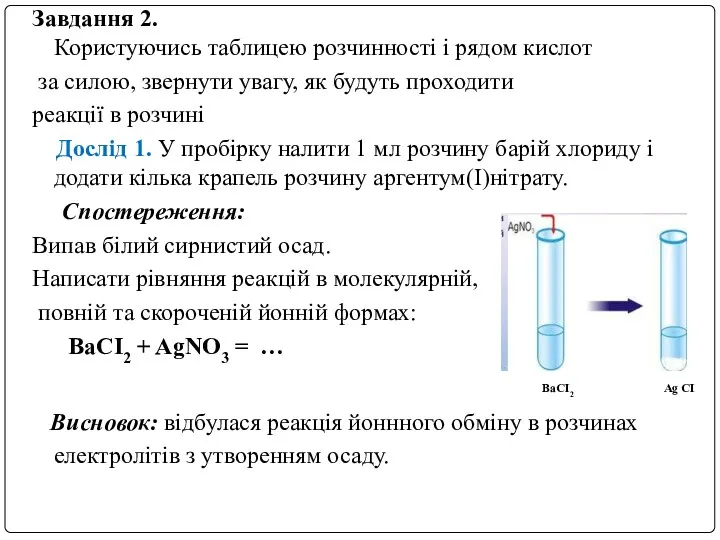
- 7. Завдання 2. Користуючись таблицею розчинності і рядом кислот за силою, звернути увагу, як будуть проходити реакції
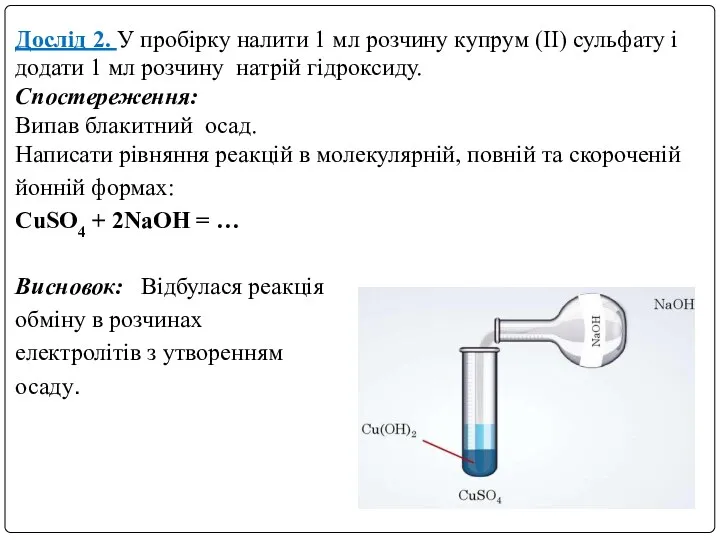
- 8. Дослід 2. У пробірку налити 1 мл розчину купрум (ІІ) сульфату і додати 1 мл розчину
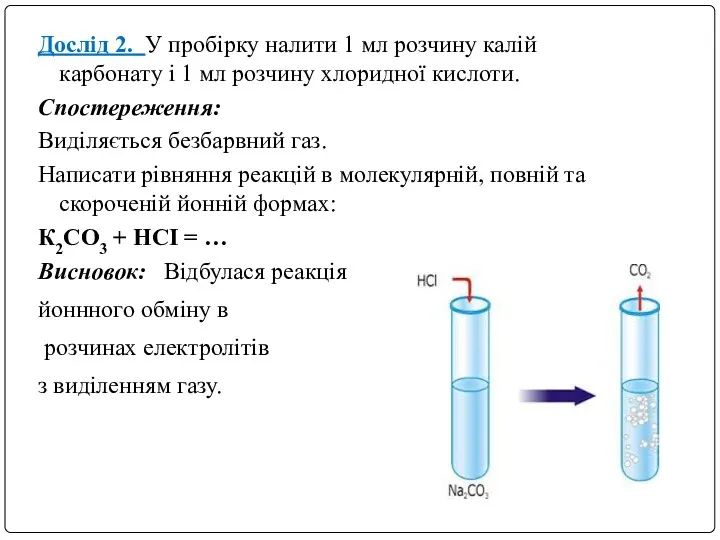
- 9. Дослід 2. У пробірку налити 1 мл розчину калій карбонату і 1 мл розчину хлоридної кислоти.
- 10. Завдання 3. Реакції нейтралізації Дослід1. У пробірку налити 1 мл розчину калій гідроксиду, додати 1-2 краплі
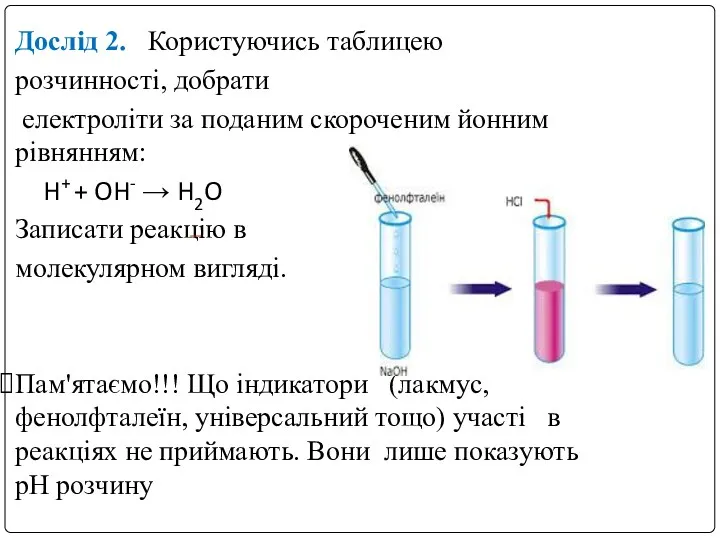
- 11. Дослід 2. Користуючись таблицею розчинності, добрати електроліти за поданим скороченим йонним рівнянням: H+ + OH- →
- 13. Виконати практичну роботу в зошитах і вислати на перевірку Домашнє завдання:
- 15. Скачать презентацию







 Химия биогенных элементов p -блока
Химия биогенных элементов p -блока Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Физические и химические явления. Признаки и условия протекания химических реакций
Физические и химические явления. Признаки и условия протекания химических реакций Оксид серы (VI). Серная кислота
Оксид серы (VI). Серная кислота Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Качественные реакции на органические вещества
Качественные реакции на органические вещества Автомобильные пластичные смазки
Автомобильные пластичные смазки Вода-растворитель. Работа воды в природе
Вода-растворитель. Работа воды в природе Хлороводород и соляная кислота
Хлороводород и соляная кислота Взаємодія кисеню зі складними речовинами
Взаємодія кисеню зі складними речовинами Хозяйственные товары из пластических масс
Хозяйственные товары из пластических масс Максимально очищенные фитопрепараты. Технология и стандартизация
Максимально очищенные фитопрепараты. Технология и стандартизация Углерод. Элемент IV группы
Углерод. Элемент IV группы Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворах
Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворах Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Дисперсная система
Дисперсная система Органічні речовини в живій природі. Рівні структурної органшзації
Органічні речовини в живій природі. Рівні структурної органшзації Общая характеристика металлов
Общая характеристика металлов Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері
Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері Кремний и его соединения
Кремний и его соединения Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Химический элемент и вещество
Химический элемент и вещество Уравнения химических реакций
Уравнения химических реакций Аміни
Аміни Обмен сложных липидов
Обмен сложных липидов Непредельные углеводороды: алкены, олефины
Непредельные углеводороды: алкены, олефины Проблема содержания нитратов в пищевых продуктах
Проблема содержания нитратов в пищевых продуктах Ұшқыш уларды оқшаулауды теориялық негіздеу
Ұшқыш уларды оқшаулауды теориялық негіздеу