Содержание
- 2. 1 15.09.2016 Урок 8 класса. Атомы и молекулы. Простые и сложные вещества.
- 3. 2 Молекулы и Атомы 15.09.2016 Вещества бывают молекулярного и немолекулярного строения. Молекулярные соединения Немолекулярные соединения NaCl
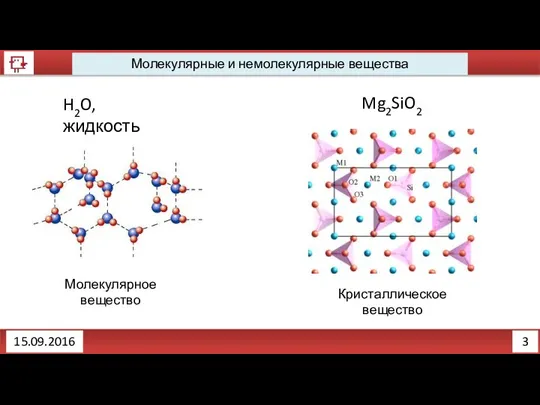
- 4. 3 Молекулярные и немолекулярные вещества 15.09.2016 H2O, жидкость Mg2SiO2 Кристаллическое вещество Молекулярное вещество
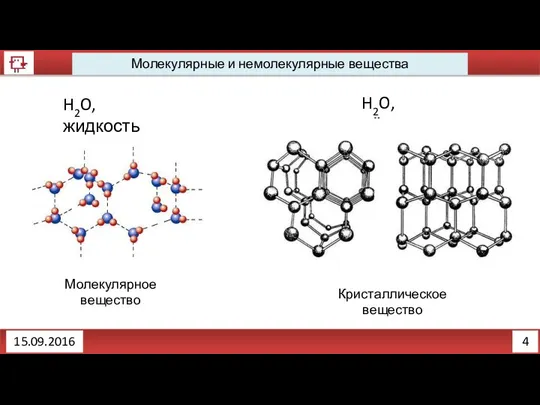
- 5. 4 Молекулярные и немолекулярные вещества 15.09.2016 H2O, жидкость H2O, лёд Кристаллическое вещество Молекулярное вещество
- 6. 5 Порядок 15.09.2016 В твёрдых и жидких телах существует упорядоченность во взаимном расположении атомов или молекул.
- 7. 6 Порядок 15.09.2016 Дальний порядок Ближний порядок Безпорядок
- 8. 7 Простые и сложные вещества 15.09.2016
- 9. 8 Простые и сложные вещества Если вещество можно разложить на другие вещества – оно является сложным.
- 10. 9 Различие смесей и химических соединений 15.09.2016
- 11. 10 Химические элементы Химический элемент – определенный тип атомов. Химический элемент – это вид атомов с
- 12. 11 Символы химических элементов Почти все символы для химических элементов придумал Берцелиус. 15.09.2016 Он предложил присваивать
- 13. 12 Масса атома 15.09.2016 Одной из характеристик атома является его масса. Только она очень мала, масса
- 14. 13 Масса атома 15.09.2016 С имеет массу 12 а.е.м. Давайте посчитаем, какая масса у Н и
- 16. Скачать презентацию








 Непредельные углеводороды: алкены, олефины
Непредельные углеводороды: алкены, олефины Основы коррозии и защиты металлов. Виды коррозии металлов
Основы коррозии и защиты металлов. Виды коррозии металлов Реакционная способность твердых тел и способы ее регулирования
Реакционная способность твердых тел и способы ее регулирования Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Водород
Водород Химические профессии на стройках Олимпиады
Химические профессии на стройках Олимпиады Основные классы неорганических веществ
Основные классы неорганических веществ Химическое равновесие. Азот (продолжение). 9 класс
Химическое равновесие. Азот (продолжение). 9 класс Физические и химические свойства алкенов
Физические и химические свойства алкенов Распространение водорода в природе. Получение в лаболатории
Распространение водорода в природе. Получение в лаболатории Природные источники углеводородов
Природные источники углеводородов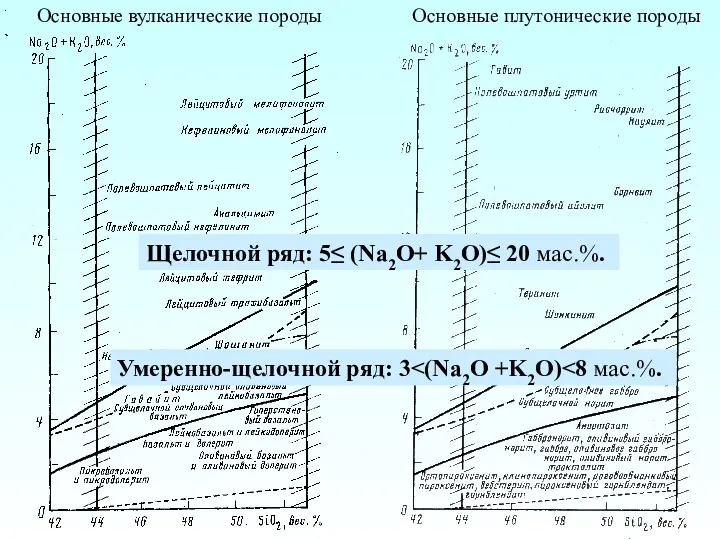 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Стронций
Стронций Пластмасса, пластикалық материалдар
Пластмасса, пластикалық материалдар Генетическая связь органических и неорганических соединений
Генетическая связь органических и неорганических соединений Строение атома. Химия. 11 класс
Строение атома. Химия. 11 класс Нефть и ее роль в мировой экономике
Нефть и ее роль в мировой экономике Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Тепловой эффект химических реакций
Тепловой эффект химических реакций Алкадиены
Алкадиены Теория электролитической диссоциации
Теория электролитической диссоциации Производные 8-замещенных хинолина
Производные 8-замещенных хинолина Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Реакции ионного обмена
Реакции ионного обмена Технология производства бутилкаучука
Технология производства бутилкаучука Алкины — углеводороды, содержащие тройную связь между атомами углерода
Алкины — углеводороды, содержащие тройную связь между атомами углерода Introduction in bioorganic chemistry. Isomerism and structure of organic compounds
Introduction in bioorganic chemistry. Isomerism and structure of organic compounds Пниктогены - элеметны VA группы
Пниктогены - элеметны VA группы