Слайд 2

История:
Пропилен (пропен) Н3С—СН==СН2 относится к углеводородам ряда этилена (алкены или олефины).
Алкены, или олефины (от лат. olefiant - масло — старое название, но широко используемое в химической литературе. Поводом к такому названию послужил хлористый этилен, полученный в XVIII столетии, — жидкое маслянист вещество.) — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна двойная связь.
Слайд 3

Физические свойства:
Пропилен представляет из себя газообразное вещество с низкой температурой кипения
t кип=-47,7 °С и температурой плавления t пл= -187,6 °С, оптическая плотность d204=0,5193.
Слайд 4
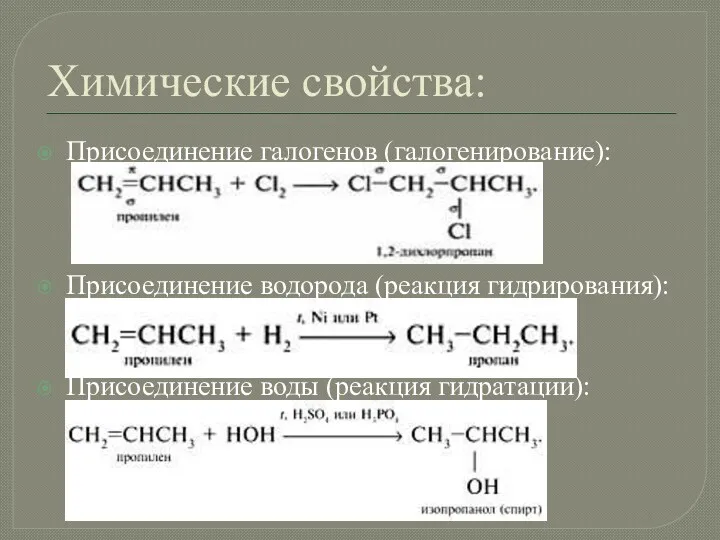
Химические свойства:
Присоединение галогенов (галогенирование):
Присоединение водорода (реакция гидрирования):
Присоединение воды (реакция гидратации):
Слайд 5

Продолжение хим.свойств
Присоединение галогеноводородов (HHal) и воды происходит по правилу В.В.Марковникова (1869):
Горение
на воздухе. При поджигании горит на воздухе:
Слайд 6

Получение:
Из лабораторных способов получения пропилена можно отметить следующие:
1. Отщепление галогеноводорода
от галогеналкилов при действии на них спиртового раствора щелочи:
H2C—CH2 – CH3 = H2C==CH2– CH3 + KCl + H2O | |
Cl H
K—ОH
2. Гидрирование пропина в присутствии катализатора (Pd):
H—C≡C— CH3 + H2 = H2C==CH— CH3
3. Дегидратация пропилового спирта (отщепление воды). В качестве катализатора используют кислоты (серную или фосфорную) или А12O3:
Н2С—СН2 — CH3 = Н2С==СН — CH3 + Н2О | |
H -OH
Слайд 7

Применение:
Пропилен находит свое применение в промышленном синтезе.
Полипропилен. Производство полипропилена в
промышленности началось в 1954 году благодаря работам Натты, который использовал для полимеризации пропилена каталитическую систему Циглера. Натта впервые получил стереорегулярный полимер, названный им изотактическим; в нем все метильные группы расположены по одну сторону цепи, что способствует благоприятной "упаковке" полимерных молекул и определяет хорошие механические свойства полипропилена.






 Кристаллическое строение и кристаллизация металлов
Кристаллическое строение и кристаллизация металлов Бережём планету вместе. Нефть
Бережём планету вместе. Нефть Органіка. Органічні речовини
Органіка. Органічні речовини Благородные газы
Благородные газы Растворы и свойства растворов. Лекция 3
Растворы и свойства растворов. Лекция 3 Типы химических реакций
Типы химических реакций Ионное произведение воды. Водородный показатель воды
Ионное произведение воды. Водородный показатель воды Новинки СН старт: июль 2016 Профессиональная химия PRO service
Новинки СН старт: июль 2016 Профессиональная химия PRO service Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Сложные углеводы. Олигосахариды и полисахариды
Сложные углеводы. Олигосахариды и полисахариды Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Драгоценные камни
Драгоценные камни Натрий алкилсульфонаттарын алу. №4 лекция
Натрий алкилсульфонаттарын алу. №4 лекция CaSO4 кристаллының ас жазықтығына проекциясының құрылымдық моделі
CaSO4 кристаллының ас жазықтығына проекциясының құрылымдық моделі Алкадиены. Циклоалканы. Лекция № 5
Алкадиены. Циклоалканы. Лекция № 5 Химический тренажер. Химические элементы
Химический тренажер. Химические элементы Осадительное титрование. (Лекция 27)
Осадительное титрование. (Лекция 27) Объёмная доля компонента смеси
Объёмная доля компонента смеси Роль воды в химических реакциях
Роль воды в химических реакциях Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса
Термокаталитические процессы. Каталитический крекинг. Классификация и основные факторы процесса Предмет и задачи химии. Вещества и их свойства. (Продолжение)
Предмет и задачи химии. Вещества и их свойства. (Продолжение) Углеводы. (Лекция 7)
Углеводы. (Лекция 7) Показатели жесткости воды
Показатели жесткости воды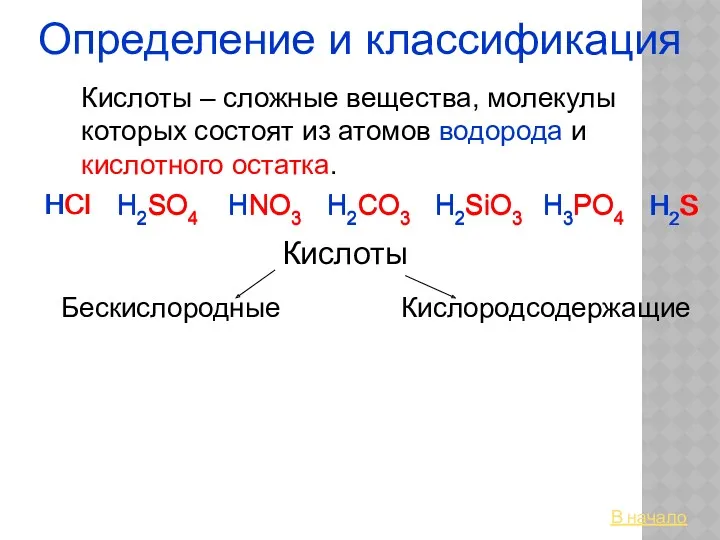 Кислоты. Определение и классификация
Кислоты. Определение и классификация Приёмы обращения с лабораторным оборудованием
Приёмы обращения с лабораторным оборудованием Нуклеиновые кислоты
Нуклеиновые кислоты Радиохимия
Радиохимия Элементы химической термодинамики. 1 и 2 законы термодинамики. Химическое равновесие
Элементы химической термодинамики. 1 и 2 законы термодинамики. Химическое равновесие