Содержание
- 2. Жизнь – это способ существования белковых тел. Ф.Энгельс
- 3. Белки – высокомолекулярные природные соединения (биополимеры), состоящие из остатков аминокислот, которые соединены пептидной связью. Белки Протеины
- 4. В состав белковых веществ входят: углерод, водород, кислород, азот, сера, фосфор. Гемоглобин – C3032H4816O872N780S8Fe4. Молекулярная масса
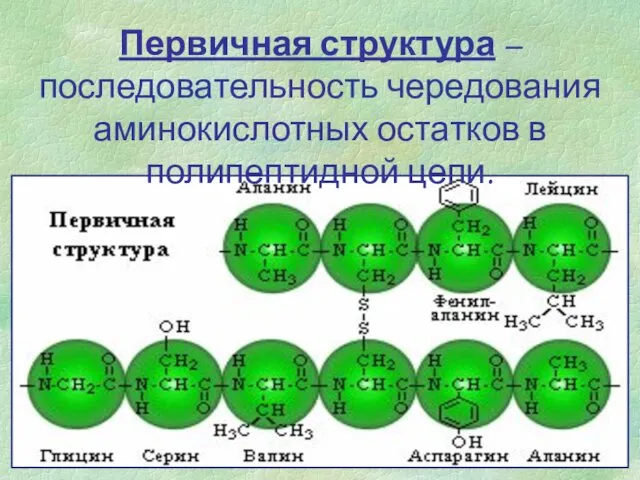
- 5. Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
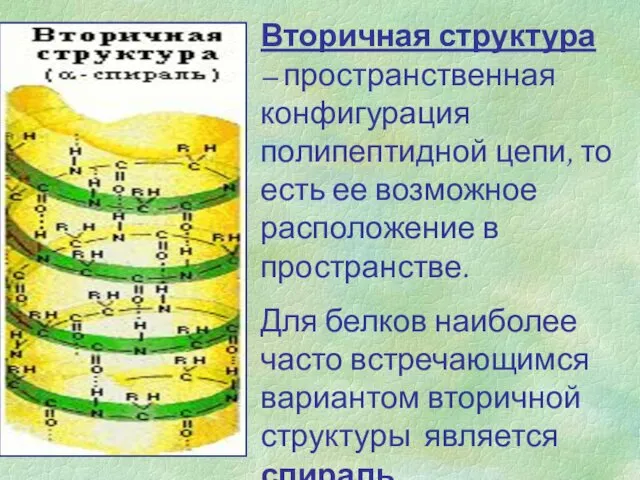
- 6. Вторичная структура – пространственная конфигурация полипептидной цепи, то есть ее возможное расположение в пространстве. Для белков
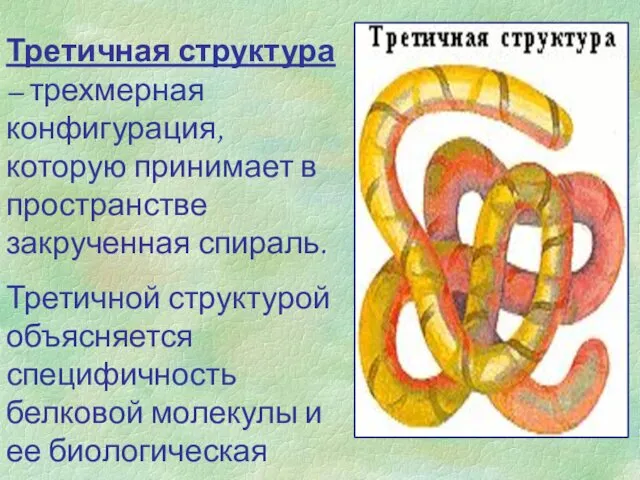
- 7. Третичная структура – трехмерная конфигурация, которую принимает в пространстве закрученная спираль. Третичной структурой объясняется специфичность белковой
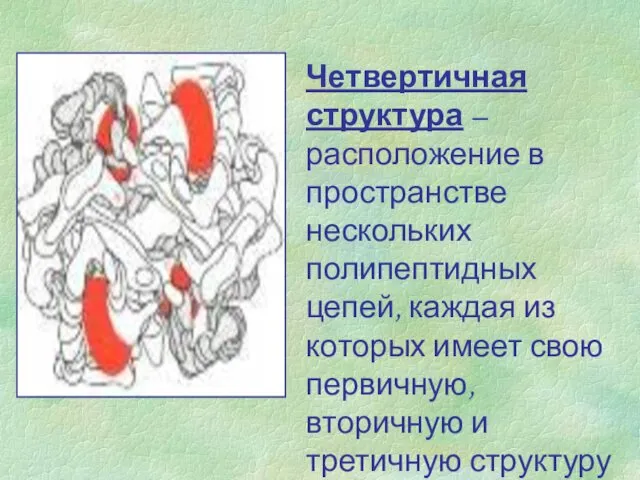
- 8. Четвертичная структура – расположение в пространстве нескольких полипептидных цепей, каждая из которых имеет свою первичную, вторичную
- 9. Функции белков Строительная (пластическая) – белки участвуют в образовании оболочки клетки, органоидов и мембран клетки. Каталитическая
- 10. Химические свойства белков 1. Гидролиз (кислотно-основный, ферментативный), в результате которого образуются аминокислоты. 2. Денатурация – нарушение
- 12. Скачать презентацию




 Количество вещества. Молярная масса. Молярный объем
Количество вещества. Молярная масса. Молярный объем Методы очистки натрия от примесей
Методы очистки натрия от примесей Газообразное состояние вещества
Газообразное состояние вещества Камни и Телец
Камни и Телец Сульфур. Характеристика елемента та утворених ним сполук, кругообіг елемента в природі
Сульфур. Характеристика елемента та утворених ним сполук, кругообіг елемента в природі Изохинолин туындыларының дәрілік заттарын талдау
Изохинолин туындыларының дәрілік заттарын талдау Растворы. Классификация, способы выражения концентрации, свойства растворов
Растворы. Классификация, способы выражения концентрации, свойства растворов Rates of reaction
Rates of reaction Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Оксиды, их классификация и свойства (8 класс)
Оксиды, их классификация и свойства (8 класс) Химическая кинетика и катализ механики. (Лекция 5)
Химическая кинетика и катализ механики. (Лекция 5) Закон сохранения массы веществ
Закон сохранения массы веществ Лекции по курсу конструкционные и биоматериалы
Лекции по курсу конструкционные и биоматериалы Природні джерела вуглеводнів і їх переробка
Природні джерела вуглеводнів і їх переробка Полимеры и ЕГЭ
Полимеры и ЕГЭ Растворы. Концентрация растворов
Растворы. Концентрация растворов Кислород. Озон. Получение кислорода
Кислород. Озон. Получение кислорода Electroanalytical Chemistry
Electroanalytical Chemistry Тест по ККЛС тема: Анализ воды очищенной и для инъекций
Тест по ККЛС тема: Анализ воды очищенной и для инъекций Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии
Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии Оксид меди
Оксид меди Основы химической термодинамики
Основы химической термодинамики Фенол. Фізичні та хімічні властивості
Фенол. Фізичні та хімічні властивості Растворы
Растворы Коррозия металлов
Коррозия металлов Чистые вещества и смеси. Растворы
Чистые вещества и смеси. Растворы Химия элементов. Комплексные соединения: типы и классификация. Методы получения и разрушения
Химия элементов. Комплексные соединения: типы и классификация. Методы получения и разрушения