Слайд 2

Фронтальна робота
1) Я кі функціональні групи входять до складу амінокислот?
2) Самостійно
виберіть із таблиці три амінокислоти та складіть формули утворених ними трипептидів.
Слайд 3

Білки
Білки (поліпептиди) — це природні високомолекулярні нітрогеновмісні органічні сполуки (біополімери), побудовані
із залишків α-амінокислот, з’єднаних пептидними зв’язками.
Слайд 4

У живих організмах амінокислотний склад білків визначається генетичним кодом, у синтезі
в більшості випадків використовуються двадцять стандартних амінокислот. Безліч їхніх комбінацій дають велику розмаїтість властивостей молекул білків.
Слайд 5

Фізичні властивості білків
Білки відрізняються за ступенем розчинності у воді, але більшість
із них у ній розчиняються. До нерозчинних належать, наприклад, кератин і фіброїн, який входить до складу шовку й павутиння. Білки також поділяються на гідрофільні й гідрофобні.
Слайд 6
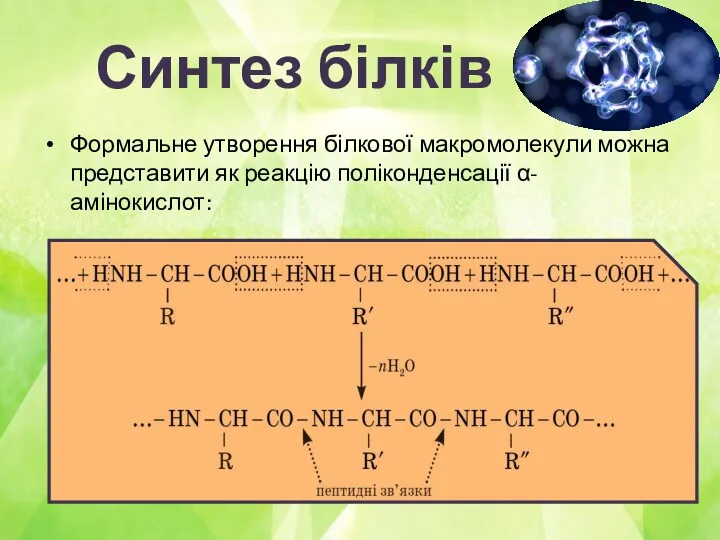
Синтез білків
Формальне утворення білкової макромолекули можна представити як реакцію поліконденсації α-амінокислот:
Слайд 7

Виділяють чотири рівні структурної організації білків.
Первинна структура — певна послідовність α-амінокислотних
залишків у поліпептидному ланцюзі.
Вторинна структура (α-спіраль) — це конформація поліпептидного ланцюга, закріплена безліччю водневих зв’язків між групами N−H і C = O. Одна з моделей вторинної структури — α-спіраль.
Слайд 8

Третинна структура — форма закрученої в просторі спіралі, утворена головним чином
за рахунок дисульфідних містків −S − S−, водневих зв’язків, гідрофобних та йонних узаємодій.
Четвертинна структура — агрегати кількох білкових макромолекул (білкові комплекси), утворені за рахунок узаємодії різних поліпептидних ланцюгів.
Слайд 9

Хімічні властивості білків
1) Гідроліз білків є гідролізом поліпептидного ланцюга з утворенням
набору амінокислот, що утворили цей поліпептидний ланцюг.
2) Денатурація — руйнування третинної та вторинної структур білкової молекули під дією нагрівання, сильних кислот, лугів, солей важких металів, спиртів, радіації.








 Алкадиены, нафтены
Алкадиены, нафтены Аминокислоты
Аминокислоты Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами
Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами Серная кислота
Серная кислота Фізичні та хімічні властивості кислот (урок хімії у 8 класі)
Фізичні та хімічні властивості кислот (урок хімії у 8 класі) Типы химических реакций , признаки и условия их протекания
Типы химических реакций , признаки и условия их протекания Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азот
Азот Хімічні властивості кислот
Хімічні властивості кислот Поширення солей у природі
Поширення солей у природі Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия ПЛАСТИК НОВЫЙ
ПЛАСТИК НОВЫЙ Stirring in liquid media
Stirring in liquid media Литий
Литий Липиды (Жиры)
Липиды (Жиры) В чём соль соли
В чём соль соли Классификация химических реакций по различным основаниям. 9 класс
Классификация химических реакций по различным основаниям. 9 класс Технологии получения полимерных нанокомпозитов
Технологии получения полимерных нанокомпозитов Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Правила роботи на уроці
Правила роботи на уроці Задачи на процентную концентрацию
Задачи на процентную концентрацию Углероды. Строение и свойства атомов
Углероды. Строение и свойства атомов Спирт µндіру технологиясы
Спирт µндіру технологиясы Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Основная. Первоначальные представления об органических веществах
Основная. Первоначальные представления об органических веществах Химические свойства серной кислоты
Химические свойства серной кислоты Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Полистирол өндірісі
Полистирол өндірісі