Содержание
- 2. Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе балқыған электролитке батырылған электродтарда электр
- 3. Электролиз кезіндегі процестер Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін электр тізбегі бар жерлерде
- 4. Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар разрядталады. Көбінесе, HI, HBr, HCl
- 5. Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі тізбек арқылы келетін электрондармен өзара
- 6. KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден кішкене артық; сондықтан NiSO4 бейтарап
- 7. Ашылу тарихы Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты. Тек сол кезде шешімі
- 8. Электролиттік процестер металдардың балқымаларының алынуы. гальваникалық қабаттардың алынуы бейорганикалық заттардың алынуы (хлор, сутегі, оттегі, сілтілер және
- 9. Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке ұмтылатын металдарды алуға болады. Ал
- 11. Скачать презентацию
Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе
Электролиз (электро... және грек. lysіs – еру, ыдырау) – еріген немесе
Электролиз кезіндегі процестер
Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін
Электролиз кезіндегі процестер
Электрондар иондармен бірінші жақты өткізгіштер екінші жақты өткізгіштермен шектесетін
Бұл жүйе энергияның химиялық көзі деп аталады, егер бұл процесстер өзімен жүреді .
Егер олардың жүруі электр энергиясының қосылуымен шартталатын болса, онда электролиз жүреді.
Электролиз кезінде электродтарда жүретін электрохимиялық процестер ең алдымен электрохимиялық жүйелерге сәйкес болатын электродтық потенциалдар қатынасына тәуелді болады.
Бірнеше мүмкін болатын процестерден минимальды энергия шығыны болатыны жүреді.
Бұл катодта ең көп электродты потенциалы болатын электрохимиялық жүйелердің тотықсызданған формаларының тотықтануы жүреді, ал анодта ең аз электродты потенциалы болатын жүйелердің тотықтанған формалары тотықсызданады.
Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар
Сулы ерітінділердің оттексіз қышқылдары және олардың тұздарының анодтағы электролизі кезінде аниондар
Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі
Егер MgCl2 балқымасы арқылы ток өткізетін болсақ, магний катиондары теріс ішкі
KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден
KOH4H=2H22O=O2H2SO4 NiSO4 ерітіндісінің никельді анодпен электролизі. Никельдің стандартты потенциалы (-0,250B) -0,41Bден
Ашылу тарихы
Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты.
Ашылу тарихы
Электрохимия ғылым ретінде ХVIII және XIX ғасырларда шет елдерде қалыптасты.
Электролиттік процестер
металдардың балқымаларының алынуы.
гальваникалық қабаттардың алынуы
бейорганикалық заттардың алынуы (хлор, сутегі, оттегі,
Электролиттік процестер
металдардың балқымаларының алынуы.
гальваникалық қабаттардың алынуы
бейорганикалық заттардың алынуы (хлор, сутегі, оттегі,
органикалық заттардың алынуы
металдардың тазартылуы (қола, күміс)
металдардың алынуы (магнии, цинк, литий, натрий, калий, алюминий
металдар беттерінің өңделуі.
электорофорез көмегімен пленкалардың жабылуы.
электродиализ және судың тұзсыздандыруы.
Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке
Электролиздің мақсатты қолданылуы: оның көмегімен таза элементтің массалық үлесі жүз процентке








 Влияние состава вещества на эффективность таяния льда и замерзания водных растворов
Влияние состава вещества на эффективность таяния льда и замерзания водных растворов Степень окисления – Условный заряд атомов химического элемента в соединении
Степень окисления – Условный заряд атомов химического элемента в соединении Основные понятия и законы химии
Основные понятия и законы химии Фазовые превращения в стали при охлаждении
Фазовые превращения в стали при охлаждении Смоги и их влияние на человека
Смоги и их влияние на человека Изомерия. Виды изомерии
Изомерия. Виды изомерии Углерод
Углерод Спирты. Определение. Классификация
Спирты. Определение. Классификация Гидролиз солей
Гидролиз солей Игра - викторина
Игра - викторина Кислородсодержащие органические вещества. Фенолы
Кислородсодержащие органические вещества. Фенолы Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Crystal defects
Crystal defects Оксиды. Классификация. Получение. Свойства
Оксиды. Классификация. Получение. Свойства Химические свойства металлов
Химические свойства металлов В чём соль соли
В чём соль соли Спирты. Классификация спиртов
Спирты. Классификация спиртов Химические свойства металлов. Коррозия металлов
Химические свойства металлов. Коррозия металлов Химические уравнения
Химические уравнения Алюминий. Сплавы алюминия
Алюминий. Сплавы алюминия Водород. Получение и свойства водорода
Водород. Получение и свойства водорода Мытье головы
Мытье головы Аналітична хімія. Лекція 1
Аналітична хімія. Лекція 1 Геохимия. Геохимическая система элементов
Геохимия. Геохимическая система элементов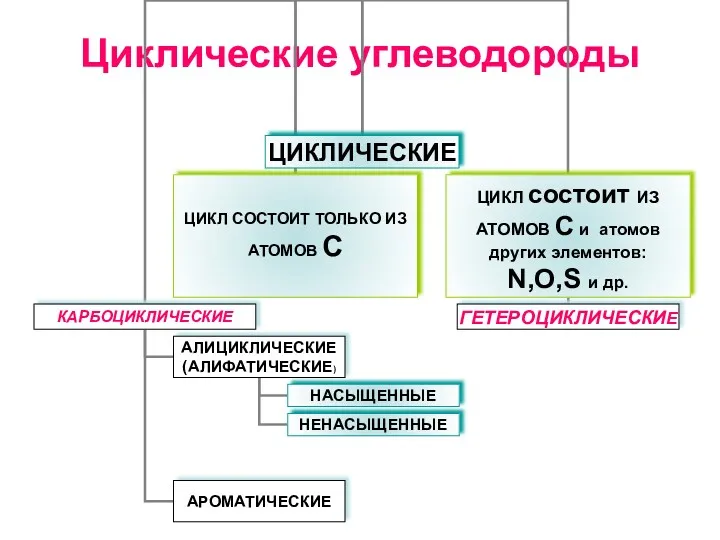 Циклические углеводороды
Циклические углеводороды Физико-химические свойства аммиака. Производство аммиака
Физико-химические свойства аммиака. Производство аммиака Окислительные свойства серной и азотной кислот
Окислительные свойства серной и азотной кислот Эмульсии. Классификация эмульсий. Механизм образования и стабилизации эмульсий. Эмульгаторы
Эмульсии. Классификация эмульсий. Механизм образования и стабилизации эмульсий. Эмульгаторы