Содержание
- 2. РАСПРОСТРАНЕНИЕ МЕТАЛЛОВ В ПРИРОДЕ
- 3. МЕТАЛЛЫ В ПРИРОДЕ. КЛАРК. Кла́рковое число́ (или кларки элементов, ещё чаще говорят просто кларк элемента) —
- 4. НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ СОЕДИНЕНИЯ МЕТАЛЛОВ В ПРИРОДЕ Из природных соединений металлов наиболее распространенными являются оксиды. Fe2O3 -
- 5. ПОЛУЧЕНИЕ МЕТАЛЛОВ
- 6. ДОБЫВАНИЕ МЕТАЛЛОВ ИЗ РУД Большинство металлов находятся в природе в виде соединений с другими элементами, в
- 7. магниетермия ПИРОМЕТАЛЛУРГИЯ Получение металлов из руд их восстановлением при высоких температурах Восстановители Углерод (кокс) Оксид углерода
- 8. ГИДРОМЕТАЛЛУРГИЯ Растворение природного соединения в виде водных растворов с помощью различных реагентов с последующим выделением металла
- 9. ЭЛЕКТРОМЕТАЛЛУРГИЯ Электрометаллургия – получение металлов из водных растворов или расплавов с помощью электрического тока (электролизом) Электролиз
- 10. ФЛОТАЦИОННЫЙ МЕТОД Флотация – метод основанный на различной смачиваемости поверхности минерала водою. Пример: руду, состоящую из
- 11. МАГНИТНЫЙ СПОСОБ Сепарация производится как в водной, так и в сухой среде. Сухая сепарация больше подходит
- 12. ПРИРОДА ХИМИЧЕСКОЙ СВЯЗИ В МЕТАЛЛАХ
- 13. ОБЩИЕ ФИЗИЧЕСКИЕ СВОЙСТВА Высокая электропроводность, высокая теплопроводность, пластичность, т.е. способность подвергаться деформации при обычных и повышенных
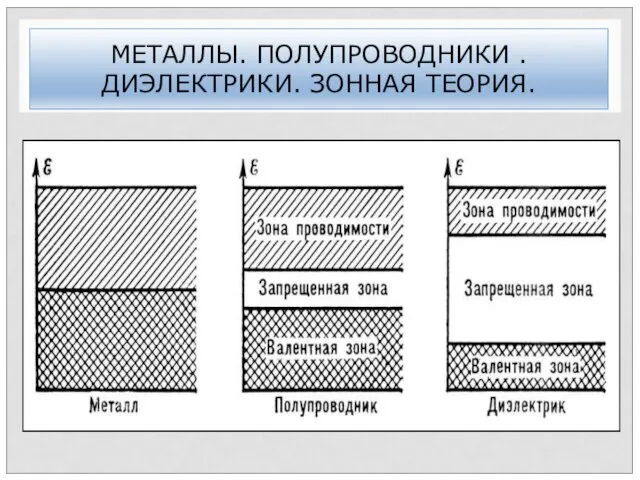
- 14. МЕТАЛЛЫ. ПОЛУПРОВОДНИКИ . ДИЭЛЕКТРИКИ. ЗОННАЯ ТЕОРИЯ.
- 15. МЕТАЛЛИЧЕСКАЯ СВЯЗЬ Способность электронов свободно передвигаться по кристаллу и переносить энергию из одной ее части в
- 16. ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
- 17. СТАНДАРТНЫЙ ВОДОРОДНЫЙ ЭЛЕКТРОД Для построения численной шкалы электродных потенциалов нужно потенциал какого-либо электродного процесса принять равным
- 18. ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЯ МЕТАЛЛОВ Потенциал водородного электрода воспроизводится с очень высокой точностью. Поэтому водородный электрод и
- 19. ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА. ЭНЕРГИЯ ИОНИЗАЦИИ Этот ряд называется электрохимическим рядом напряжения металлов. Энергия ионизации, определяется положением металла
- 20. АКТИВНОСТЬ МЕТАЛЛОВ В СООТВЕТСТВИИ С РЯДОМ НАПРЯЖЕНИЯ МЕТАЛЛОВ Пользуясь этим рядом, можно предсказать, как металл будет
- 21. АКТИВНОСТЬ МЕТАЛЛОВ В СООТВЕТСТВИИ С РЯДОМ НАПРЯЖЕНИЯ МЕТАЛЛОВ Li, K, Ba, Na, La, Mg, Lu, Be,
- 22. ОБЩИЕ ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ Химические свойства металлов определяются: строением их атомов, типом кристаллической решетки. Главное и
- 23. ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. ВЗАИМОДЕЙСТВИЕ С ПРОСТЫМИ ВЕЩЕСТВАМИ МЕТАЛЛ водород азот галогены кислород фосфор сера углерод кремний
- 24. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ
- 25. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ С ТЕРМОДИНАМИЧЕСКОЙ ТОЧКИ ЗРЕНИЯ Взаимодействие металлов с водой идет по реакции: Ме0
- 26. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ Активные металлы (металлы от начала ряда активности до Mg) с водой дают
- 27. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С КИСЛОТАМИ
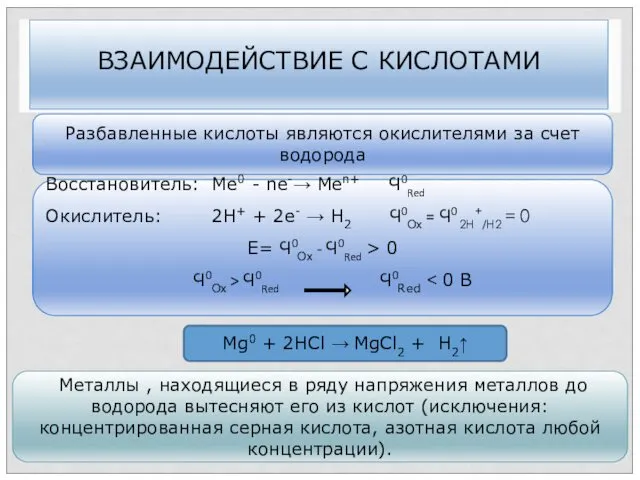
- 28. ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ Металлы , находящиеся в ряду напряжения металлов до водорода вытесняют его из кислот
- 29. ПАССИВАЦИЯ МЕТАЛЛОВ КИСЛОТАМИ Иногда образуются нерастворимые или малорастворимые продукты, которые тормозят реакцию. Например, свинец Pb не
- 30. ТАБЛИЦА РАСТВОРИМОСТИ
- 31. Концентрированная серная кислота восстанавливается до следующих продуктов H2S+6O4 (к) → S+4O2 → S0 → H2S2- ВЗАИМОДЕЙСТВИЕ
- 32. Малоактивные металлы реагируют с кислотой, восстанавливая ее до SO2 2H2S6+O4(k) + Cu0 = CuSO4 + SO2
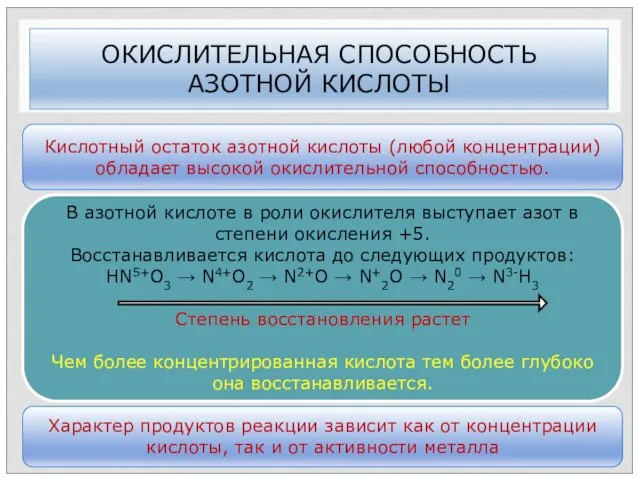
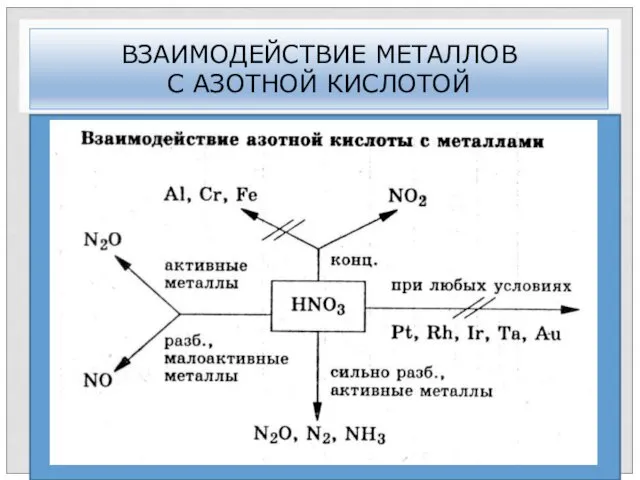
- 33. ОКИСЛИТЕЛЬНАЯ СПОСОБНОСТЬ АЗОТНОЙ КИСЛОТЫ Кислотный остаток азотной кислоты (любой концентрации) обладает высокой окислительной способностью. В азотной
- 34. ТЯЖЕЛЫЕ МЕТАЛЛЫ Известно около сорока различных определений термина тяжелые металлы, и невозможно указать на одно из
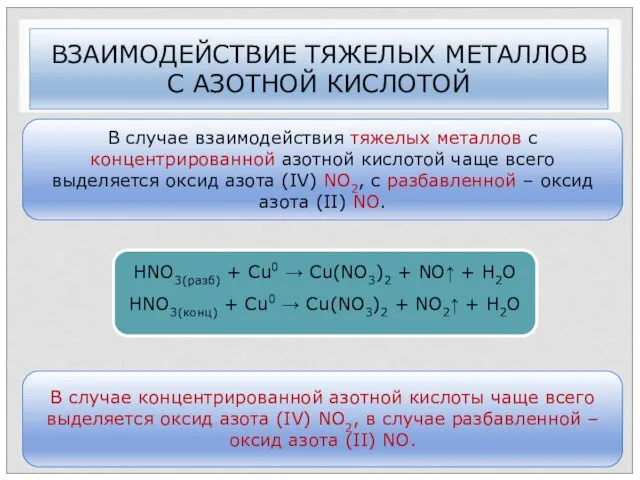
- 35. ВЗАИМОДЕЙСТВИЕ ТЯЖЕЛЫХ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ В случае взаимодействия тяжелых металлов с концентрированной азотной кислотой чаще
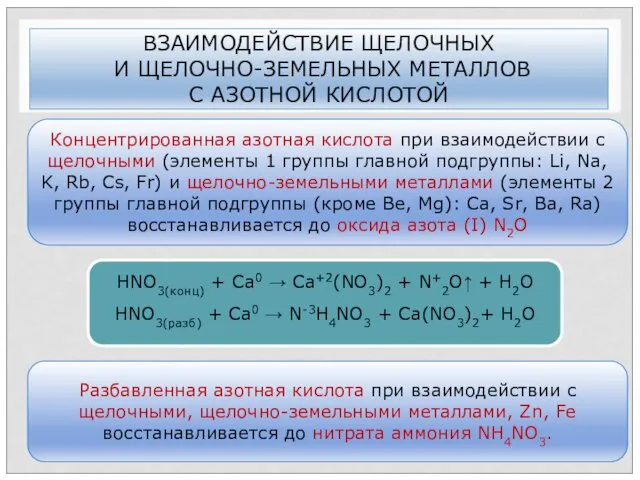
- 36. ВЗАИМОДЕЙСТВИЕ ЩЕЛОЧНЫХ И ЩЕЛОЧНО-ЗЕМЕЛЬНЫХ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ Концентрированная азотная кислота при взаимодействии с щелочными (элементы
- 37. ВЛИЯНИЕ СТЕПЕНИ ОКИСЛЕНИЯ МЕТАЛЛА. ПАССИВАЦИЯ В зависимости от химической природы металла отмечены следующие закономерности: металлы, у
- 38. ВЗАИМОДЕЙСТВИЕ СО СМЕСЯМИ КИСЛОТ Окислительная способность азотной кислоты усиливается добавлением к ней фтороводородной или хлороводородной кислот.
- 39. ВЗАИМОДЕЙСТВИЕ СО СМЕСЯМИ КИСЛОТ Au+ HN+5O3 + 4HCl → H[AuCl4] + NO ↑ + 2H2O «Царская
- 40. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДНЫМИ РАСТВОРАМИ ЩЕЛОЧЕЙ
- 41. Механизм протекания реакции (окисление идет за счет молекул воды): Zn +2 H2O = Zn(OH)2↓ + H2↑
- 42. УСТОЙЧИВОСТЬ АНИОННЫХ КОМПЛЕКСОВ Чем устойчивее комплексные анионы типа [Э(ОН)n]x-, тем легче идет реакция. Замечено, что такие
- 43. 2W + 4NaOH + 3O2 = 2Na2WO4 + 2 H2O ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВЫСОКИМИ СТЕПЕНЯМИ ОКИСЛЕНИЯ
- 44. Реакция идет по схеме: Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] 2Al + 6H2O → 2Al(OH)3
- 45. КОРРОЗИЯ МЕТАЛЛОВ
- 46. КОРРОЗИЯ МЕТАЛЛОВ. Коррозия – это самопроизвольно протекающий процесс разрушения металла в результате взаимодействия с окружающей средой.
- 47. МАТЕРИАЛЬНЫЕ ПОТЕРИ. Материальные потери при коррозии: Разрушение трубопроводов, металлических частей машин, корпусов судов, морских сооружений (более
- 48. МЕХАНИЗМ ПРОЦЕССА КОРРОЗИИ. Процесс идет с выделением энергии и рассеивания вещества (энтропия системы возрастает ∆S >
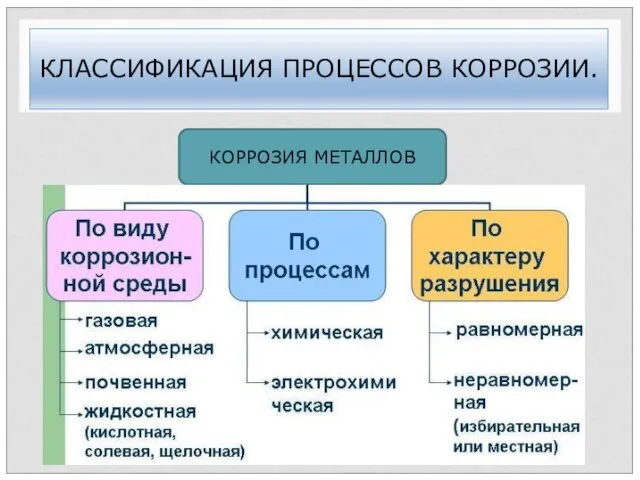
- 49. КЛАССИФИКАЦИЯ ПРОЦЕССОВ КОРРОЗИИ. КОРРОЗИЯ МЕТАЛЛОВ
- 50. ХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ
- 51. СУЩНОСТЬ ХИМИЧЕСКОЙ КОРРОЗИИ. Химическая коррозия характерна для сред, не проводящих электрический ток. Сущность процесса химической коррозии
- 52. ХИМИЧЕСКАЯ КОРРОЗИЯ В ГАЗОВОЙ СРЕДЕ Механизм такой коррозии сводится к диффузии ионов металла сквозь пленку продуктов
- 53. ПРИМЕР ХИМИЧЕСКОЙ КОРРОЗИИ В ЖИДКОЙ СРЕДЕ.
- 54. СКОРОСТЬ ОКИСЛЕНИЯ Сплошность пленки ( ) оценивается отношением объема образовавшегося оксида к объему металла, израсходованного на
- 55. Если = 1,2 – 1,6, то образующаяся оксидная пленка сплошная. Такая пленка тормозит диффузию окислителя. И
- 56. ВОРОНЕНИЕ СТАЛИ Вороне́ние стали (оксидирование, чернение (оксидирование, чернение, синение) — процесс получения на поверхности углеродистой или
- 57. ВЛИЯНИЕ СТРОЕНИЯ ОКСИДНОЙ ПЛЕНКИ НА СКОРОСТЬ КОРРОЗИИ Для металлов с переменной степенью окисления строение пленки по
- 58. КОЛИЧЕСТВЕННАЯ ОЦЕНКА СКОРОСТИ КОРРОЗИИ Количественно скорость любого вида коррозии измеряется в единицах массы потерянного металла (∆m)
- 59. АГРЕССИВНЫЕ СРЕДЫ И УСТОЙЧИВОСТЬ РАЗЛИЧНЫХ МЕТАЛЛОВ Кроме кислорода сильным агрессивным свойством обладают и другие газы. Наиболее
- 60. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ
- 61. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Электрохимическая коррозия характерна для сред, имеющих ионную проводимость, т.е. для электролитов Анодное окисление металла.
- 62. УСЛОВИЯ, СПОСОБСТВУЮЩИЕ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ Положение металла в ряду активности металлов: чем дальше расположены друг от друга,
- 63. МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ. АНОДНЫЙ ПРОЦЕСС. Механизм электрохимической коррозии определяется разностью потенциалов катодных и анодных участков и
- 64. КАТОДНЫЙ ПРОЦЕСС ДЕПОЛЯРИЗАЦИИ. Катодный процесс, чаще всего, идет с кислородной или водородной деполяризацией. Деполяризатор – это
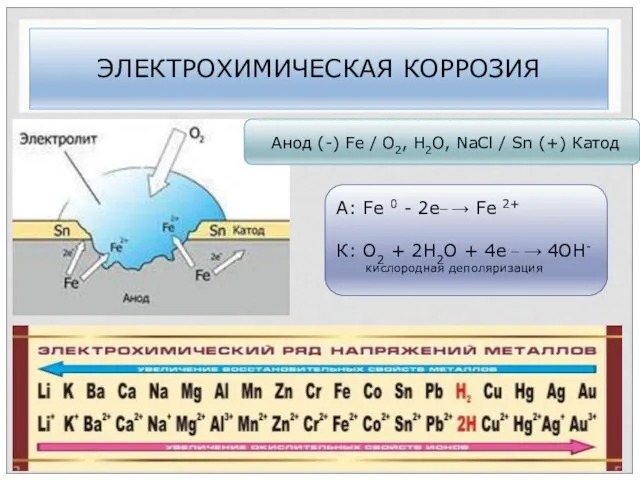
- 65. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Анод (-) Fe / О2, Н2О, NaCl / Sn (+) Катод A: Fe 0
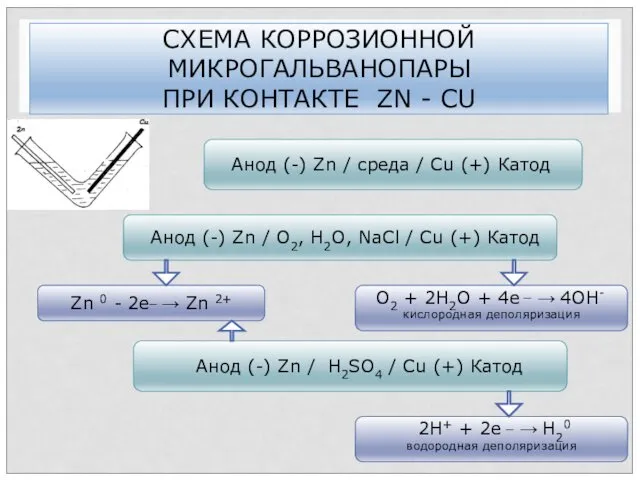
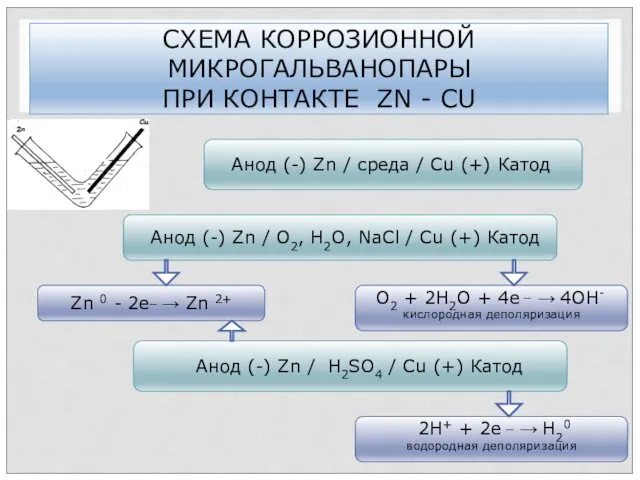
- 66. СХЕМА КОРРОЗИОННОЙ МИКРОГАЛЬВАНОПАРЫ ПРИ КОНТАКТЕ ZN - CU Анод (-) Zn / среда / Сu (+)
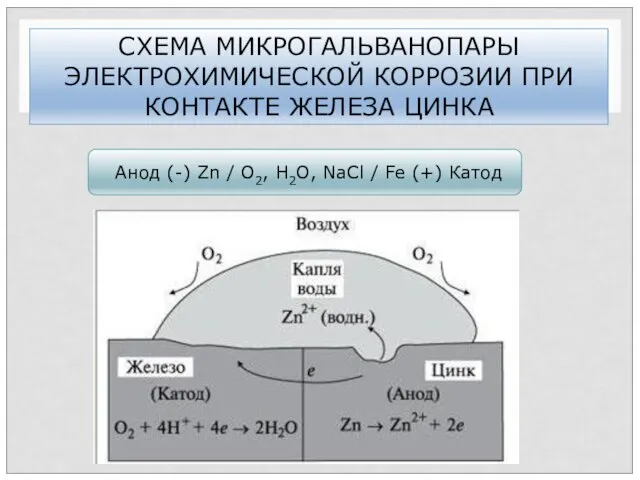
- 67. СХЕМА МИКРОГАЛЬВАНОПАРЫ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ ПРИ КОНТАКТЕ ЖЕЛЕЗА ЦИНКА Анод (-) Zn / О2, Н2О, NaCl /
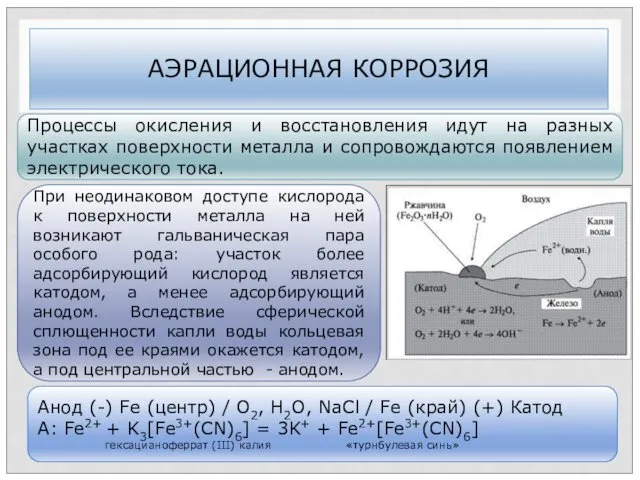
- 68. АЭРАЦИОННАЯ КОРРОЗИЯ Процессы окисления и восстановления идут на разных участках поверхности металла и сопровождаются появлением электрического
- 69. ПАССИВАЦИЯ МЕТАЛЛОВ ПРИ КОРРОЗИЯ Иногда скорость коррозии может лимитироваться анодным процессом. Это характерно для металлов, способных
- 70. УСЛОВИЯ ПРОТЕКАНИЯ КОРРОЗИИ С КИСЛОРОДНОЙ И ВОДОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ ∆G = -nFE Е= Ϥ0Ох - Ϥ0Red >
- 71. УСЛОВИЯ ПРОТЕКАНИЯ КОРРОЗИИ С КИСЛОРОДНОЙ И ВОДОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ Если E0Me+n/Me0 Если E0Me+n/Me0 меньше потенциала кислородного электрода,
- 72. УСЛОВИЯ ПРОТЕКАНИЯ КОРРОЗИИ С КИСЛОРОДНОЙ И ВОДОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ Если E0Me+n/Me0 > E0О2/ОН- потенциала кислородного электрода (область
- 73. МЕТОДЫ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ
- 74. МЕТОДЫ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ Все методы защиты условно делятся на следующие группы: Легирование металлов; Защитные
- 75. ЛЕГИРОВАНИЕ МЕТАЛЛОВ Это метод защиты, связанный с изменением свойств корродирующего металла. Эффективный, хотя обычно дорогой метод
- 76. ЗАЩИТНЫЕ ПОКРЫТИЯ. МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ Защитные покрытия - это слои, искусственно создаваемые на поверхности металла для предохранения
- 77. КАТОДНЫЕ МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ К катодным покрытиям относятся покрытия, электродные потенциалы которых в данной среде имеют более
- 78. АНОДНЫЕ МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ Анодные покрытия имеют более отрицательный потенциал, чем потенциал основного металла. Например: покрытие стали
- 79. СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛИЧЕСКИХ ЗАЩИТНЫХ ПОКРЫТИЙ Электрохимический (гальванические покрытия). Металлизация (Погружение в расплавленный металл). Термодиффузионный способ (для
- 80. НЕМЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ В качестве таких покрытий могут быть: неорганические эмали, лакокрасочные покрытия, покрытия смолами, пластмассами, полимернами
- 81. ЭЛЕКТРОХИМИЧЕСКАЯ ЗАЩИТА. ПРОТЕКТОРЫ Катодная защита – изделие подключается к (-) внешнего источника тока, оно становится катодом,
- 82. ИЗМЕНЕНИЕ СВОЙСТВ КОРРОЗИОННОЙ СРЕДЫ С целью снижения коррозионной активности среды проводят ее обработку. Например: удаление кислорода
- 83. ИНГИБИТОРЫ Наиболее четко ингибирующее действие выражено у следующих типов соединений: амины, азотосодержащие гетероциклические соединения, сульфиды, альдегиды,
- 84. МЕХАНИЗМ ДЕЙСТВИЯ ИНГИБИТОРОВ Анодные ингибиторы– окислители (NO2-, NO3-, CrO42-, PO43-). Металл при этом переходит в устойчивое
- 85. ВЫВОДЫ ПО ТЕМЕ: ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛА
- 86. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С КИСЛОТАМИ
- 87. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
- 88. СХЕМА КОРРОЗИОННОЙ МИКРОГАЛЬВАНОПАРЫ ПРИ КОНТАКТЕ ZN - CU Анод (-) Zn / среда / Сu (+)
- 90. Скачать презентацию






























![ВЗАИМОДЕЙСТВИЕ СО СМЕСЯМИ КИСЛОТ Au+ HN+5O3 + 4HCl → H[AuCl4]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/102299/slide-38.jpg)


![УСТОЙЧИВОСТЬ АНИОННЫХ КОМПЛЕКСОВ Чем устойчивее комплексные анионы типа [Э(ОН)n]x-, тем](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/102299/slide-41.jpg)





































 Химические свойства металлов
Химические свойства металлов Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? d-элементы
d-элементы Подготовка к ВПР по химии. 11 класс
Подготовка к ВПР по химии. 11 класс Метаболизм кетоновых тел. Метаболизм холестерина
Метаболизм кетоновых тел. Метаболизм холестерина Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия Кислотные дожди
Кислотные дожди The Molecules of Life
The Molecules of Life Цинк и его соединения
Цинк и его соединения Фосфор и его соединения
Фосфор и его соединения Химия воды
Химия воды Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Классификация химических элементов
Классификация химических элементов Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Гониометрическое исследование кристаллов
Гониометрическое исследование кристаллов Сплавы железа с углеродом: стали и чугуны
Сплавы железа с углеродом: стали и чугуны Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування
Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування Мінерали та гірські породи
Мінерали та гірські породи Серная кислота
Серная кислота Electrolysis
Electrolysis Вещества
Вещества Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Аминокислоты 2
Аминокислоты 2 Метаболизм углеводов
Метаболизм углеводов Спектральные методы: атомная спектроскопия
Спектральные методы: атомная спектроскопия Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості