Содержание
- 2. Введение Химическая связь – силы, обуславливающие устойчивое существование двух и многоатомных соединений. В результате образования химической
- 3. Основные виды связей Химическая связь Ионная Ковалентная Металлическая Межмолекулярные взаимодействия: водородная связь ван-дер-ваальсовы силы * Основы
- 4. Правило октета В результате образования химической связи атомы приобретают такую же электронную конфигурацию, как у благородных
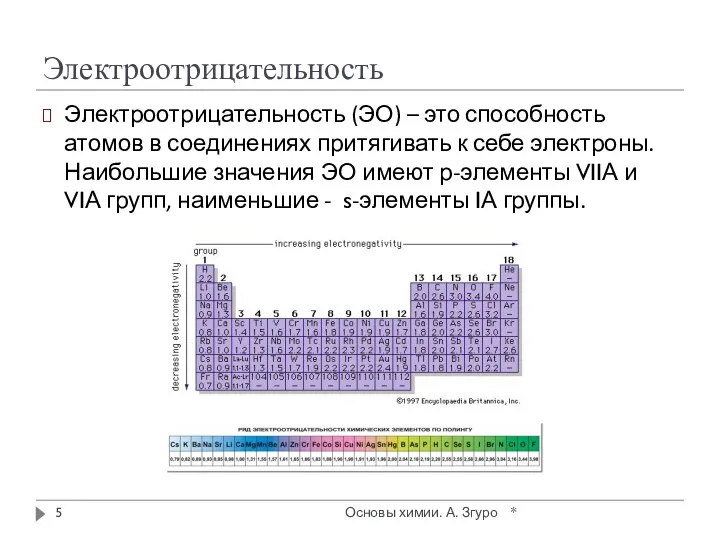
- 5. Электроотрицательность Электроотрицательность (ЭО) – это способность атомов в соединениях притягивать к себе электроны. Наибольшие значения ЭО
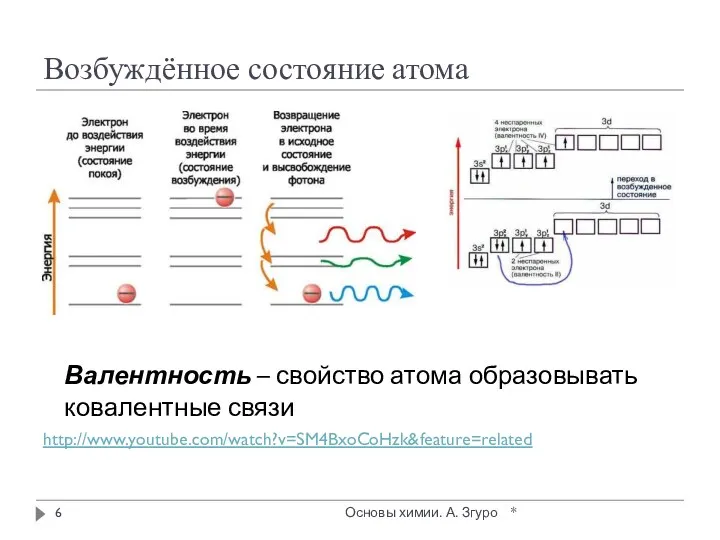
- 6. Возбуждённое состояние атома Валентность – свойство атома образовывать ковалентные связи http://www.youtube.com/watch?v=SM4BxoCoHzk&feature=related * Основы химии. А. Згуро
- 7. Ионная химическая связь Это химическая связь, возникающая в результате электростатического взаимодействия положительно и отрицательно заряженных ионов
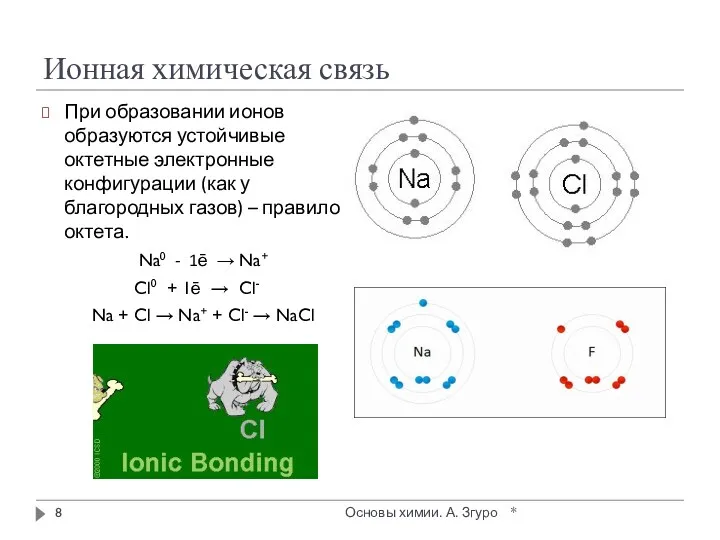
- 8. Ионная химическая связь При образовании ионов образуются устойчивые октетные электронные конфигурации (как у благородных газов) –
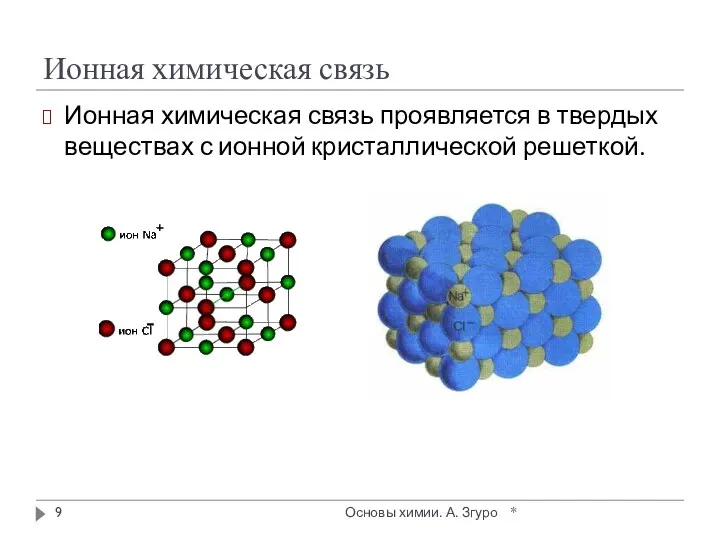
- 9. Ионная химическая связь Ионная химическая связь проявляется в твердых веществах с ионной кристаллической решеткой. * Основы
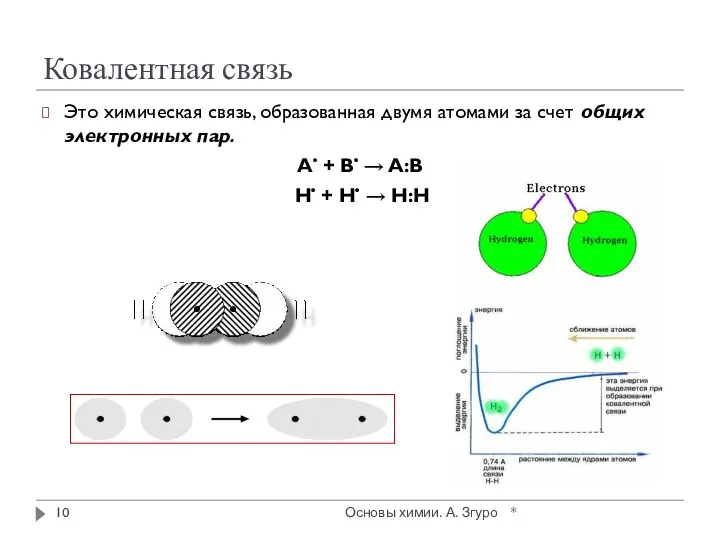
- 10. Ковалентная связь Это химическая связь, образованная двумя атомами за счет общих электронных пар. A• + B•
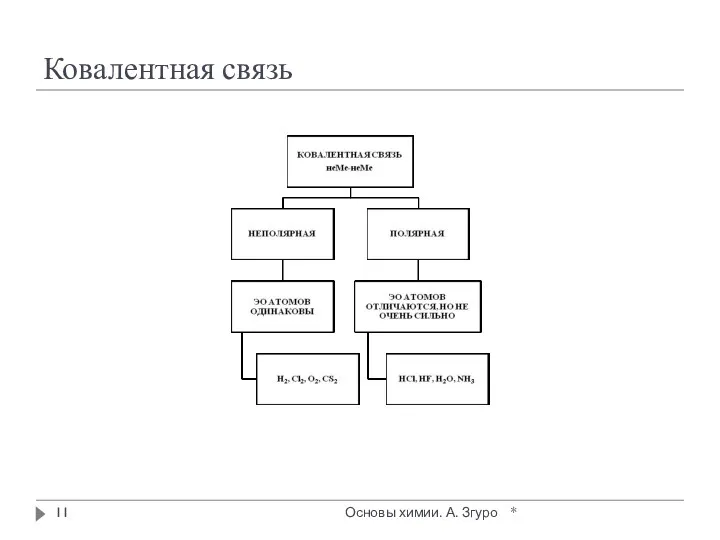
- 11. Ковалентная связь * Основы химии. А. Згуро
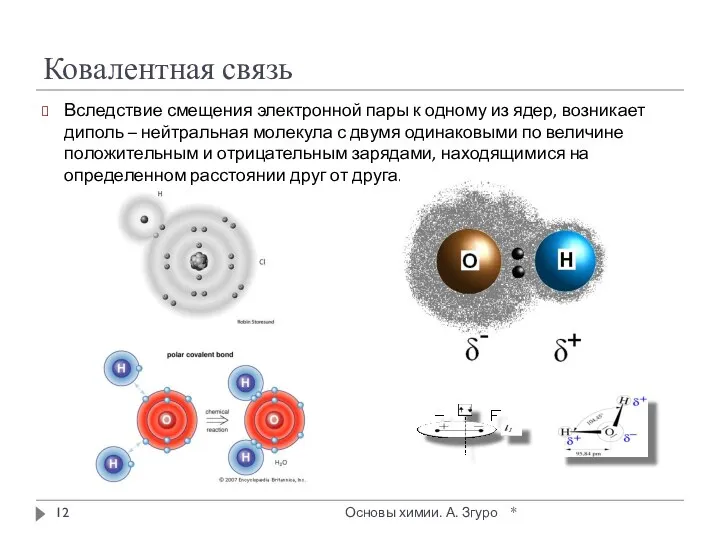
- 12. Ковалентная связь Вследствие смещения электронной пары к одному из ядер, возникает диполь – нейтральная молекула с
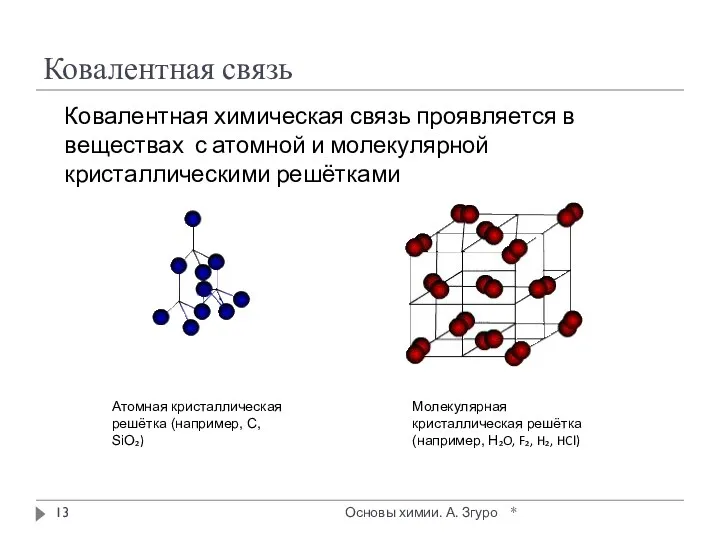
- 13. Ковалентная связь Ковалентная химическая связь проявляется в веществах с атомной и молекулярной кристаллическими решётками * Основы
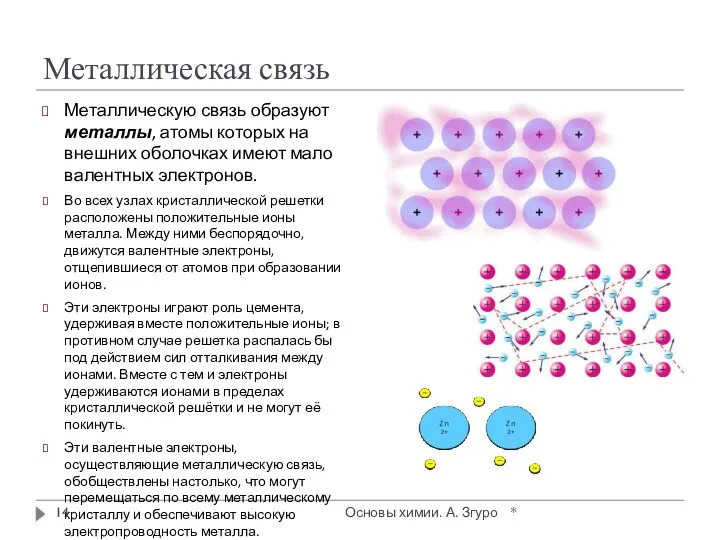
- 14. Металлическая связь Металлическую связь образуют металлы, атомы которых на внешних оболочках имеют мало валентных электронов. Во
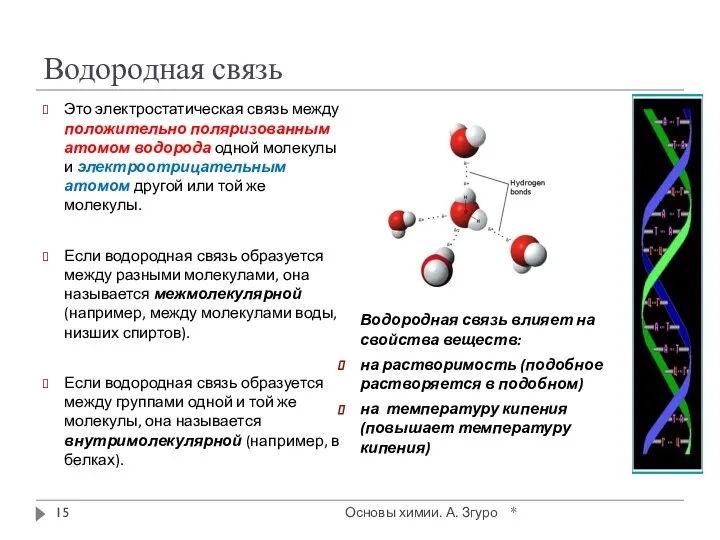
- 15. Водородная связь Это электростатическая связь между положительно поляризованным атомом водорода одной молекулы и электроотрицательным атомом другой
- 16. Водородная связь Чем полярнее связь в водородном соединении, тем прочнее возникающая водородная связь H∙∙∙F энергия связи
- 17. Характеристики связи Длина связи Энергия связи Направленность связи Полярность связи * Основы химии. А. Згуро
- 18. Длина связи Это расстояние между ядрами атомов в соединении * Основы химии. А. Згуро
- 19. Энергия связи Это количество энергии, которое выделяется при образовании химической связи, кДж/моль. Столько же энергии нужно
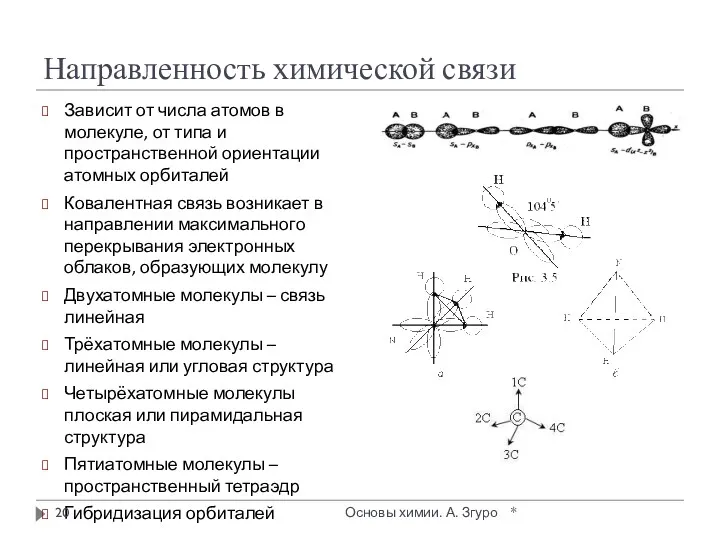
- 20. Направленность химической связи Зависит от числа атомов в молекуле, от типа и пространственной ориентации атомных орбиталей
- 21. Полярность химической связи Полярность связи определяется тем, какова электроотрицательность атомов, образующих связь Полярность связи характеризуется величиной
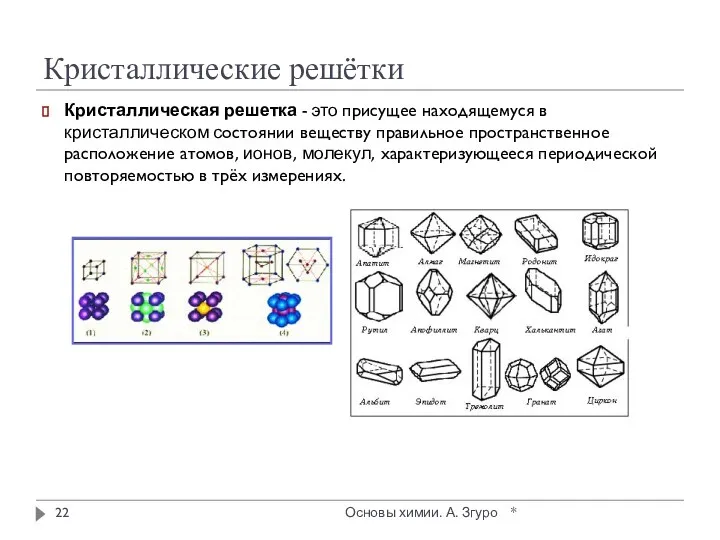
- 22. Кристаллические решётки Кристаллическая решетка - это присущее находящемуся в кристаллическом состоянии веществу правильное пространственное расположение атомов,
- 23. Ионная кристаллическая решётка Обычно ионные кристаллы твердые, но хрупкие. Ионные кристаллы отличаются высокими температурами плавления. В
- 24. Атомная кристаллическая решётка Атомные кристаллы состоят из отдельных атомов, объединенных ковалентными связями (алмаз, графит). Нередко соединения
- 25. Молекулярная кристаллическая решётка Молекулярные кристаллы построены из отдельных молекул, внутри которых атомы соединены ковалентными связями. Между
- 26. Металлическая кристаллическая решётка Характерна для металлов. В ней имеется металлическая связь между атомами. В металлических кристаллах
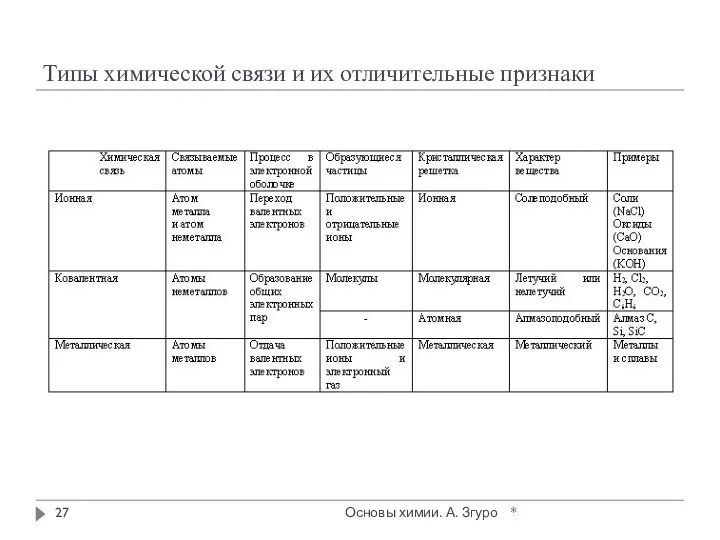
- 27. Типы химической связи и их отличительные признаки * Основы химии. А. Згуро
- 29. Скачать презентацию













 Общая характеристика неметаллов
Общая характеристика неметаллов Химическая кинетика. Основные закономерности протекания химических реакций (лекция 5)
Химическая кинетика. Основные закономерности протекания химических реакций (лекция 5) Теория электролитической диссоциации
Теория электролитической диссоциации Группа веществ, изолируемых полярными растворителями
Группа веществ, изолируемых полярными растворителями Химиялық элементтердің тірі және өлі табиғатта таралуы
Химиялық элементтердің тірі және өлі табиғатта таралуы Особенности органических веществ. 9 класс
Особенности органических веществ. 9 класс Тұндыру әдістері
Тұндыру әдістері ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации
ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Химияны оқыту әдістері
Химияны оқыту әдістері Нефть и способы её переработки
Нефть и способы её переработки Элементы группы галогенов
Элементы группы галогенов Теория сильных и слабых электролитов
Теория сильных и слабых электролитов Витамины. Ашылу тарихы
Витамины. Ашылу тарихы Хімічні елементи, їхні назви і символи. Поширеність хімічних елементів у природі
Хімічні елементи, їхні назви і символи. Поширеність хімічних елементів у природі Ion exchange
Ion exchange Синтетические органические вещества
Синтетические органические вещества Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Простые вещества - неметаллы. 8 класс
Простые вещества - неметаллы. 8 класс Сложные эфиры. Жиры
Сложные эфиры. Жиры Периодический закон химических элементов Д. И. Менделеева и периодическая система
Периодический закон химических элементов Д. И. Менделеева и периодическая система Алюминий и его соединения
Алюминий и его соединения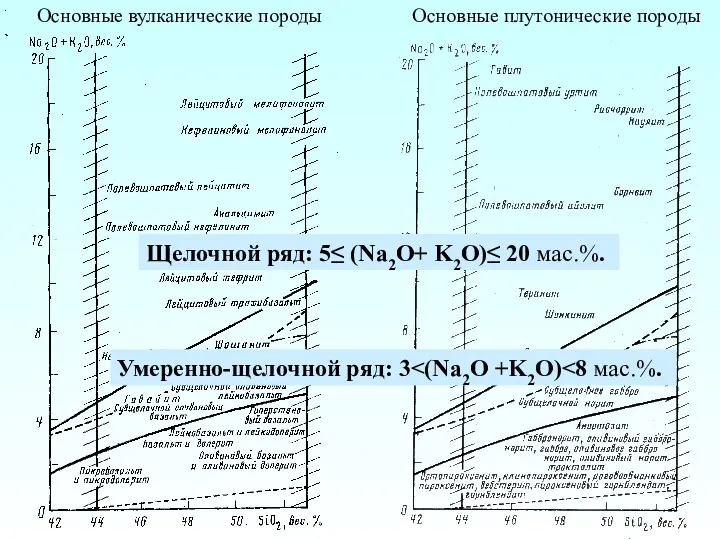 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Газоподібна і тверда фаза грунту. Методи аналізу зернового складу
Газоподібна і тверда фаза грунту. Методи аналізу зернового складу Аммиак. Образование молекулы аммиака
Аммиак. Образование молекулы аммиака Кислоты и их свойства
Кислоты и их свойства Сложные эфиры
Сложные эфиры Використання натуральних та штучних добавок при виготовленні харчових продукцій
Використання натуральних та штучних добавок при виготовленні харчових продукцій