Содержание
- 2. Запас энергии системы характеризует количество внутренней энергии . Эту находящуюся в скрытом виде энергию обозначают символом
- 3. При любом процессе соблюдается закон сохранения энергии: теплота, поглощенная системой, идет на изменении ее внутренней энергии
- 4. При химических процессах А – работа против внешнего давления, т.е.: A = p · ∆V, где
- 5. Энтальпия показывает теплосодержание системы. По знаку энтальпия противоположна тепловому эффекту реакции. Тепловой эффект показывает сколько теплоты
- 6. Первый закон термодинамики Первый закон термодинамики - это одно из выражений закона сохранения энергии: энергия не
- 7. Энтальпия разложения химического соединения равна, но противоположна по знаку энтальпии его образования из тех же продуктов
- 8. При расчетах энтальпии реакций особое значение имеет энтальпия образования соединения. Энтальпией образования соединения называется изменение энтальпии
- 9. CaO(к) → Ca(к)+ ½ O2,(r), ΔH◦обр.(CaO)= +635.1 кДж/моль SiO2(к) → Si(к) + O2, ΔН ◦обр (SiO2)=
- 10. Из этого расчета видно, что энтальпия реакции равна разности суммы энтальпии образования продуктов и исходных веществ
- 11. Энтропия и её изменение в химическом процессе. Энергия Гиббса Большинство реакций при обычных условиях проходит с
- 12. , С(к) + Н2О(к)= СО( r )+ H 2 ( r ) Степень порядка 2 Самопроизвольный
- 13. Самопроизвольный процесс, проходящий без изменения энергетического состояния системы, совершается в направлении, при котором система переходит в
- 14. Если в самопроизвольном процессе степень беспорядка не изменяется, ΔS = 0, то направление процесса определяется изменением
- 15. В химических процессах одновременно действуют две силы: стремление частиц объединиться за счёт прочных связей, что уменьшает
- 16. ΔG = ΔН – TΔS ΔG = ΔGр-ии = ∑ νΔGnpoд -∑ νΔGисх-х в-в ΔН =
- 17. В самопроизвольной реакции всегда изменение изобарного потенциала отрицательно: ΔG Состояние, при котором ΔG=0, характеризуется тем, что
- 18. При стандартных условиях при равновесии концентрации всех веществ равны по 1 моль/л, а парциальные давления по
- 19. Процессы, которые происходят в природе или которые мы используем в промышленности, можно объединить в две большие
- 21. Скачать презентацию


















 Разнообразие неметаллов
Разнообразие неметаллов Подгруппа углерода
Подгруппа углерода Метод МО
Метод МО Химия и производство
Химия и производство Реакции подлинности лекарственных веществ
Реакции подлинности лекарственных веществ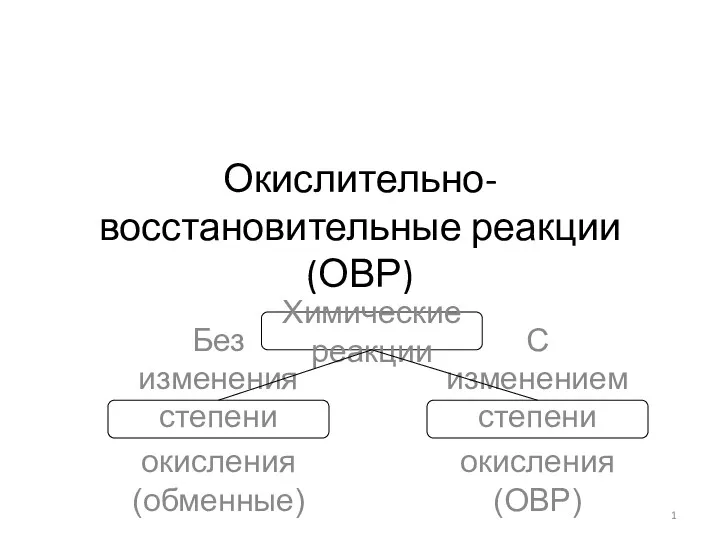 Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс
Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс Производство аммиака и азотной кислоты
Производство аммиака и азотной кислоты Кремний и его соединения
Кремний и его соединения Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Химическая кинетика и катализ
Химическая кинетика и катализ Происхождение химических элементов
Происхождение химических элементов Кинетика химических реакций. Химическое равновесие. (Лекция 5)
Кинетика химических реакций. Химическое равновесие. (Лекция 5) Липиды. Составные части липидов
Липиды. Составные части липидов Chemical Equilibrium. Topic 3.3
Chemical Equilibrium. Topic 3.3 Дефекты в твердых телах
Дефекты в твердых телах Побочная подгруппа 1 и 2. Медь
Побочная подгруппа 1 и 2. Медь Закономерности процессов нитрования НЦ
Закономерности процессов нитрования НЦ Экстракция. Понятия в экстракции
Экстракция. Понятия в экстракции Циклоалканы
Циклоалканы Пиролиз нефтяного сырья
Пиролиз нефтяного сырья Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері
Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Поверхностные явления. Адсорбция
Поверхностные явления. Адсорбция АЛЮМИНИЙ
АЛЮМИНИЙ