Слайд 2

Химический знак –
Порядковый номер –
Относительная атомная масса Ar (Н)
=
Химическая формула –
Относительная молекулярная масса Mr (Н) =
Валентность - .
Слайд 3
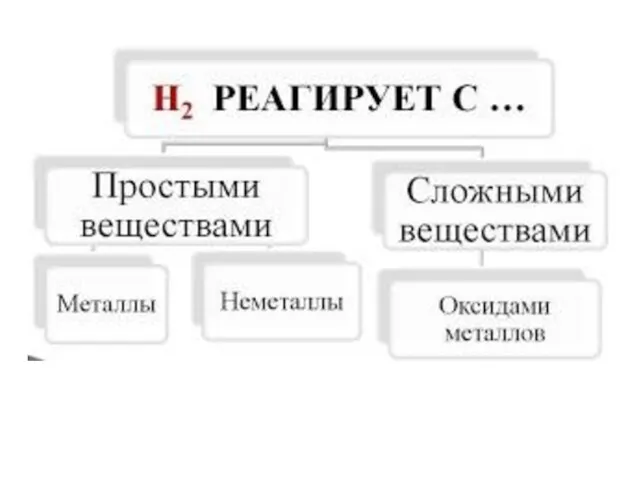
Слайд 4
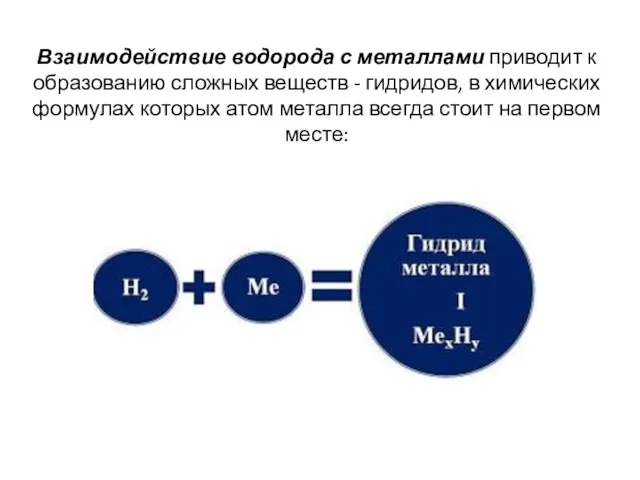
Взаимодействие водорода с металлами приводит к образованию сложных веществ - гидридов, в
химических формулах которых атом металла всегда стоит на первом месте:
Слайд 5

Н2 + 2Li = 2LiH
Гидриды металлов легко разлагаются водой с образованием соответствующей
щелочи и водорода:
СаH2 + 2Н2О = Са(ОН)2 + 2Н2↑
Слайд 6
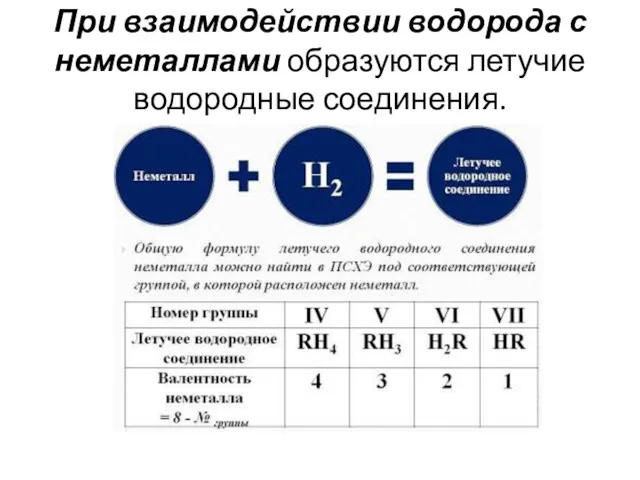
При взаимодействии водорода с неметаллами образуются летучие водородные соединения.
Слайд 7

1). С кислородом Водород образует воду:
2Н2 + О2 = 2Н2О + Q
(смесь 2 объемов Н2 и 1
объема О2 называется гремучим газом).
2). С галогенами Водород образует галогеноводороды, например:
Н2 + Cl2 = 2НСl
3). С азотом Водород взаимодействует с образованием аммиака:
ЗН2 + N2 = 2NН3
4). При нагревании Водород энергично реагирует с серой:
Н2 + S = H2S (сероводород),
5). С чистым углеродом Водород может реагировать без катализатора только при высоких температуpax:
2Н2 + С (аморфный) = СН4 (метан)






 Максимально очищенные фитопрепараты. Технология и стандартизация
Максимально очищенные фитопрепараты. Технология и стандартизация Лекарственные средства, производные пиридина и пиперазина
Лекарственные средства, производные пиридина и пиперазина Растворы. Классификация, способы выражения концентрации, свойства растворов
Растворы. Классификация, способы выражения концентрации, свойства растворов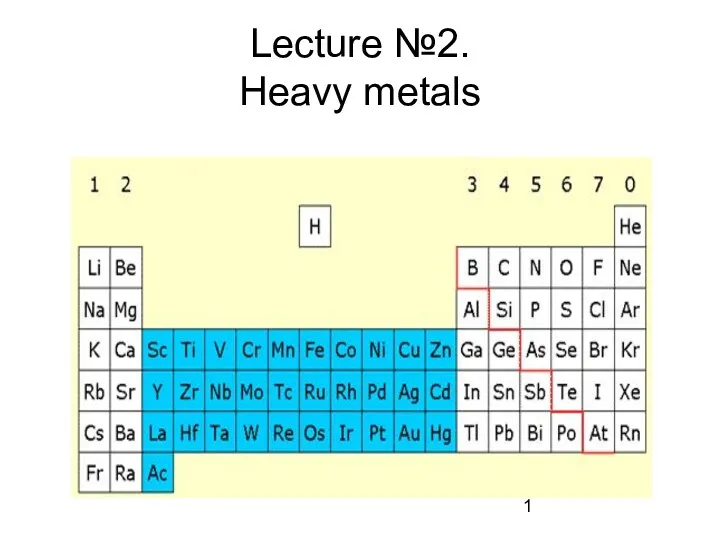 Heavy metals
Heavy metals Химические методы выявления потожировых следов
Химические методы выявления потожировых следов Искусственные и трансурановые элементы
Искусственные и трансурановые элементы Карбонові кислоти
Карбонові кислоти Перманганат калия
Перманганат калия АЛКАНЫ Строение молекулы метана.
АЛКАНЫ Строение молекулы метана. Вещественный состав магматических горных пород и петрохимические пересчеты
Вещественный состав магматических горных пород и петрохимические пересчеты Химические свойства основных классов неорганических соединений
Химические свойства основных классов неорганических соединений Периодический закон Менделеева
Периодический закон Менделеева Кислород
Кислород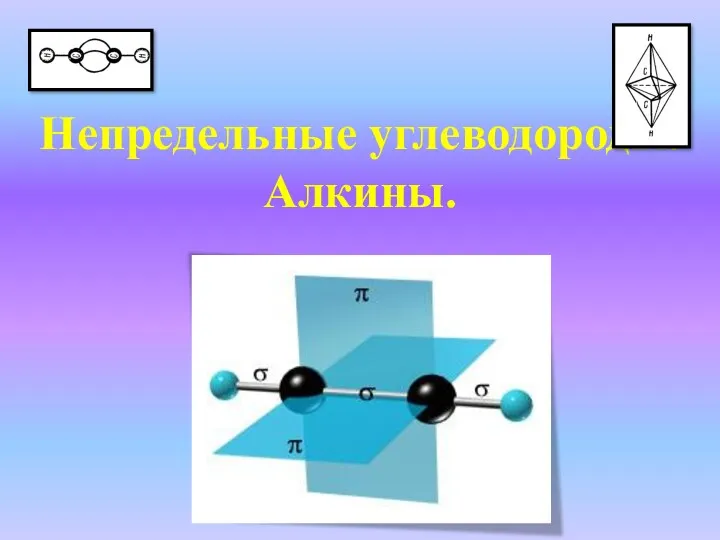 Непредельные углеводороды. Алкины
Непредельные углеводороды. Алкины Аллотропия
Аллотропия Химическая промышленность России входит в авангардную тройку
Химическая промышленность России входит в авангардную тройку Вещества и физические тела
Вещества и физические тела Химическая технология природных энергоносителей и углеродных материалов
Химическая технология природных энергоносителей и углеродных материалов Алканы.Определение. Общая формула класса углеводородов
Алканы.Определение. Общая формула класса углеводородов Уникальная соль (для дошколников)
Уникальная соль (для дошколников)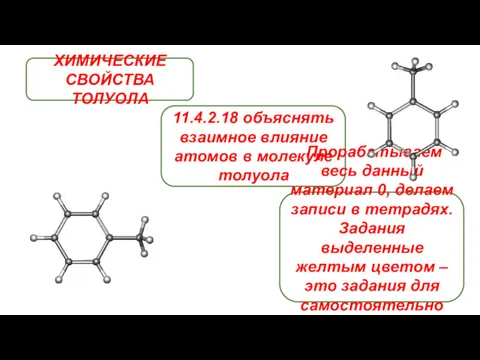 Химические свойства толуола
Химические свойства толуола Окислительно-восстановительные реакции. Основные положения электронной теории ОВР
Окислительно-восстановительные реакции. Основные положения электронной теории ОВР Перегонка с водяным паром
Перегонка с водяным паром Вода
Вода Припекание взаимно растворимых твердых тел
Припекание взаимно растворимых твердых тел 5.Алкины
5.Алкины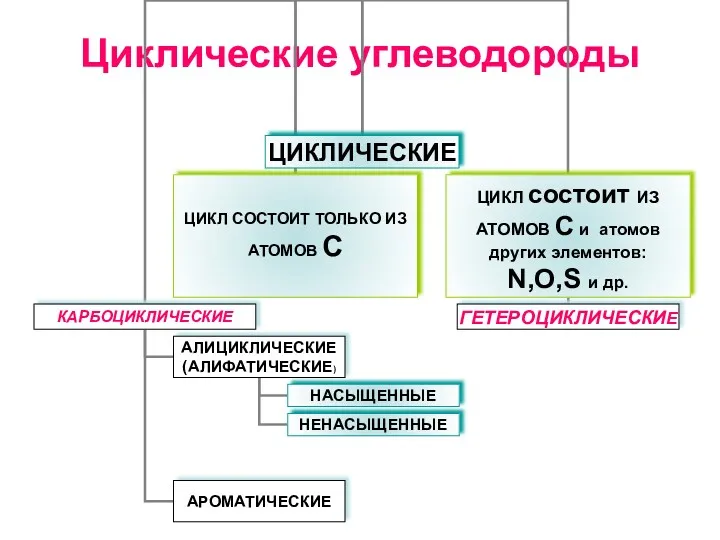 Циклические углеводороды
Циклические углеводороды Химический элемент водород
Химический элемент водород