Содержание
- 2. Ребенок – не кувшин, который надо наполнить, а лампада, которую надо зажечь Средневековые гуманисты
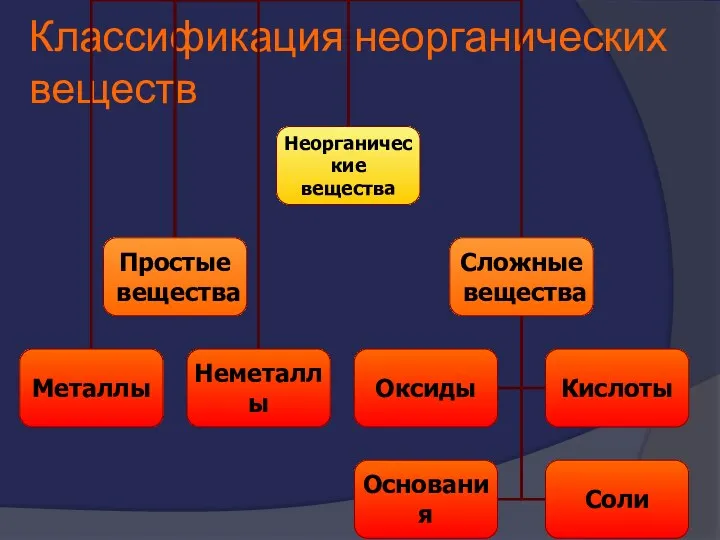
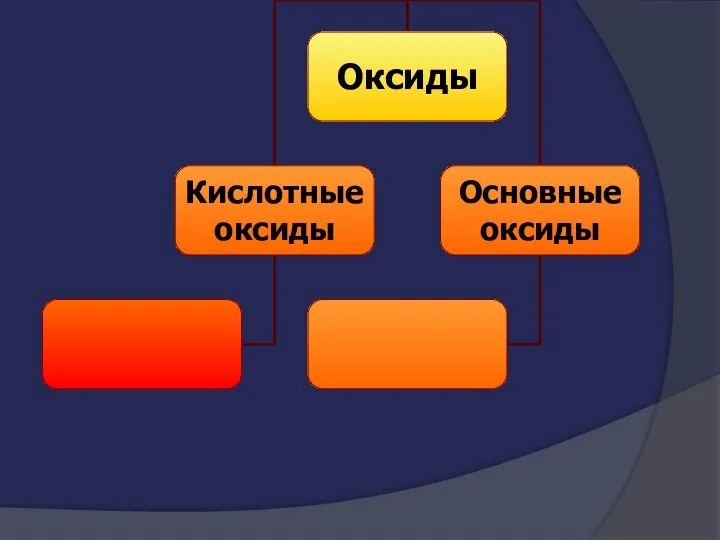
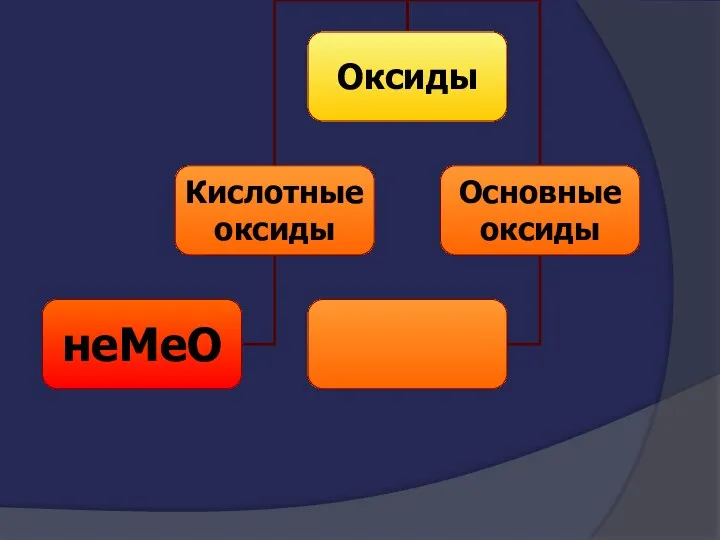
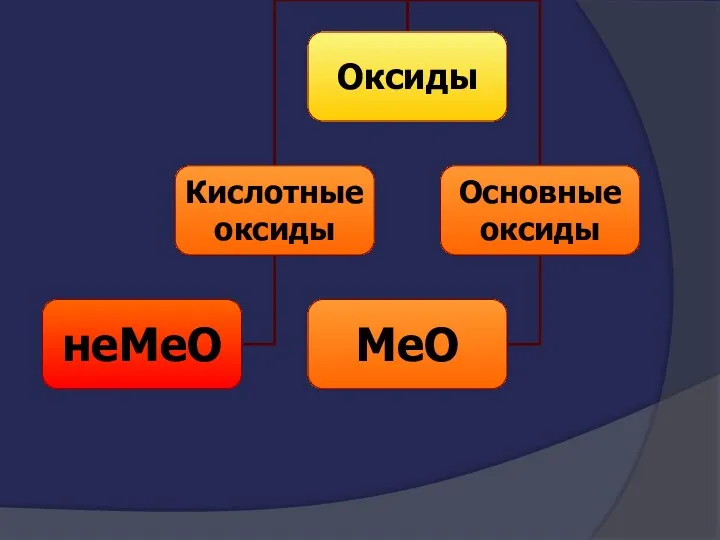
- 3. Классификация неорганических веществ
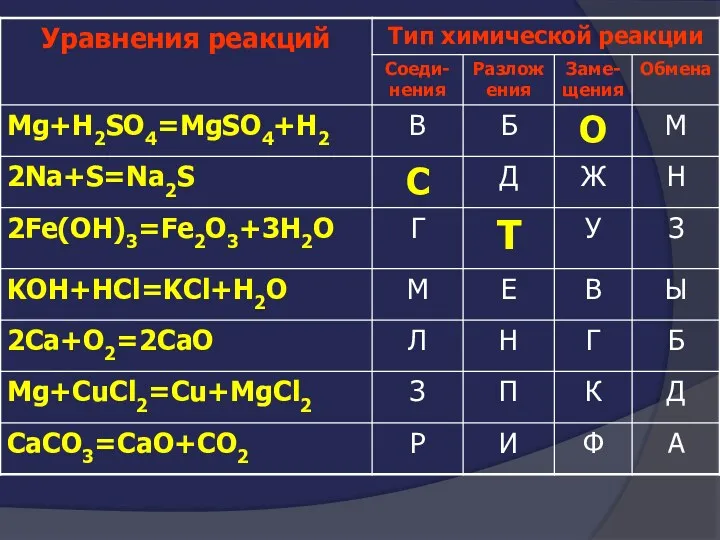
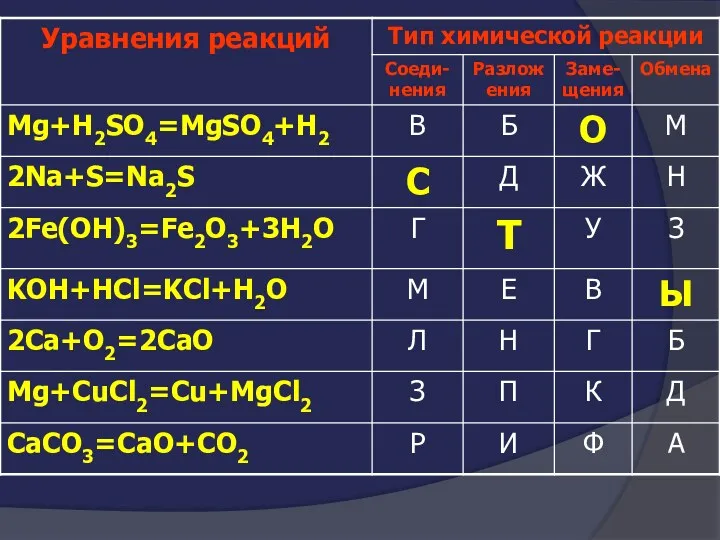
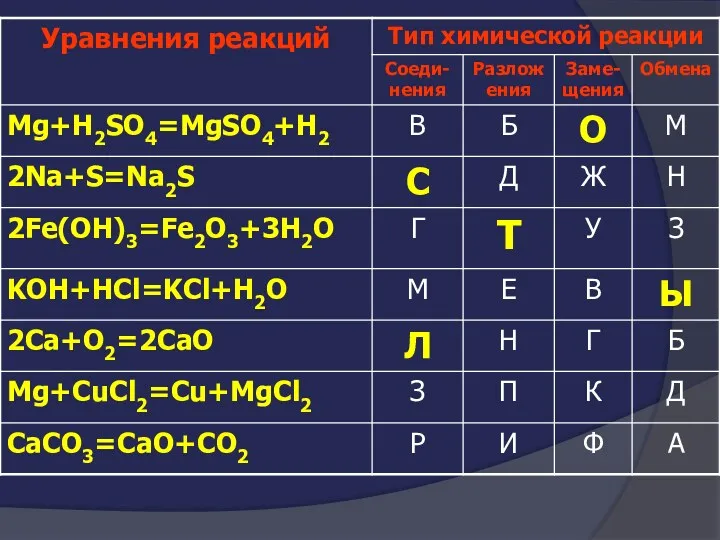
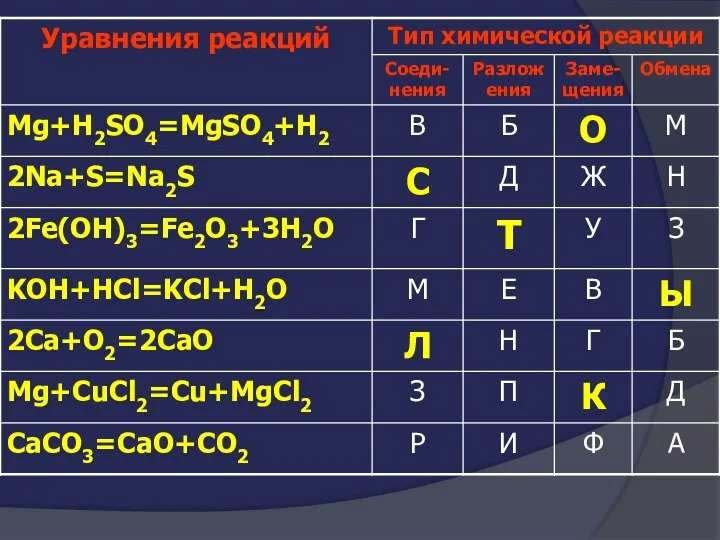
- 12. О С Т Ы Л К И
- 13. Тема урока: КИСЛОТЫ
- 14. Задачи урока: Знать определение, состав, классификацию, номенклатуру кислот Уметь определять кислоты среди других веществ, классифицировать кислоты,
- 15. КИСЛОТЫ В КУЛИНАРИИ Уксусная и лимонная кислоты.
- 16. КИСЛОТЫ В МЕДИЦИНЕ Аскорбиновая, ацетилсалициловая и другие
- 17. Соляная кислота, находящаяся в желудке, помогает переваривать пищу. Молочная кислота образуется в мышцах при физической нагрузке.
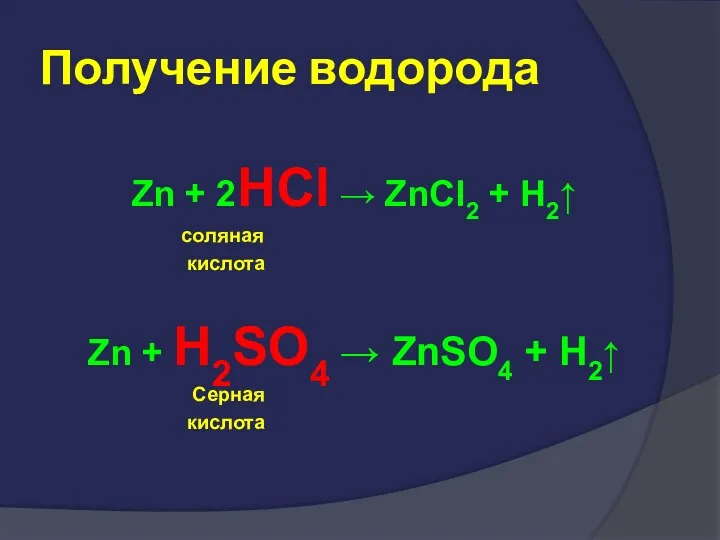
- 18. Получение водорода Zn + 2HCl → ZnCl2 + H2↑ соляная кислота Zn + H2SO4 → ZnSO4
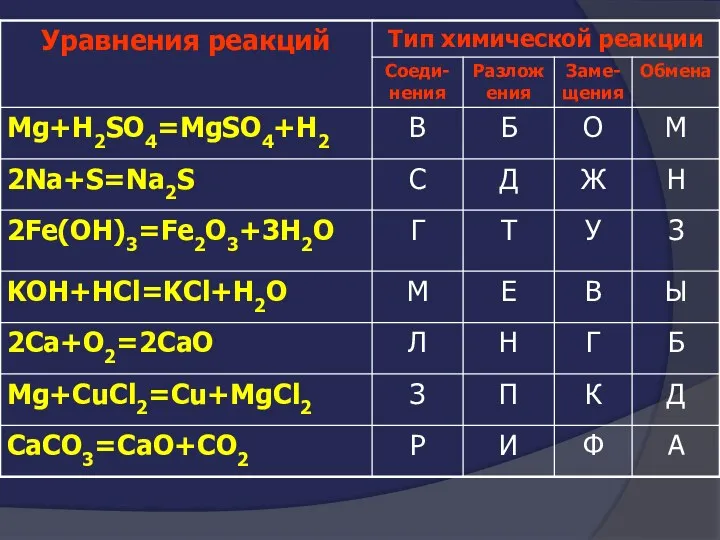
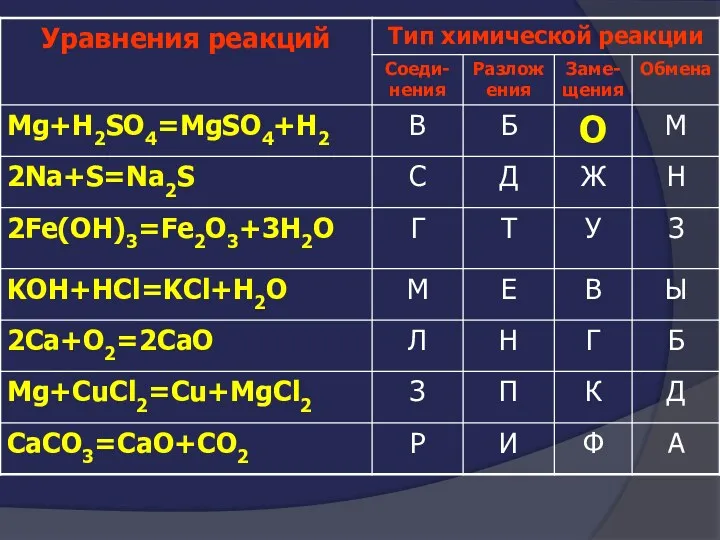
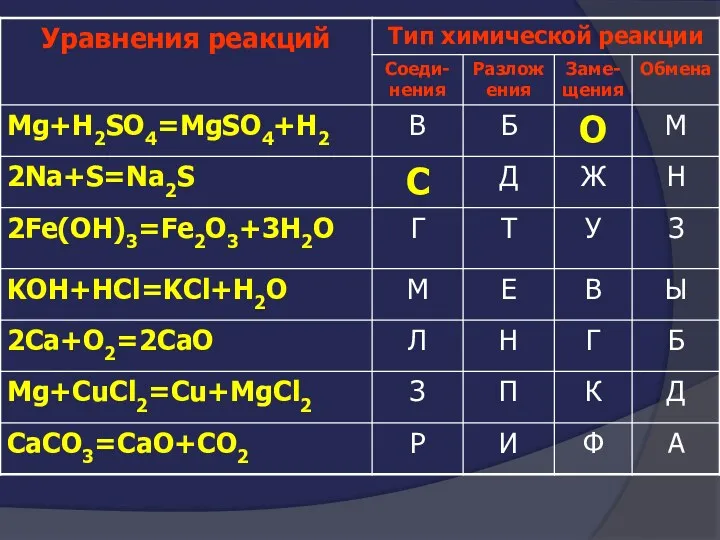
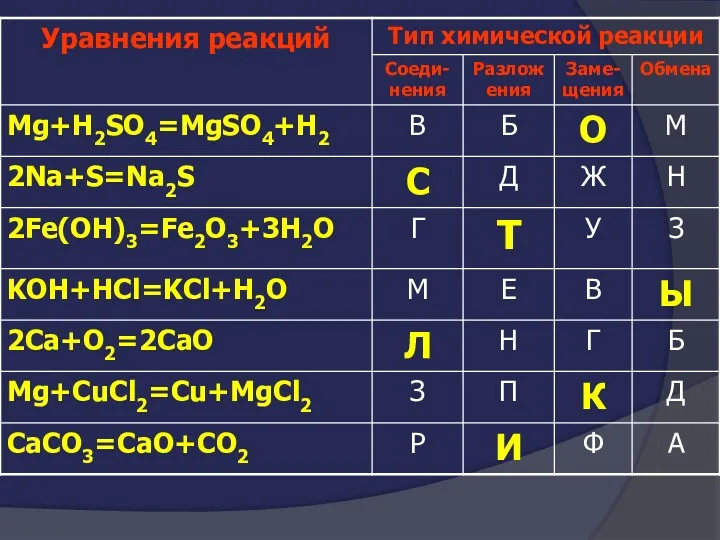
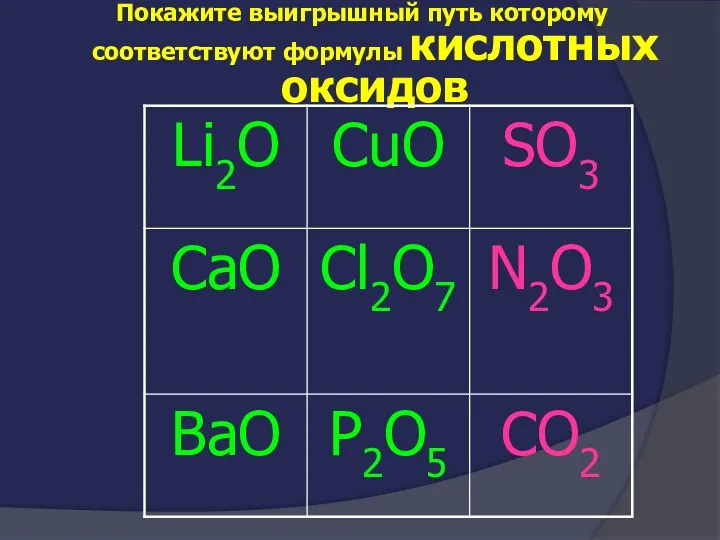
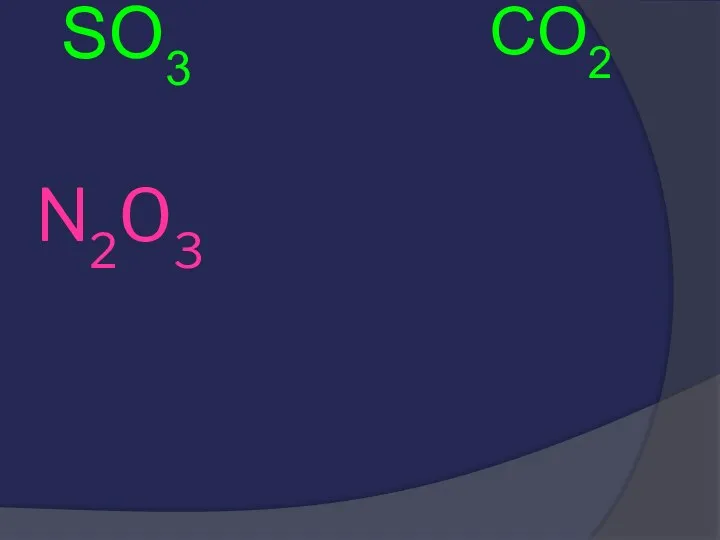
- 24. Покажите выигрышный путь которому соответствуют формулы кислотных оксидов
- 25. Покажите выигрышный путь которому соответствуют формулы кислотных оксидов
- 26. N2O3 SO3 CO2
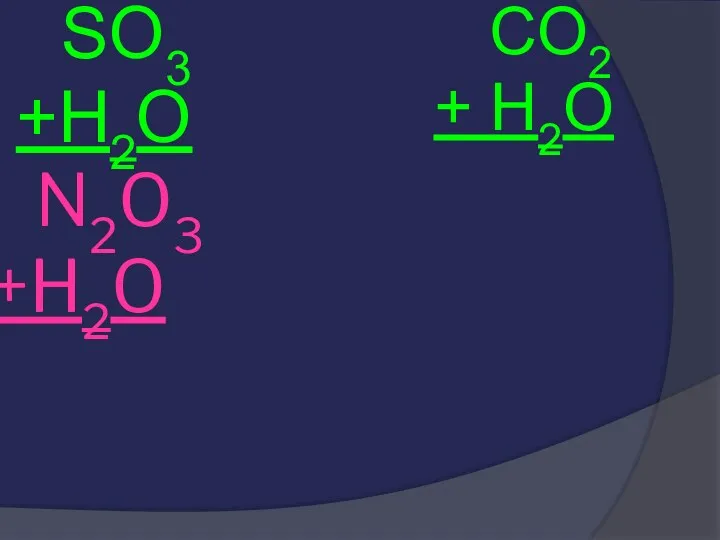
- 27. N2O3 +H2O SO3 +H2O CO2 + H2O
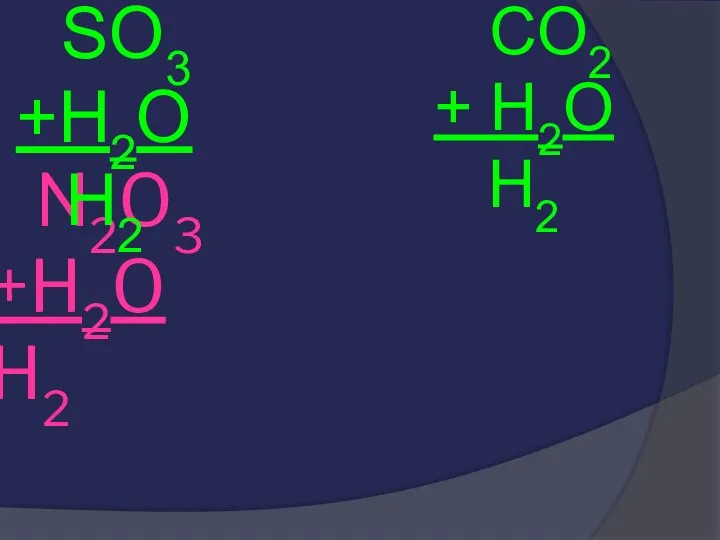
- 28. N2O3 +H2O H2 SO3 +H2O H2 CO2 + H2O H2
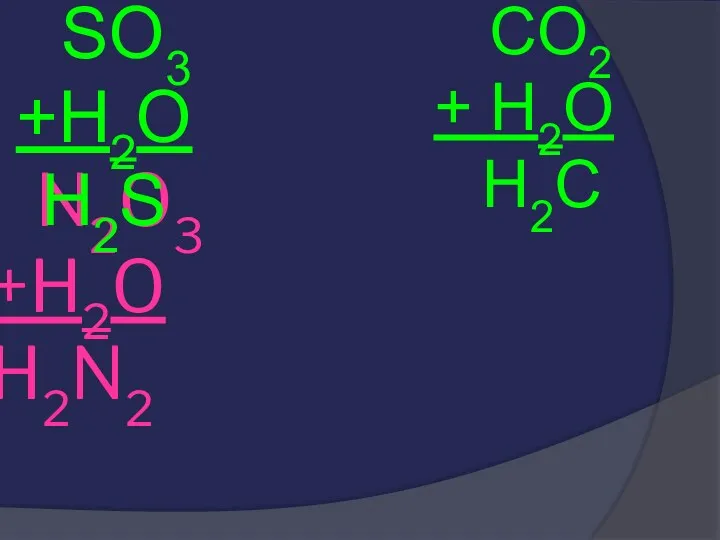
- 29. N2O3 +H2O H2N2 SO3 +H2O H2S CO2 + H2O H2C
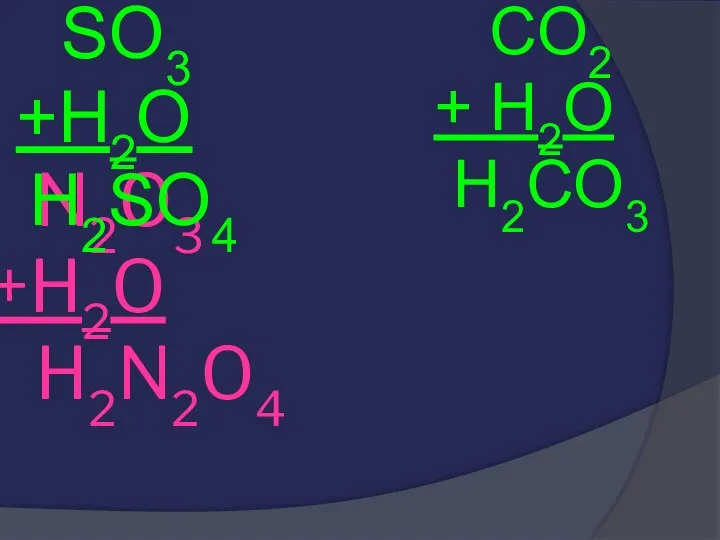
- 30. N2O3 +H2O H2N2O4 SO3 +H2O H2SO4 CO2 + H2O H2CO3
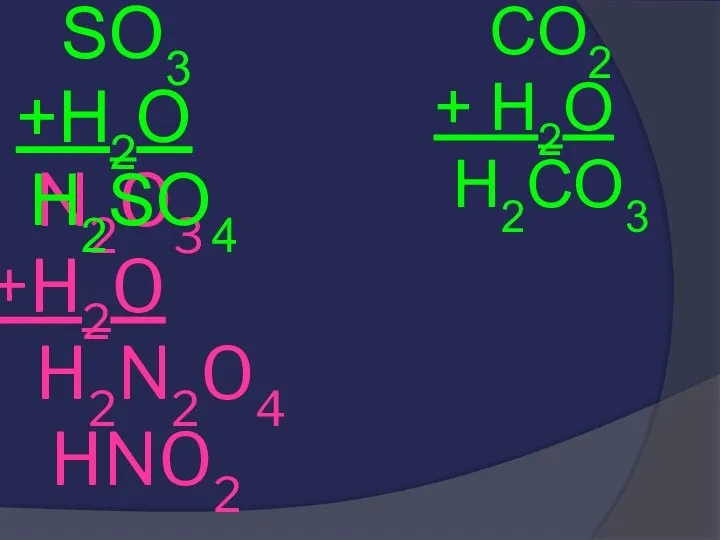
- 31. N2O3 +H2O H2N2O4 HNO2 SO3 +H2O H2SO4 CO2 + H2O H2CO3
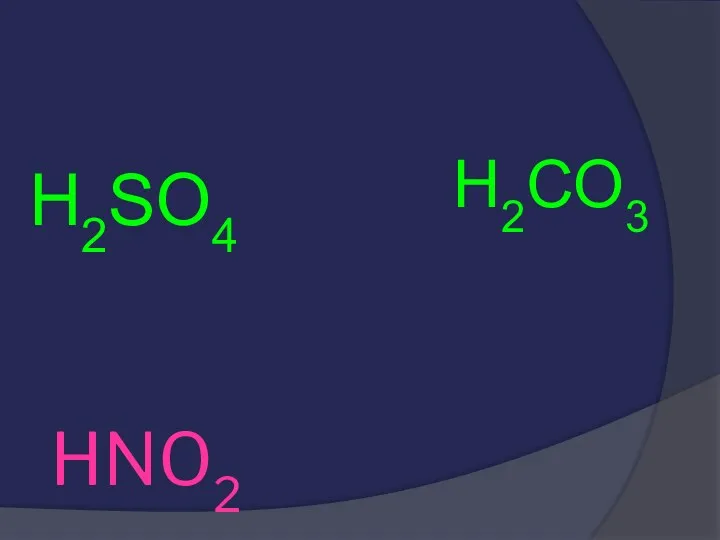
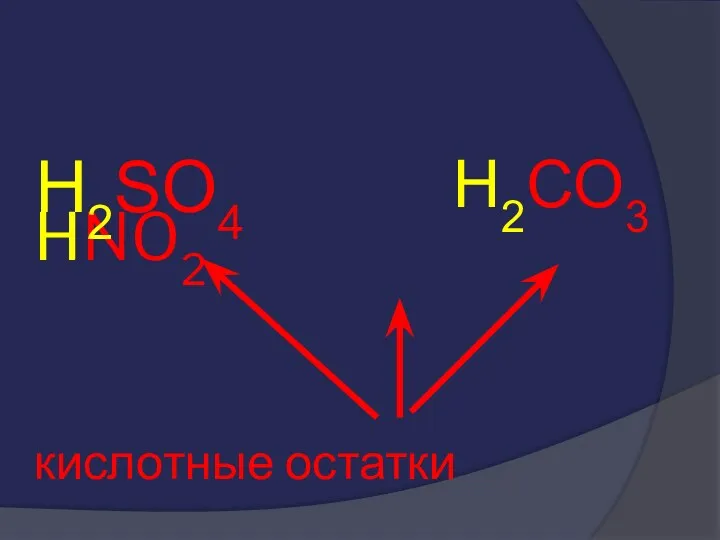
- 32. HNO2 H2SO4 H2CO3
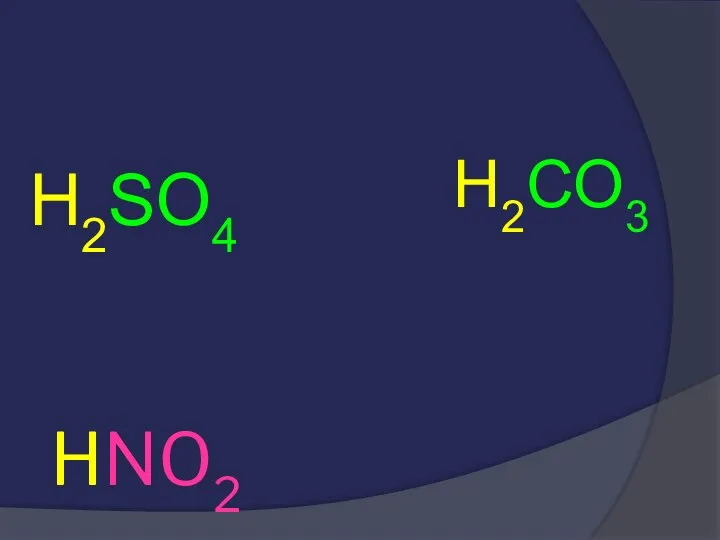
- 33. HNO2 H2SO4 H2CO3
- 34. HNO2 кислотные остатки H2SO4 H2CO3
- 35. Кислоты - это сложные вещества, состоящие из одного или нескольких атомов водорода и кислотного остатка HxR
- 36. X I HxR
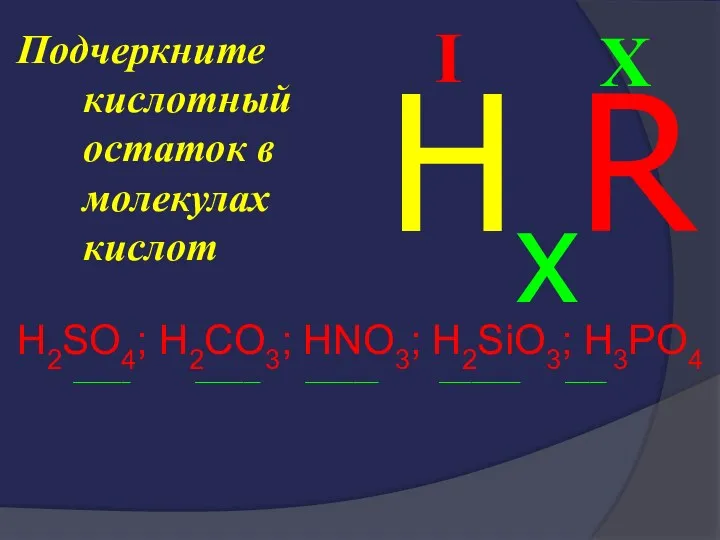
- 37. Подчеркните кислотный остаток в молекулах кислот H2SO4; H2CO3; HNO3; H2SiO3; H3PO4 _______ ________ _________ __________ _____
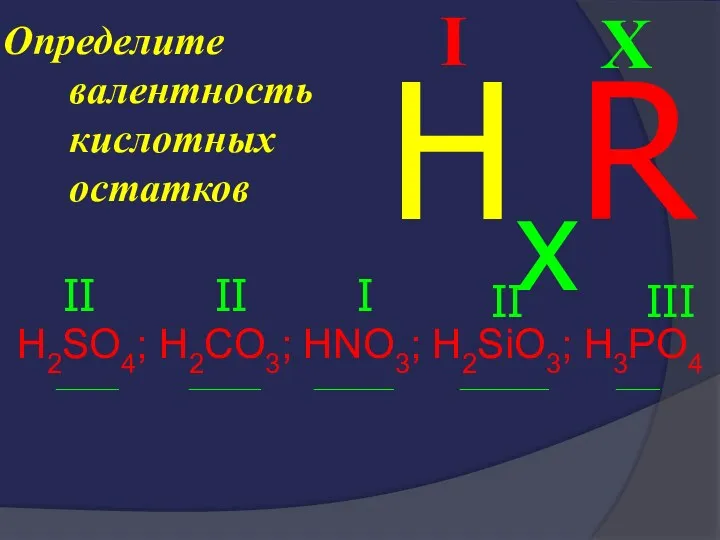
- 38. Определите валентность кислотных остатков H2SO4; H2CO3; HNO3; H2SiO3; H3PO4 _______ ________ _________ __________ _____ X I
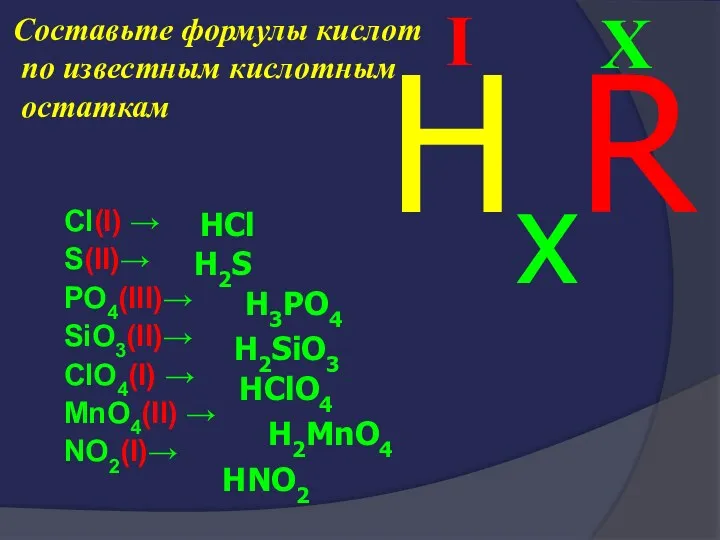
- 39. Составьте формулы кислот по известным кислотным остаткам Cl(I) → S(II)→ PO4(III)→ SiO3(II)→ ClO4(I) → MnO4(II) →
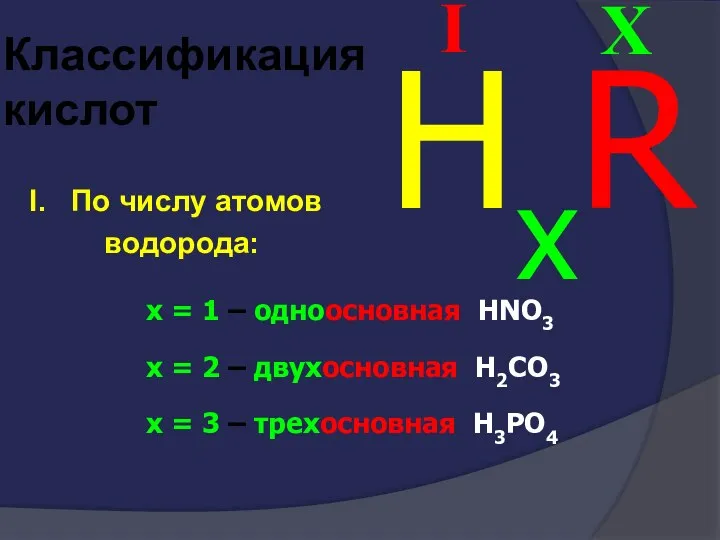
- 40. Классификация кислот I. По числу атомов водорода: X I HxR x = 1 – одноосновная HNO3
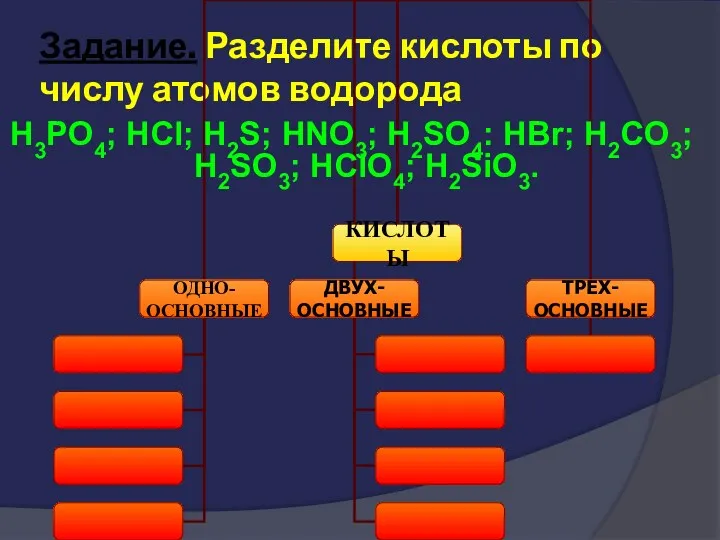
- 41. Задание. Разделите кислоты по числу атомов водорода H3PO4; HCl; H2S; HNO3; H2SO4: HBr; H2CO3; H2SO3; HClO4;
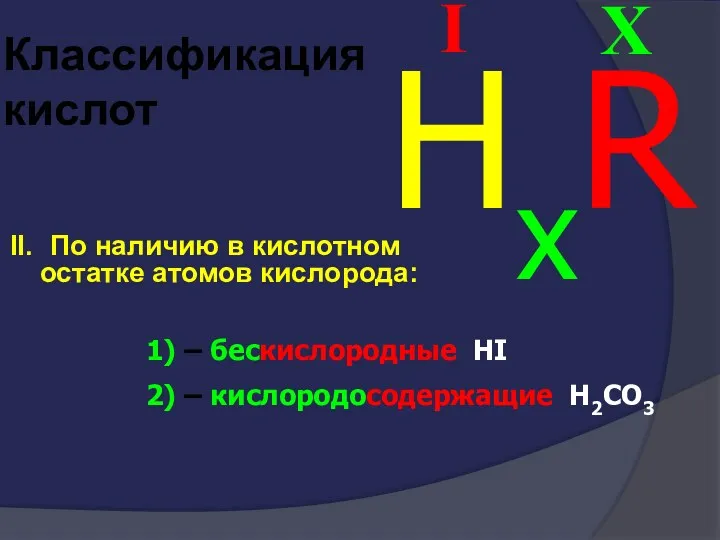
- 42. Классификация кислот II. По наличию в кислотном остатке атомов кислорода: X I HxR 1) – бескислородные
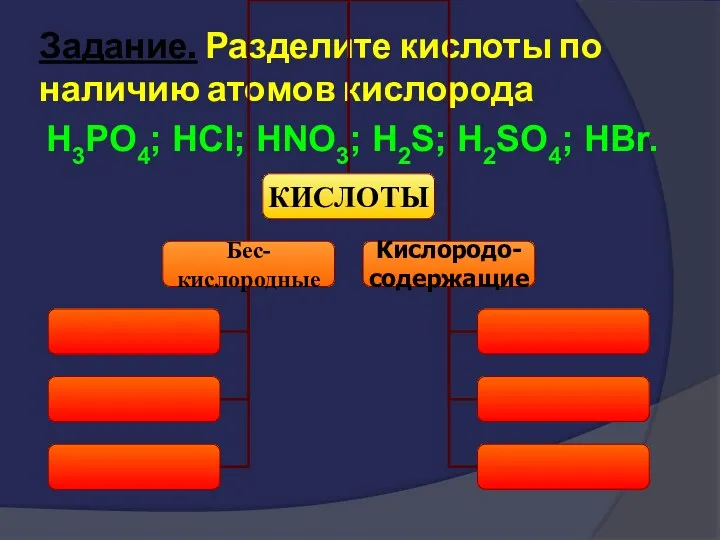
- 43. Задание. Разделите кислоты по наличию атомов кислорода H3PO4; HCl; HNO3; H2S; H2SO4; HBr.
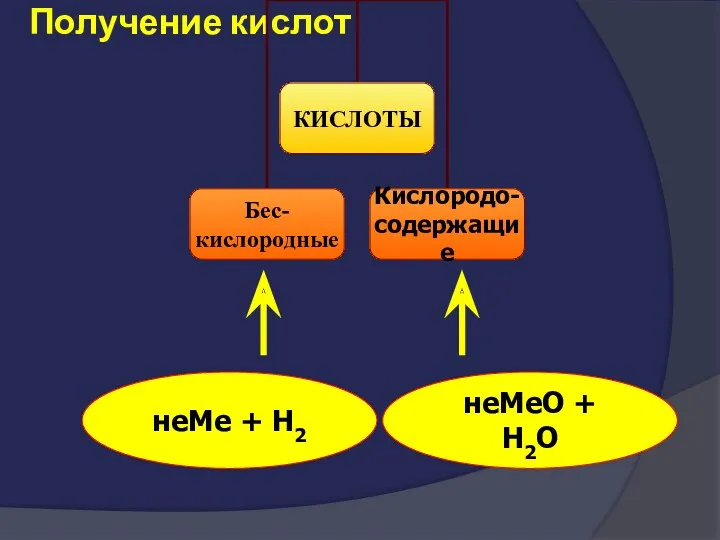
- 44. Получение кислот неМе + Н2 неМеО + Н2О
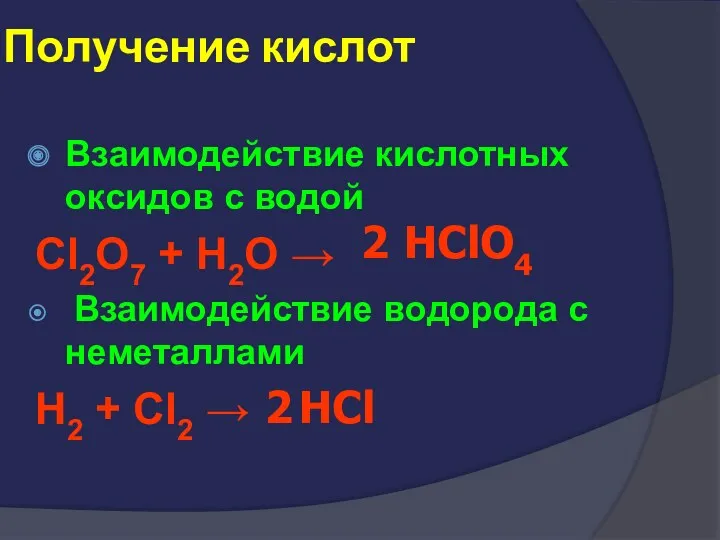
- 45. Получение кислот Взаимодействие кислотных оксидов с водой Cl2O7 + H2O → Взаимодействие водорода с неметаллами H2
- 46. Физические свойства кислот H2 CO3 = CO2↑ +H2O – угольная кислота H2SO3 = SO2↑ + H2O
- 47. Индикаторы вещества, дающие цветные химические реакции в зависимости от среды раствора Лакмус Метилоранж Фенолфталеин
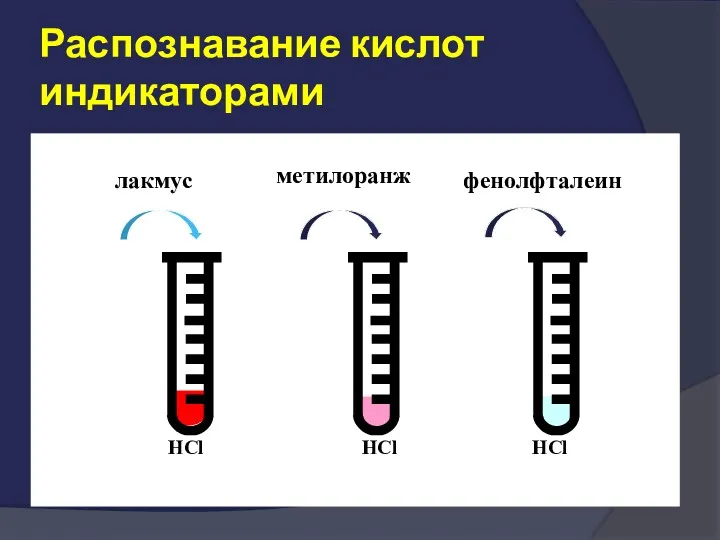
- 48. Распознавание кислот индикаторами лакмус метилоранж фенолфталеин HCl HCl HCl
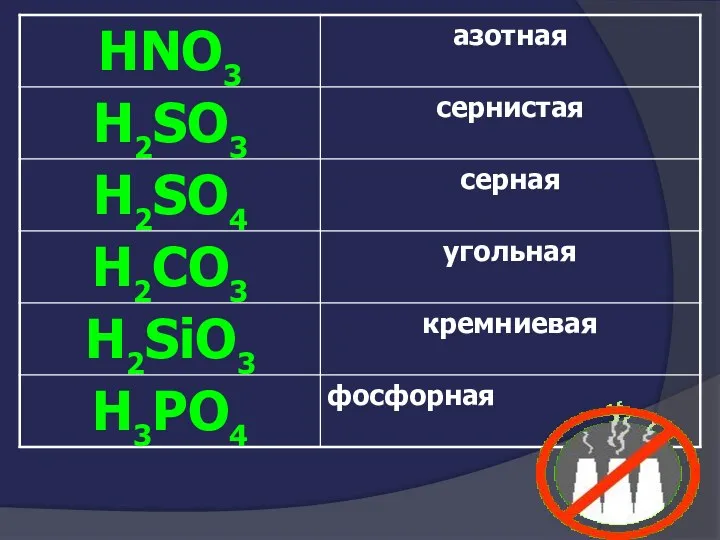
- 49. Названия кислот.
- 51. Что запомнили?
- 52. Что поняли?
- 53. Чему научились?
- 54. 1. Найди группу формул кислот: а) NH3 HCl H2 SO4 б) H2S HNO3 HBr в) HCl
- 55. 3. Даны вещества: CuO, NaOH, H3PO4, CO2, CaCO3, HCl, Cu(OH)2, HNO3, BaO, H2S, K2SO3, H2SO4, Al(OH)3,
- 56. Домашнее задание § 34, 36 готовиться к химическому диктанту по названиям кислот с листа-упражнения выполнить задания
- 58. Скачать презентацию



















 Значение органической химии в жизни человека
Значение органической химии в жизни человека Коррозия металлов
Коррозия металлов Водород. Изотопы водорода. Свойства, получение и применение водорода. Топливные элементы
Водород. Изотопы водорода. Свойства, получение и применение водорода. Топливные элементы Неорганические строительные материалы. Стекло
Неорганические строительные материалы. Стекло Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Урок + презентация Азот. 9 класс.
Урок + презентация Азот. 9 класс. Токсическое действие диоксинов и диоксиноподоных соединений
Токсическое действие диоксинов и диоксиноподоных соединений Розчин і його компоненти
Розчин і його компоненти Ароматические углеводороды. Арены
Ароматические углеводороды. Арены Carbohydrates (sugars)
Carbohydrates (sugars) Коррозия и методы борьбы с ней
Коррозия и методы борьбы с ней Поверхностно-активные вещества (ПАВ). Классификация, свойства и условия применения
Поверхностно-активные вещества (ПАВ). Классификация, свойства и условия применения Alyuminiy_ego_soedinenia
Alyuminiy_ego_soedinenia Фосфор
Фосфор Воспламенение (зажигание) газовых смесей
Воспламенение (зажигание) газовых смесей Теоретическое и прикладное материаловедение. Занятие 2
Теоретическое и прикладное материаловедение. Занятие 2 Строение атома. Теории строения атома
Строение атома. Теории строения атома Химия в продуктах питания
Химия в продуктах питания Алкины
Алкины Silicon. Silicate minerals. Weathering
Silicon. Silicate minerals. Weathering Соли. Определение солей
Соли. Определение солей Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів
Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворах
Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворах Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Электрохимические производства
Электрохимические производства Масс-Спектроскопия
Масс-Спектроскопия Борьба с биологической коррозией
Борьба с биологической коррозией Көміртекті материалдар
Көміртекті материалдар