Содержание
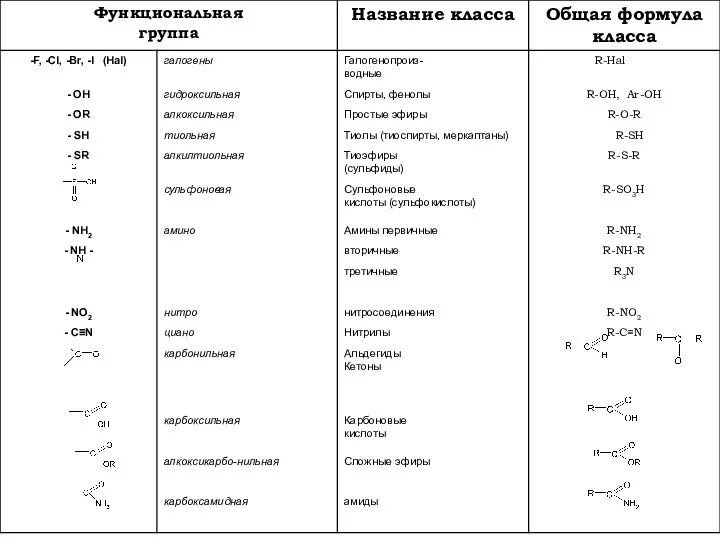
- 2. ПЛАН ЛЕКЦИИ Классификация (электронная версия) Номенклатура (электронная версия) Теория химического строения Типы гибридизации, конформации Виды связей
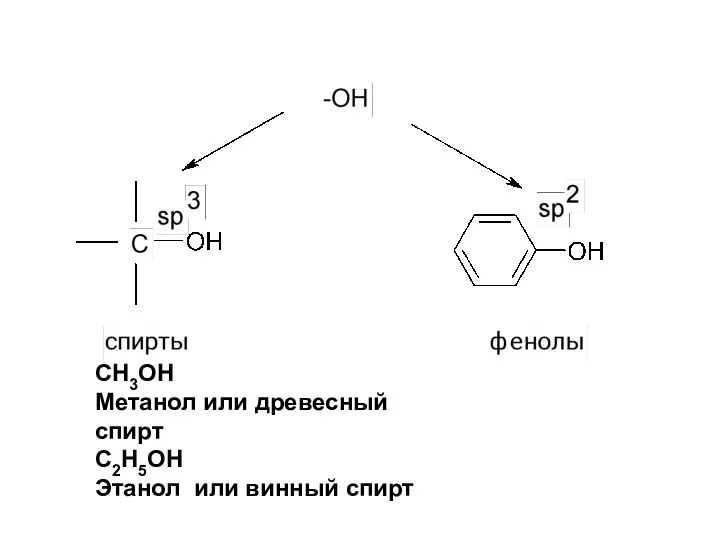
- 4. СН3ОН Метанол или древесный спирт С2Н5ОН Этанол или винный спирт
- 6. Тривиальные и номенклатурные названия альдегидов Тривиальные номенклатурные формальдегид метаналь уксусный альдегид этаналь пропионовый альдегид пропаналь масляный
- 7. Тривиальные и номенклатурные названия монокарбоновых кислот и их солей НСООН муравьиная /метановая формиаты СН3СООН уксусная/этановая ацетаты
- 8. Тривиальные и номенклатурные названия дикарбоновых кислот и их солей НООС-СООН щавелевая/этандиовая оксалаты НООС-СН2-СООН малоновая/пропандиовая малоаты НООС-СН2-СН2-
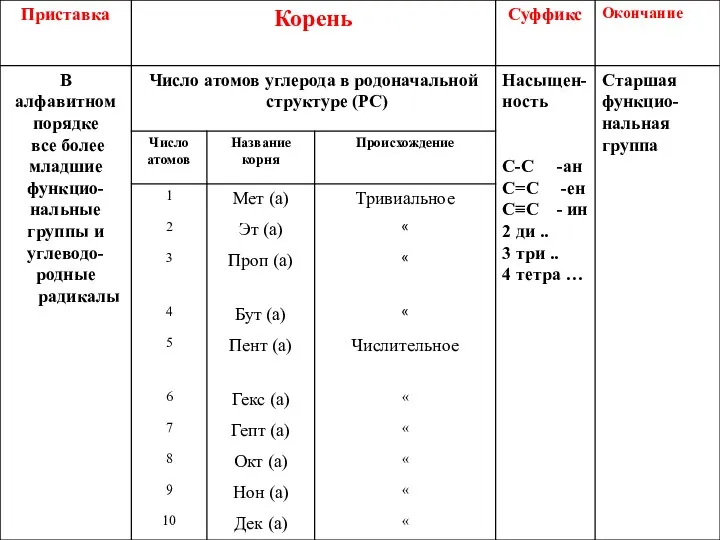
- 9. Заместительная систематическая номенклатура органических соединений (IUPAC)
- 12. 3.Химическое строение органических соединений 1.Типы гибридизации атомов. Конформации молекул
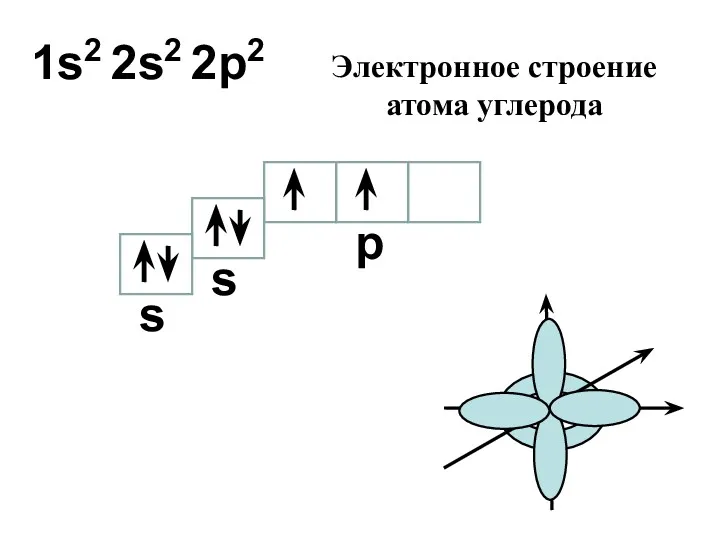
- 13. 1s2 2s2 2p2 s s p Электронное строение атома углерода
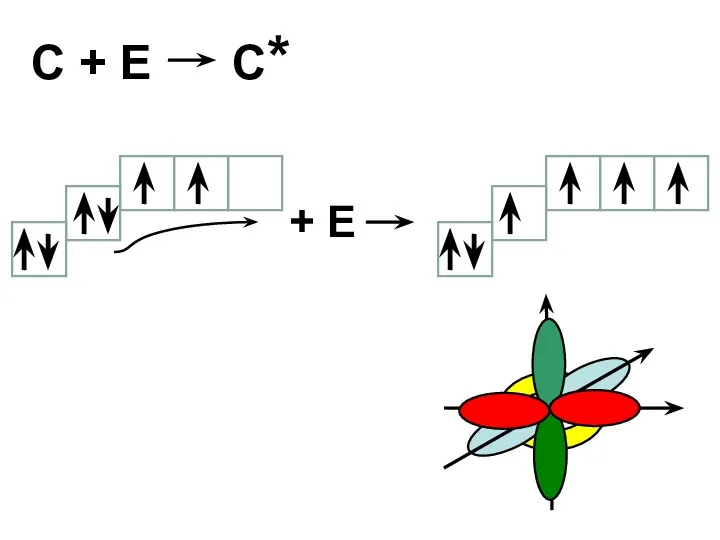
- 14. C + E C* + E
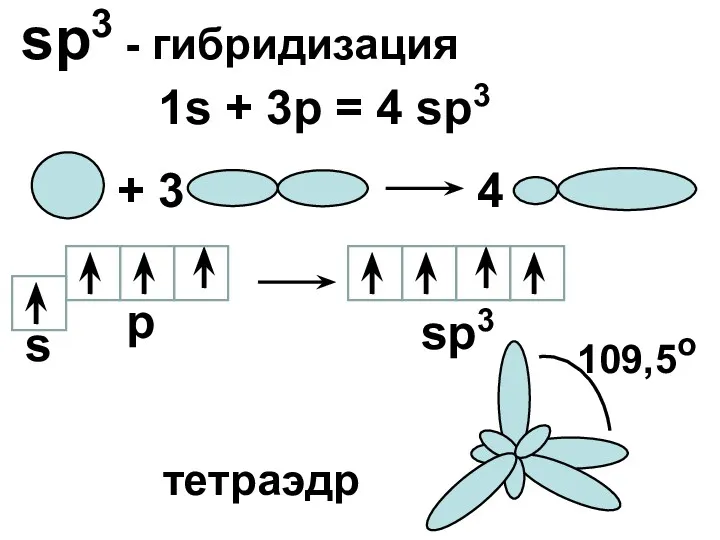
- 15. sp3 - гибридизация 1s + 3p = 4 sp3 + 3 4 s p sp3 109,5o
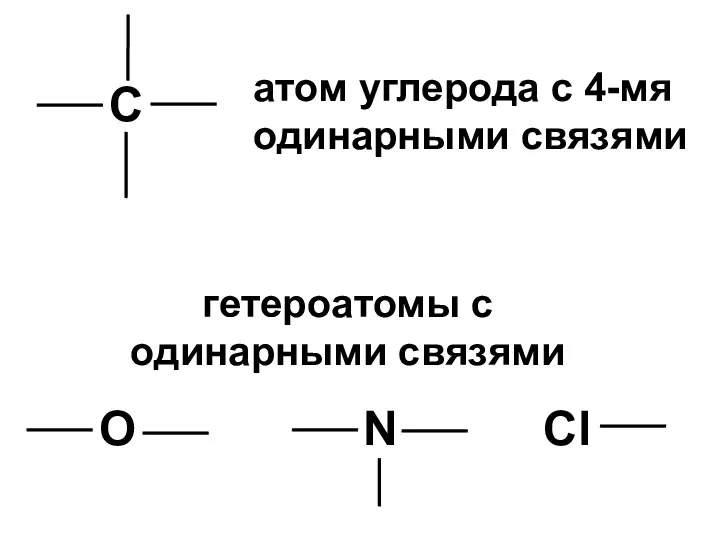
- 16. С атом углерода с 4-мя одинарными связями гетероатомы с одинарными связями О N Cl
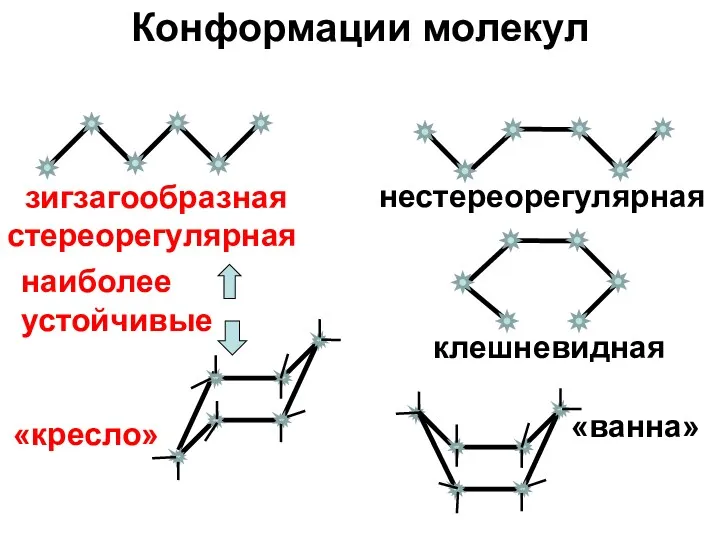
- 17. Конформации молекул зигзагообразная стереорегулярная клешневидная нестереорегулярная «кресло» «ванна» наиболее устойчивые
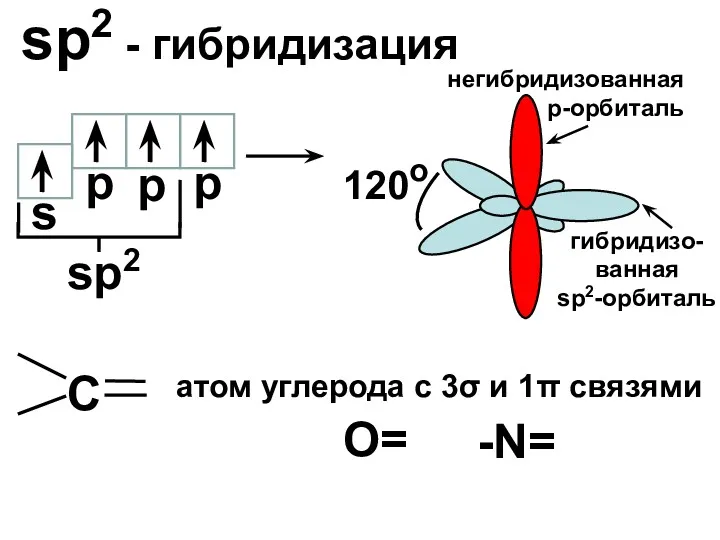
- 18. sp2 - гибридизация s p sp2 120o p p негибридизованная р-орбиталь гибридизо-ванная sp2-орбиталь С атом углерода
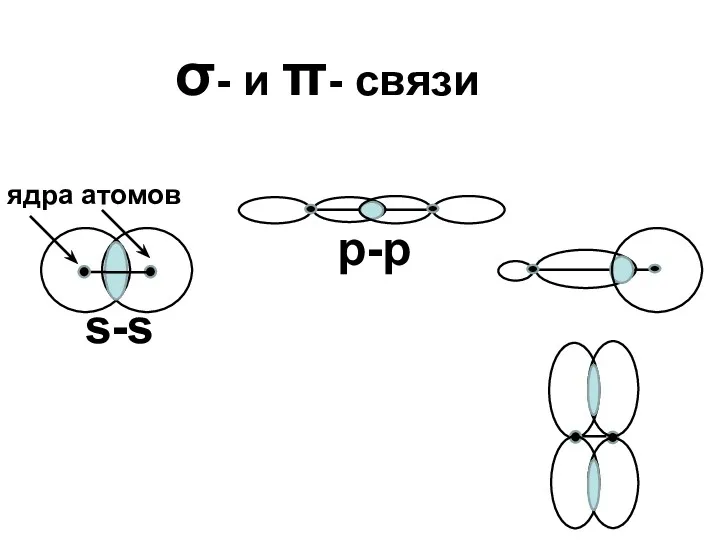
- 19. σ- и π- связи s-s ядра атомов р-р
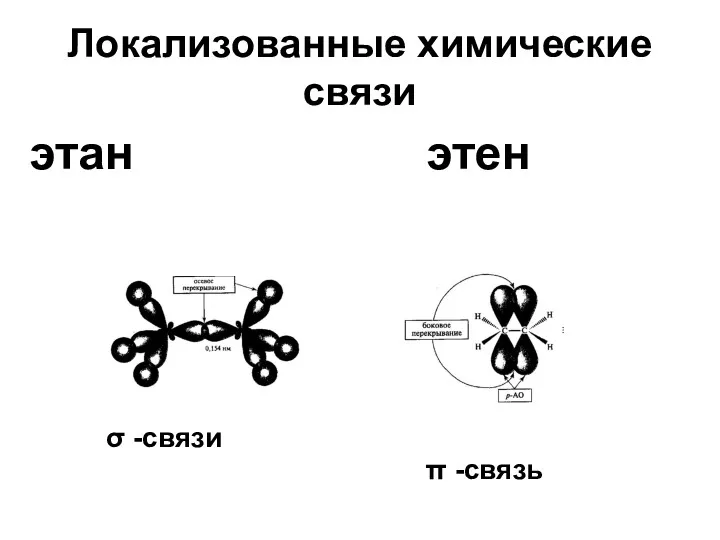
- 20. Локализованные химические связи этан этен σ -связи π -связь
- 21. Явление сопряжения
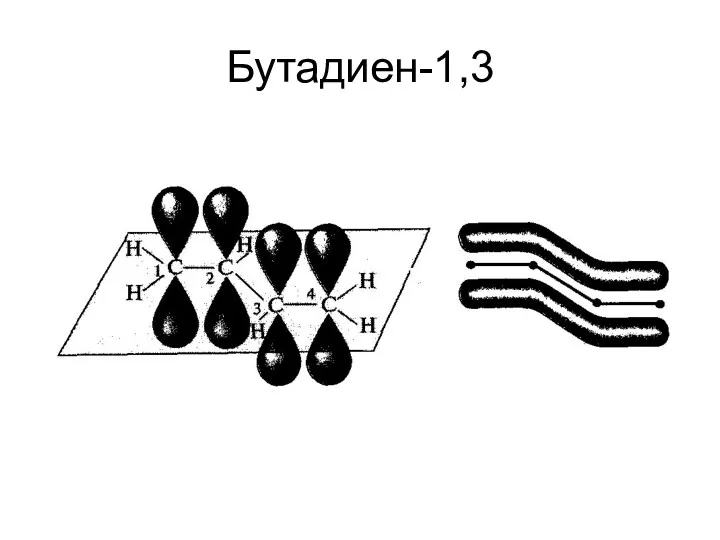
- 22. Бутадиен-1,3
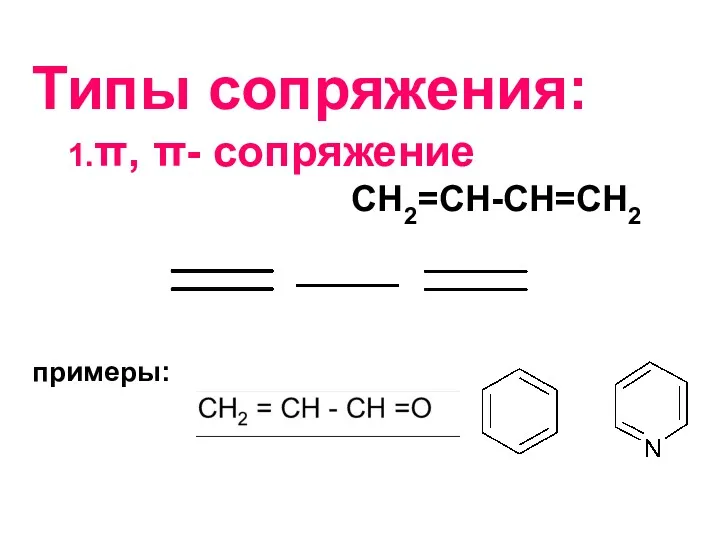
- 23. Типы сопряжения: 1.π, π- сопряжение СН2=СН-СН=СН2 примеры:
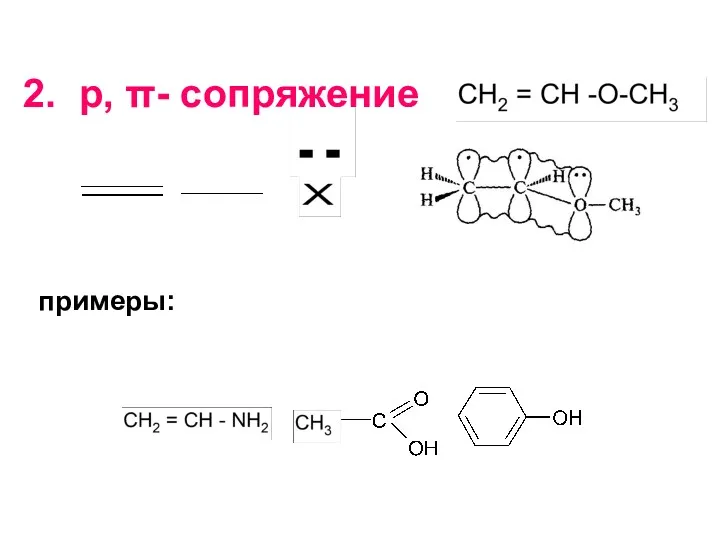
- 24. примеры: 2. р, π- сопряжение
- 25. Число электронов в сопряжении: π-связь предоставляет 2 электрона, гетероатом в р,π-сопряжении также предоставляет 2 электрона
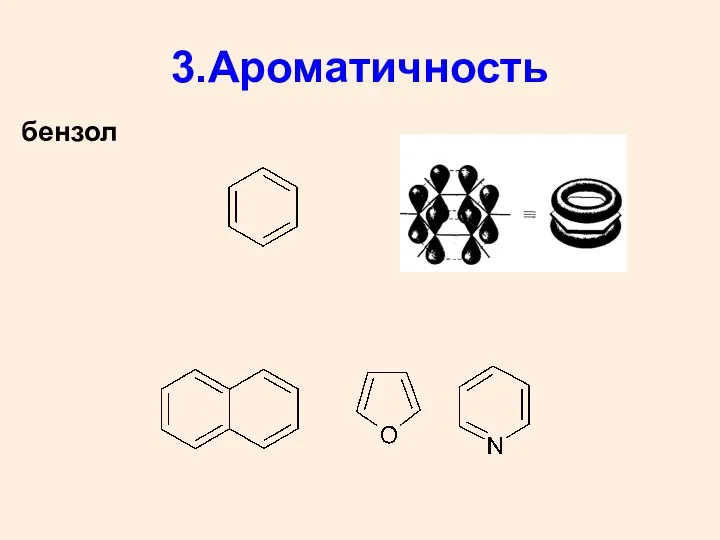
- 26. 3.Ароматичность бензол
- 27. Структурные признаки ароматичности плоскостное строение цикла (все атомы в sp2 – гибридном состоянии); замкнутая π-сопряженная система
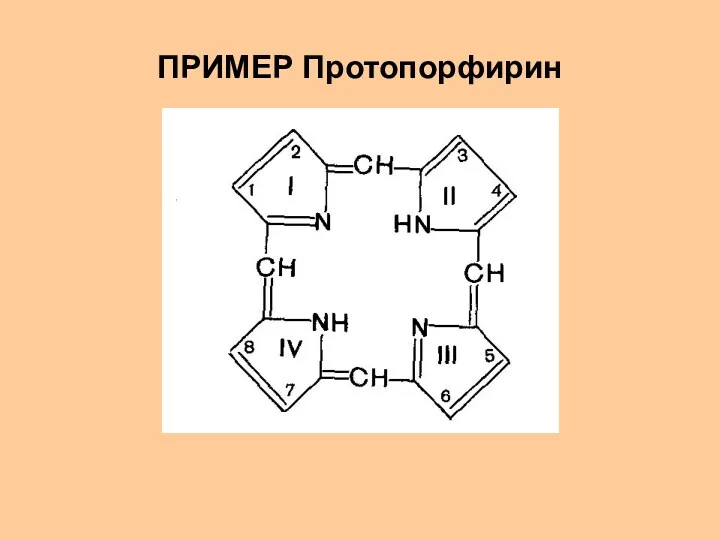
- 28. ПРИМЕР Протопорфирин
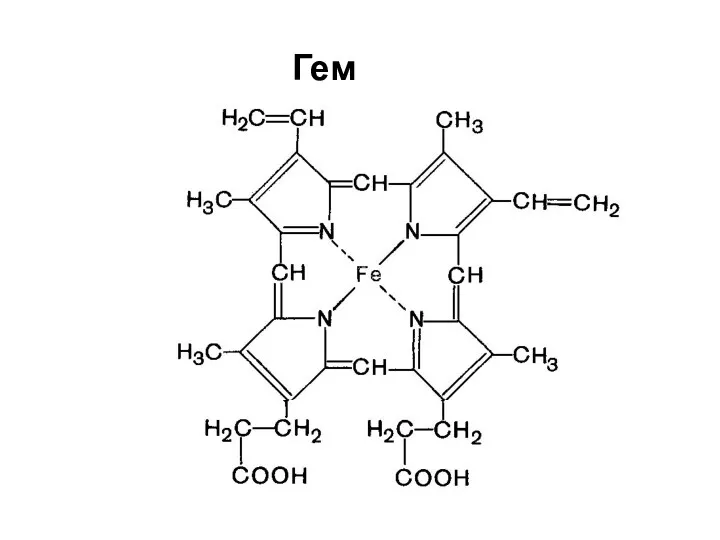
- 29. Гем
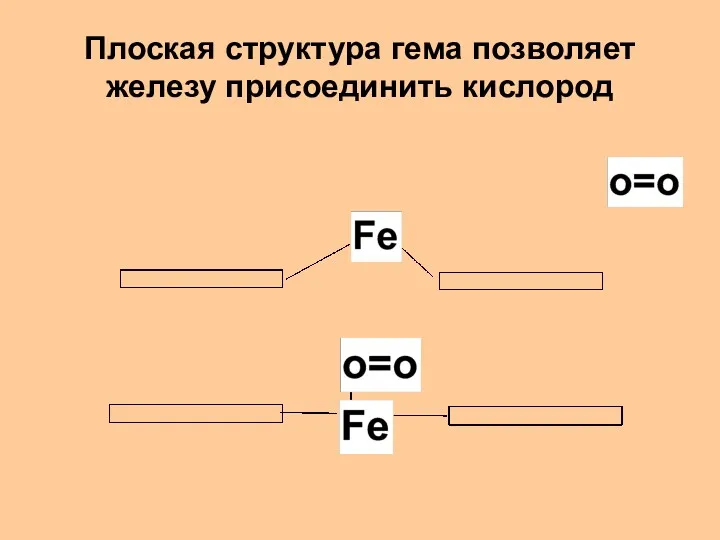
- 30. Плоская структура гема позволяет железу присоединить кислород
- 31. Взаимное влияние атомов в органических молекулах
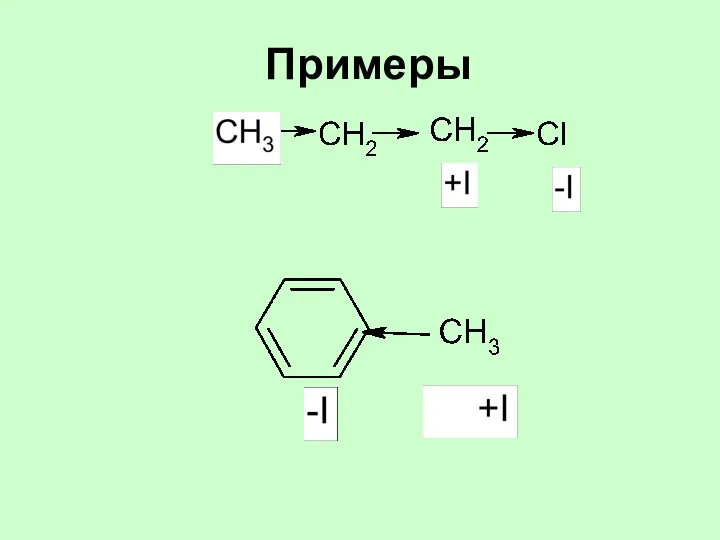
- 32. Индуктивный электронный эффект (±I) Сравнительная электроотрицательность F> O > N > Csp > Csp2 > Csp3
- 33. Примеры
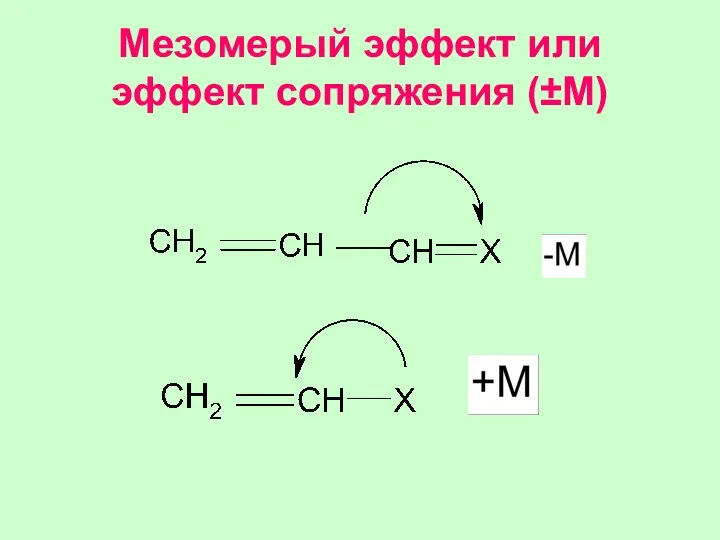
- 34. Мезомерый эффект или эффект сопряжения (±M)
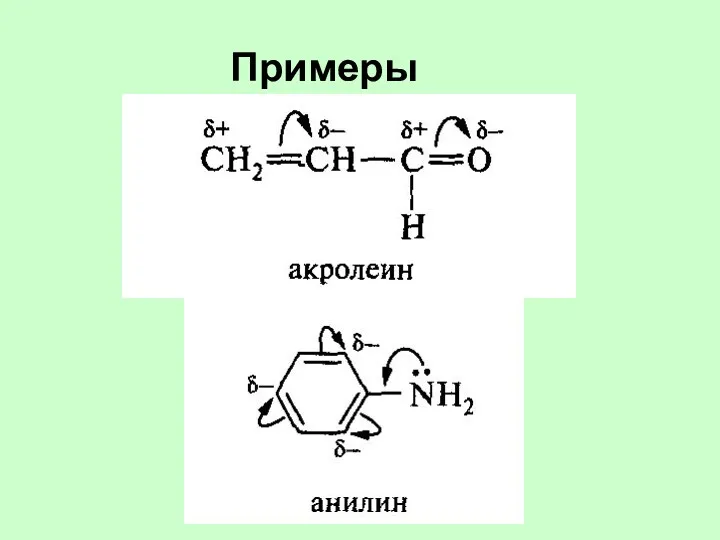
- 35. Примеры
- 36. Электронный эффекты заместителей
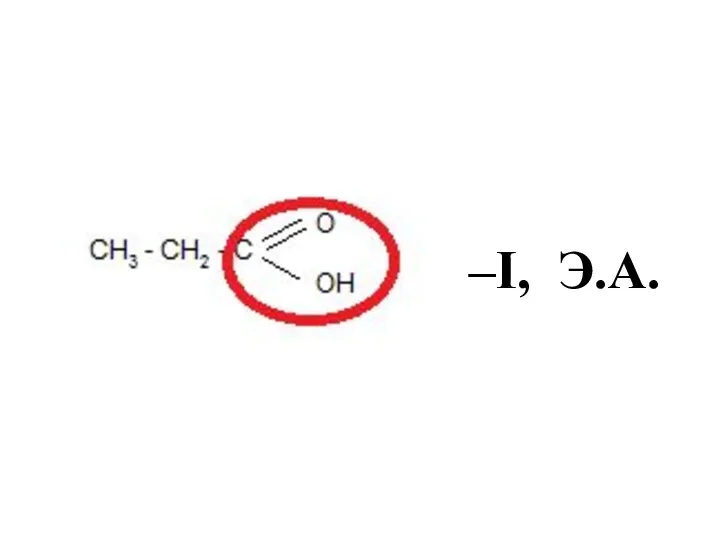
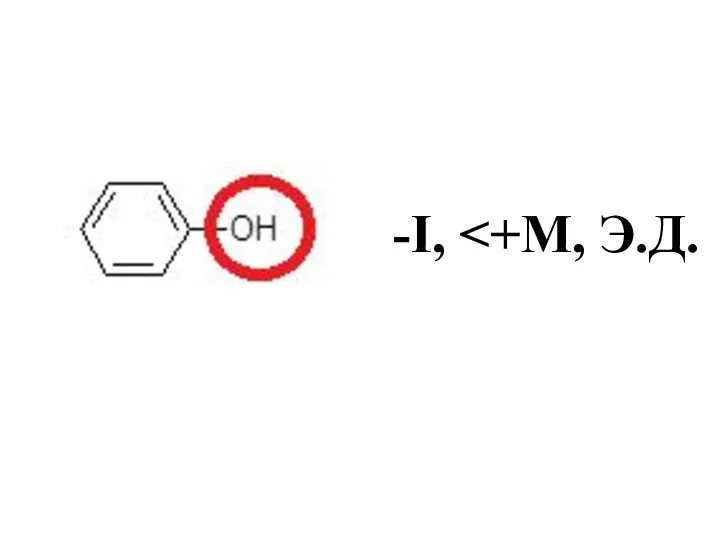
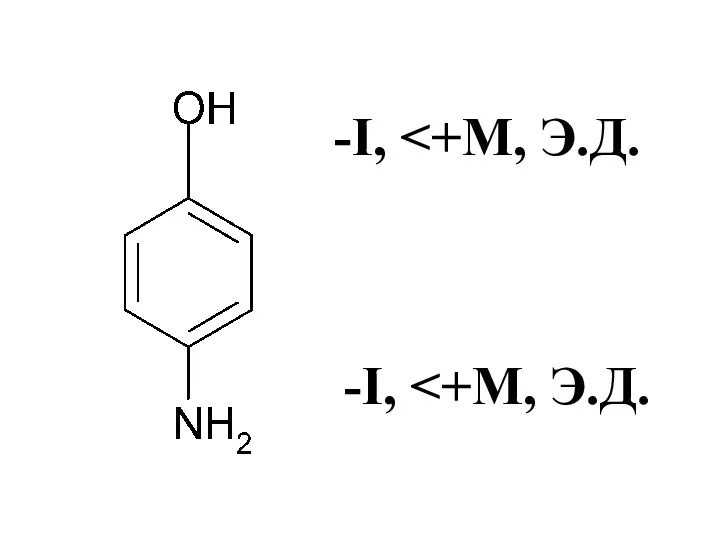
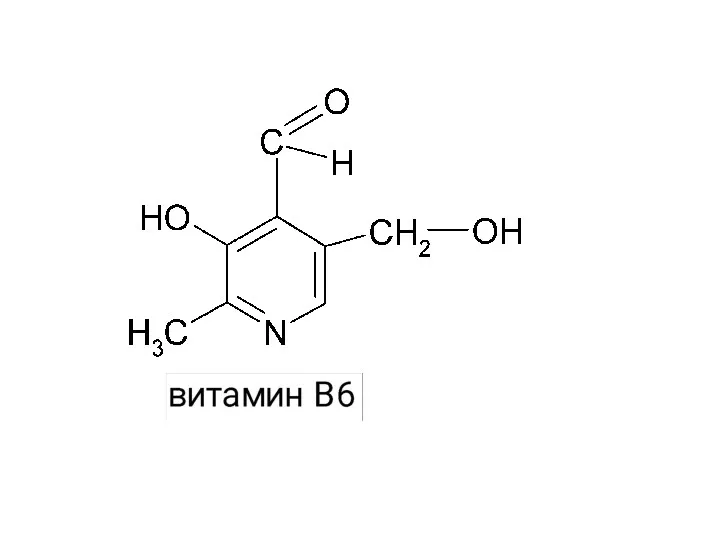
- 37. Функциональные группы как электронодоноры или электроноакцепторы -I , Э.А.
- 38. –I, Э.А.
- 39. -I,
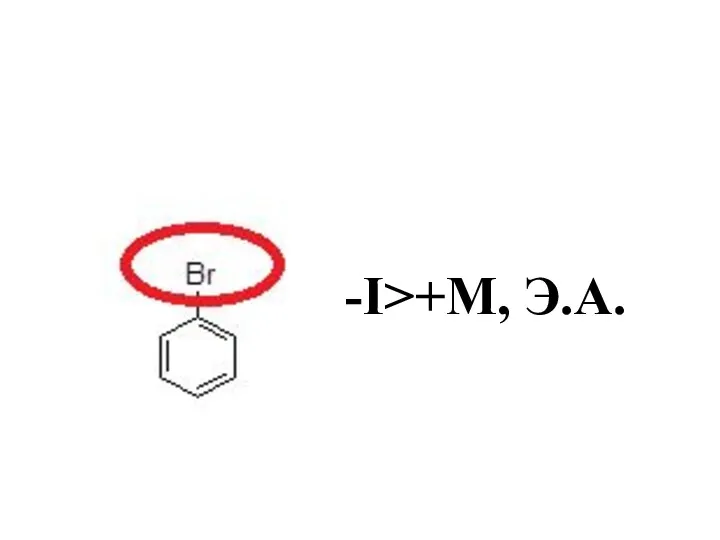
- 40. -I>+М, Э.А.
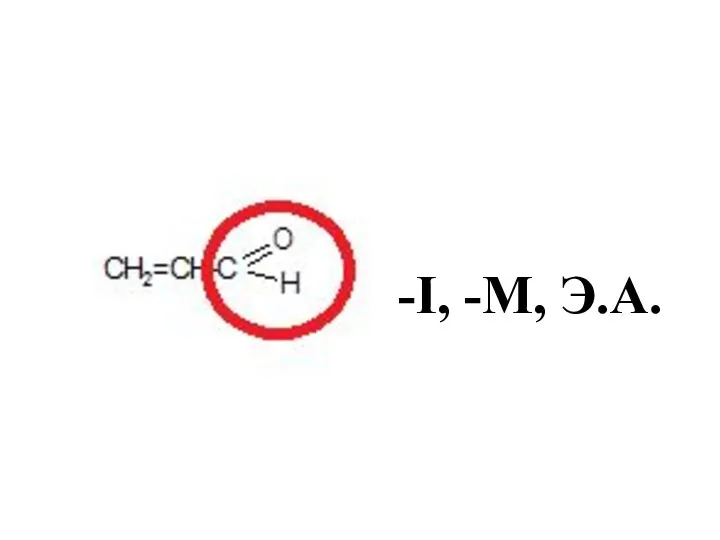
- 41. -I, -М, Э.А.
- 43. -I, -I,
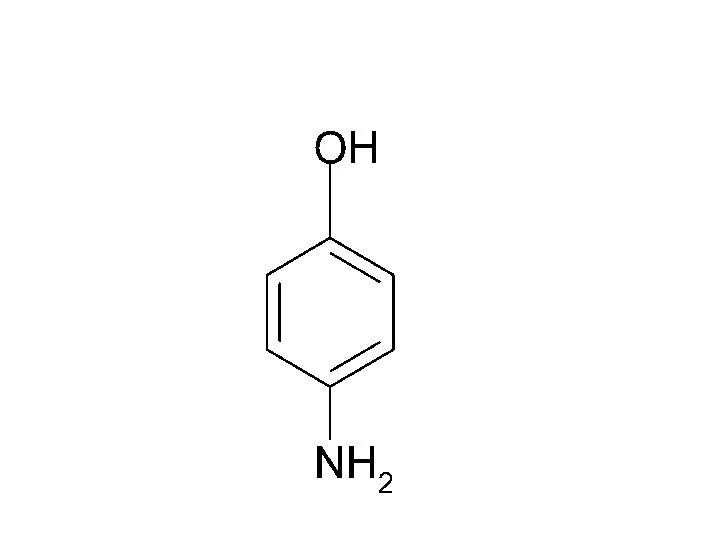
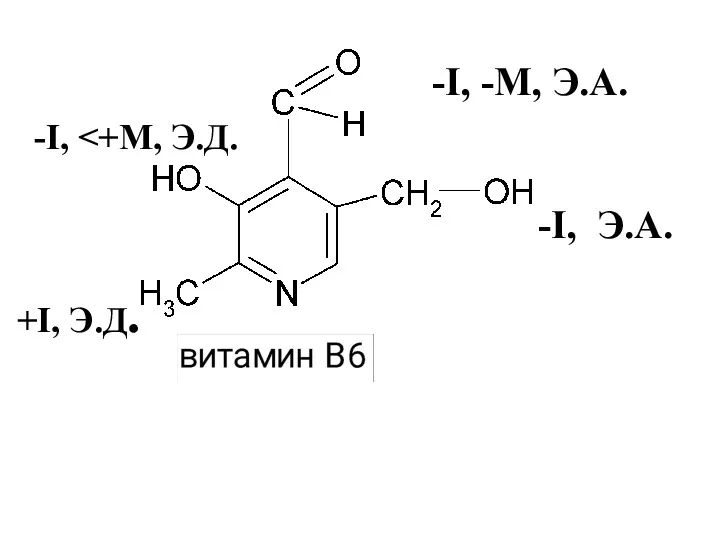
- 45. -I, -I, -М, Э.А. +I, Э.Д. -I, Э.А.
- 47. Реакционная способность органических соединений
- 48. Виды химических реакций I.Кислотно-основные II. Характерные реакции органических соединений Окислительно-восстановительные реакции III. IV. Качественные реакции
- 49. I. Кислотно-основные свойства органических соединений Кислота R-XH Кислотный центр -ХН -SH, -OH, -NH, -CH Основание H-X
- 50. R – XH = R-X- + H+ кислота сопряженное основание (анион) Усиливают кислотность: сопряжение с кислотным
- 51. карбоновые кислоты> фенолы > тиолы > многоатомные спирты> одноатомные спирты > амины
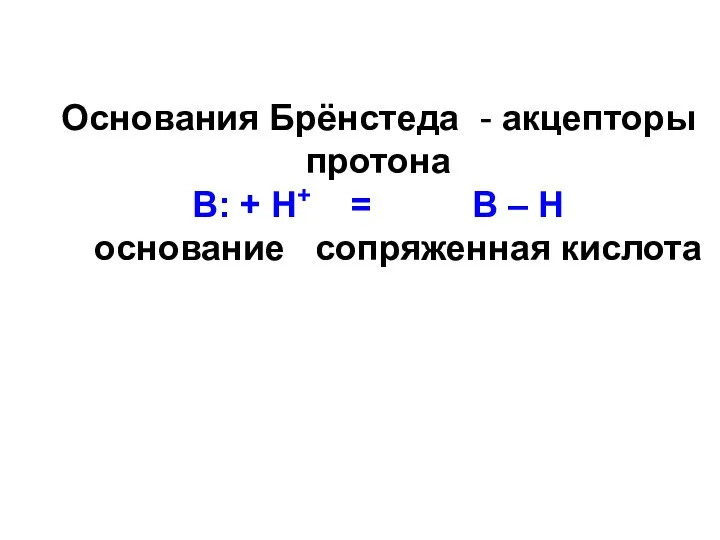
- 52. Основания Брёнстеда - акцепторы протона В: + Н+ = В – Н основание сопряженная кислота
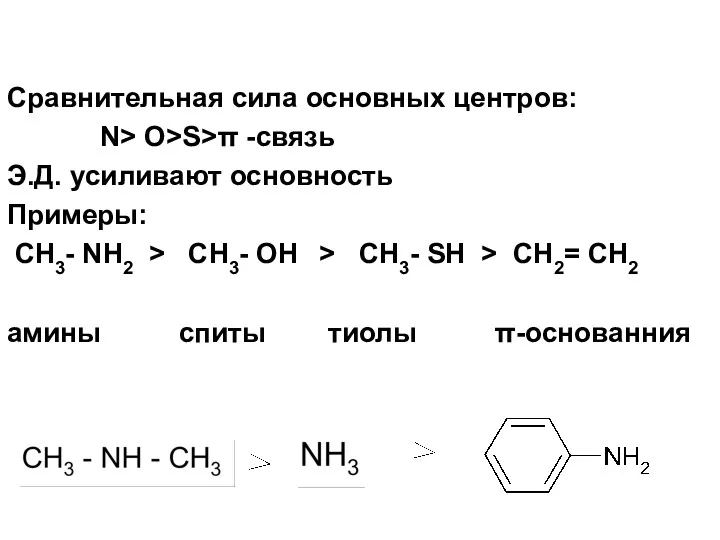
- 53. Сравнительная сила основных центров: N> O>S>π -связь Э.Д. усиливают основность Примеры: CH3- NH2 > CH3- OH
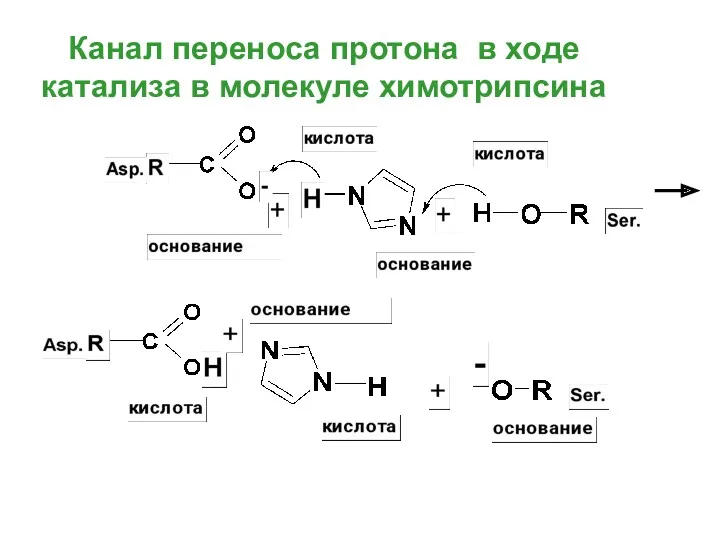
- 54. Канал переноса протона в ходе катализа в молекуле химотрипсина
- 55. Характерные реакции органических соединений
- 56. Основные понятия Субстрат – вещество, у которого происходит разрыв связи у атома углерода. Определяет тип реакции
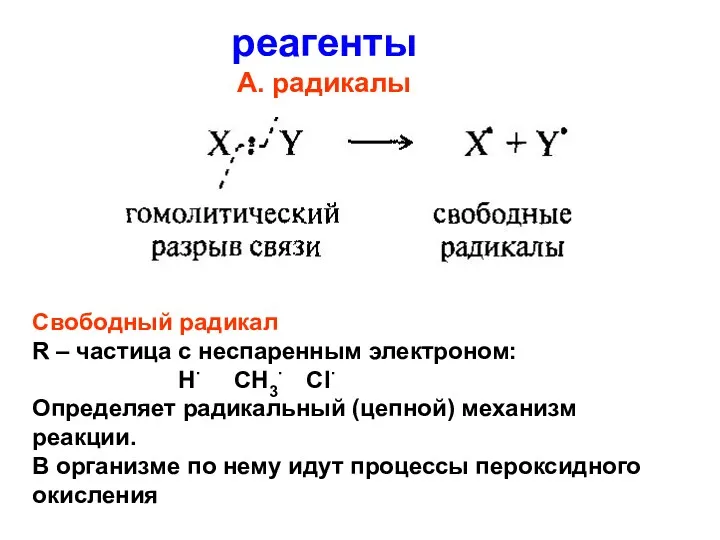
- 57. реагенты А. радикалы Свободный радикал R – частица с неспаренным электроном: Н∙ СН3∙ Сl∙ Определяет радикальный
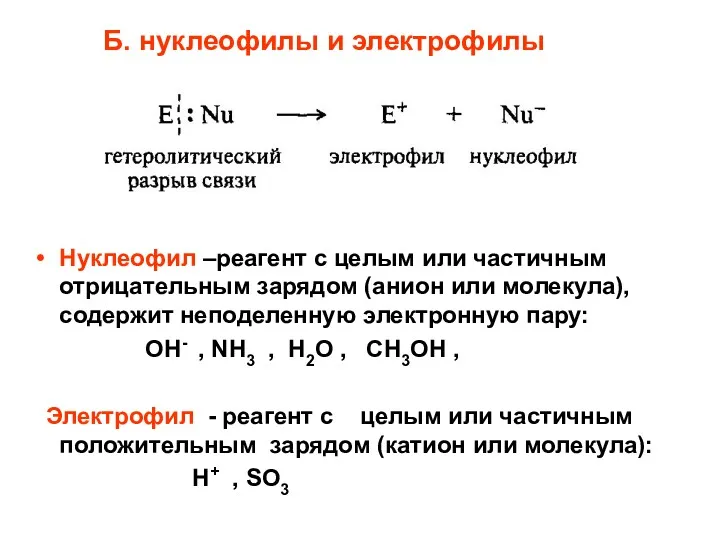
- 58. Б. нуклеофилы и электрофилы Нуклеофил –реагент с целым или частичным отрицательным зарядом (анион или молекула), содержит
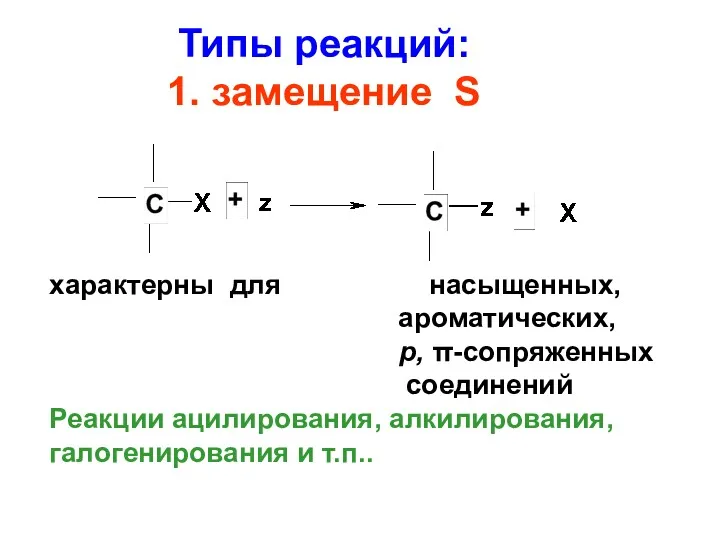
- 59. Типы реакций: 1. замещение S характерны для насыщенных, ароматических, р, π-сопряженных соединений Реакции ацилирования, алкилирования, галогенирования
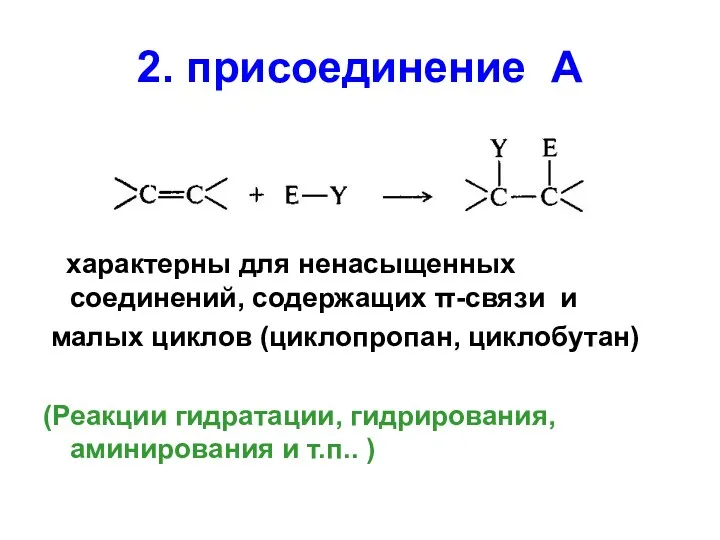
- 60. 2. присоединение А характерны для ненасыщенных соединений, содержащих π-связи и малых циклов (циклопропан, циклобутан) (Реакции гидратации,
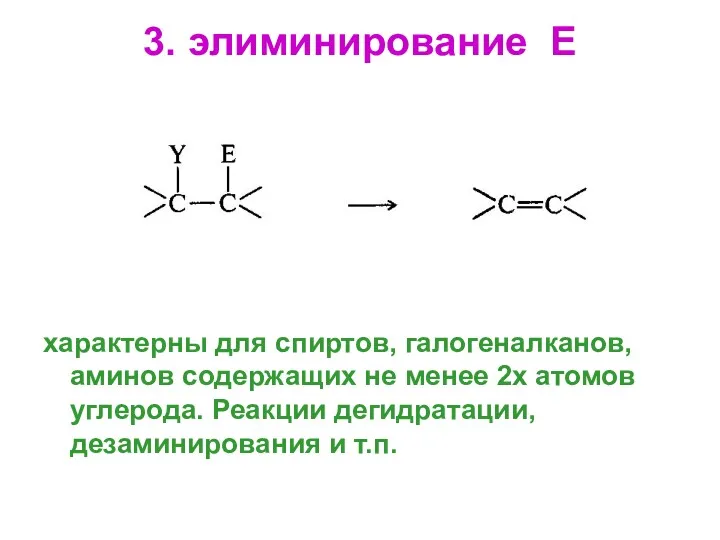
- 61. 3. элиминирование Е характерны для спиртов, галогеналканов, аминов содержащих не менее 2х атомов углерода. Реакции дегидратации,
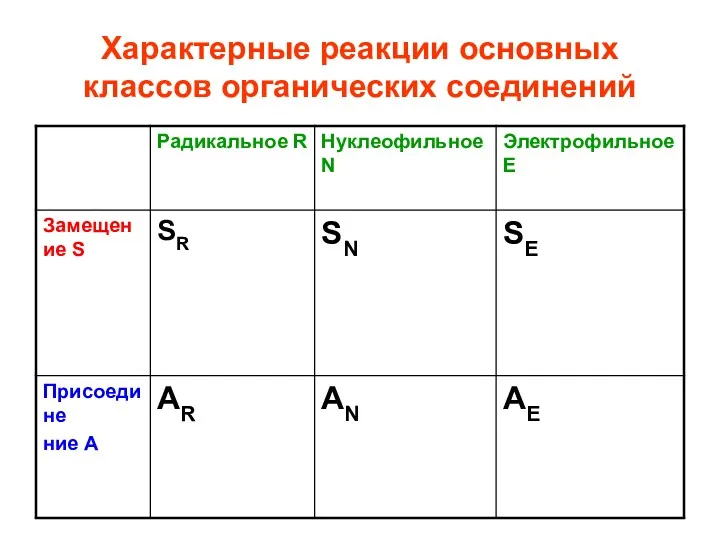
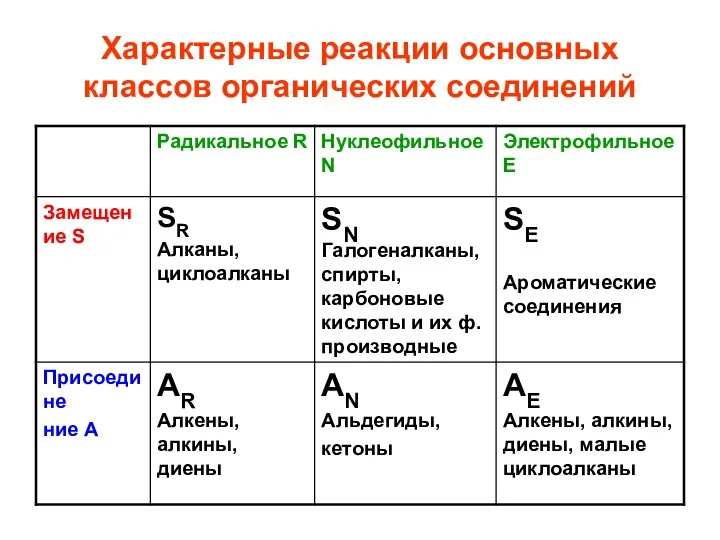
- 62. Характерные реакции основных классов органических соединений
- 63. Характерные реакции основных классов органических соединений
- 64. Электронодоноры активизируют субстрат в реакциях электрофильного замещения SE или присоединения AE Электроноакцепторы активизируют субстрат в реакциях
- 66. Скачать презентацию






















 Типы химических реакций
Типы химических реакций Мыльная история. (3 класс)
Мыльная история. (3 класс) Карбоновые кислоты. Строение, гомологический ряд, изомерия и номенклатура
Карбоновые кислоты. Строение, гомологический ряд, изомерия и номенклатура Соляная кислота и её соли
Соляная кислота и её соли Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Нұсқа талдау
Нұсқа талдау Сера и её соединения
Сера и её соединения Электролиз
Электролиз Смоги и их влияние на человека
Смоги и их влияние на человека Вплив хімічних сполук на довкілля
Вплив хімічних сполук на довкілля Положение тугоплавких металлов в Периодической системе элементов
Положение тугоплавких металлов в Периодической системе элементов Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Phosphorus
Phosphorus СВОЙСТВА ЧЕРНЫХ И ЦВЕТНЫХ МЕТАЛЛОВ.
СВОЙСТВА ЧЕРНЫХ И ЦВЕТНЫХ МЕТАЛЛОВ. Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Амінокислоти. Класифікація та номенклатура
Амінокислоти. Класифікація та номенклатура Химические свойства основных неорганических соединений в свете ЭД и ОВР
Химические свойства основных неорганических соединений в свете ЭД и ОВР Органическая химия. Жиры
Органическая химия. Жиры Химические реакторы. Лекция №10
Химические реакторы. Лекция №10 Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі
Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі Кто хочет стать отличником по химии. Игра
Кто хочет стать отличником по химии. Игра Механохимиялық активтеу әдісі. Реакция түрлері
Механохимиялық активтеу әдісі. Реакция түрлері Основные положения теории электролитической диссоциации
Основные положения теории электролитической диссоциации Алмаз. Алмаз дегеніміз не
Алмаз. Алмаз дегеніміз не Циклоалканы
Циклоалканы Зависимость свойств веществ от типа химической связи и кристаллической решетки
Зависимость свойств веществ от типа химической связи и кристаллической решетки Превращение веществ
Превращение веществ Анализ качества лекарственных средств органической природы из группы галогенпроизводных углеводородов жирного ряда
Анализ качества лекарственных средств органической природы из группы галогенпроизводных углеводородов жирного ряда