Слайд 2

Подготовили:
ученицы 9-Б класса
Дяченко Анастасия
Кокоза Карина
Слайд 3

План
Положение неметаллов в периодической системе
Особенности строения атомов неметаллов
Явление аллотропии на
примере неметаллов
Физические свойства неметаллов
Электро-отрицательность неметаллов
Неметаллы в природе
Слайд 4
Слайд 5
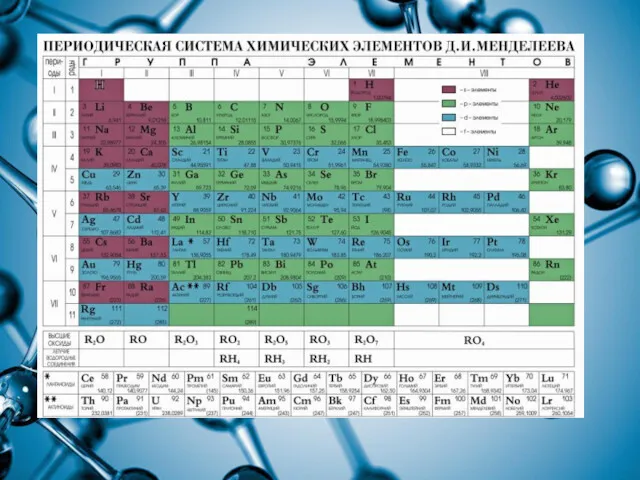
Положение неметаллов в периодической системе
Слайд 6
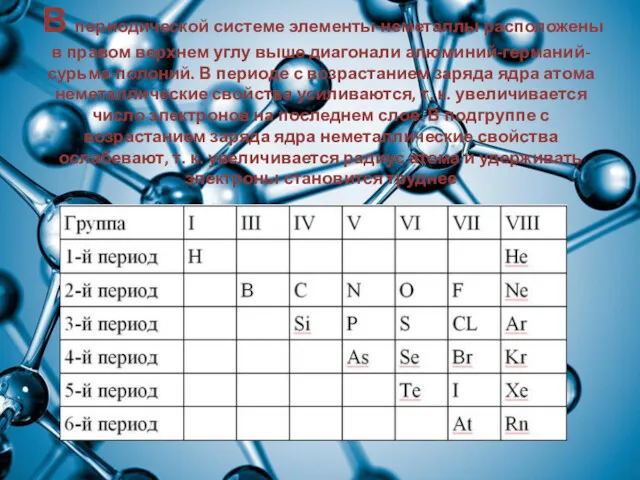
В периодической системе элементы-неметаллы расположены в правом верхнем углу выше диагонали
алюминий-германий-сурьма-полоний. В периоде с возрастанием заряда ядра атома неметаллические свойства усиливаются, т. к. увеличивается число электронов на последнем слое. В подгруппе с возрастанием заряда ядра неметаллические свойства ослабевают, т. к. увеличивается радиус атома и удерживать электроны становится труднее
Слайд 7

Особенности строения атомов неметаллов
Слайд 8

Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов
на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов. Особенно сильные окислительные свойства, т. е. способность присоединять электроны, проявляют неметаллы, находящиеся во 2-ом и 3-м периодах VI-VII групп. Если сравнить расположение электронов по орбиталям в атомах фтора, хлора и других галогенов, то можно судить и об их отличительных свойствах. У атома фтора свободных орбиталей нет. Поэтому атомы фтора могут проявить только валентность I и степень окисления ― 1.
Слайд 9

Слайд 10

Явление аллотропии на примере неметаллов
Слайд 11

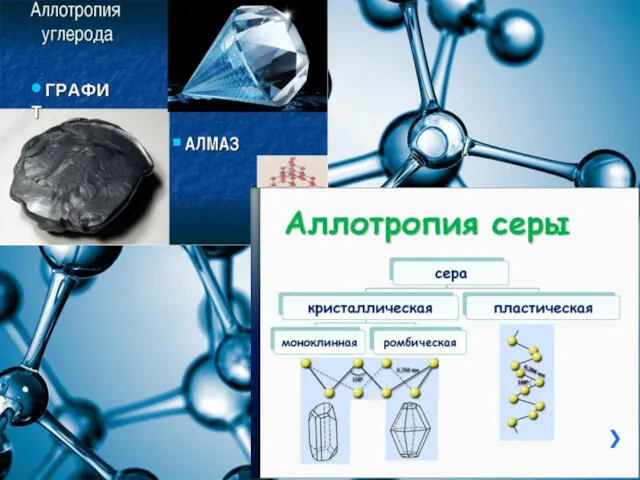
Аллотро́пия (от др.-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование двух и более
простых веществ одного и того же химического элемента, различных по строению и свойствам — так называемых аллотропных (или аллотропических) модификаций или форм.
Аллотропные модификации фосфора (белый, красный, жёлтый, чёрный фосфор)В настоящее время известно более 400 разновидностей простых веществ. Способность элемента к образованию аллотропных форм обусловлена строением атома, которое определяет тип химической связи, строение молекул и кристаллов.
Как правило, большее число аллотропных форм образуют элементы, имеющие переменные значения координационного числа или степени окисления (олово, фосфор). Другим важным фактором является катенация — способность атомов элемента образовывать гомоцепные структуры (например, сера). Склонность к аллотропии более выражена у неметаллов, за исключением галогенов и благородных газов, и полуметаллов.
Слайд 12
Слайд 13

Физические свойства неметаллов
Слайд 14

Слайд 15
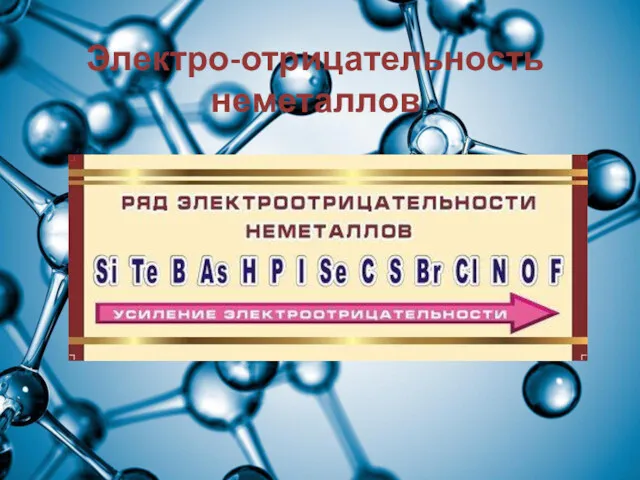
Электро-отрицательность неметаллов
Слайд 16

Электроотрицательность - способность атомов смещать в свою сторону электроны при образовании
химической связи.
Атомы неметаллов, кроме фтора, могут проявлять и положительную и отрицательную валентность.
При соединении неметалла с неметаллом менее электроотрицательный из них проявляет положительную, а более электроотрицательный – отрицательную валентность. Так, при соединении двух неметаллов, принадлежащих к одному и тому же периоду периодической системы, электроны смещаются от левого к правому, например в молекуле С4+О22- электроны смещены от атома С к атомам О, а в молекуле O2+F2- – от атома О к атомам F. При соединении двух неметаллов, принадлежащих к одной и той же группе периодической системы, электроны смещаются от нижнего к верхнему, например, в молекулах S6+O32- электроны смещены от атома серы к атомам кислорода, а в молекулах Cl3+F3- – от атомов хлора к атомам фтора.
Слайд 17
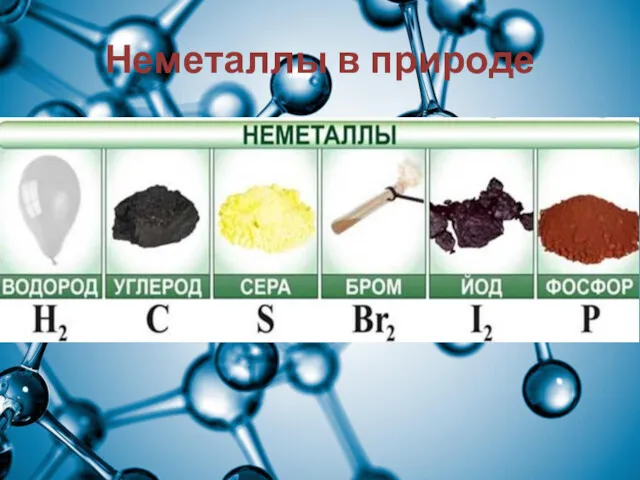
Слайд 18

Неметаллы находятся в земной коре (в большинстве своем кислород и кремний
— 76 % от массы земной коры а также As, Se, I, Te, но в очень незначительных количествах), в воздухе (азот и кислород) , в составе растительной массы (98,5 % — углерод, водород, кислород, сера, фосфор и азот), а также в основе массы человека (97,6 % — — углерод, водород, кислород, сера, фосфор и азот). Водород и гелий – входят в состав космических объектов, включая Солнце. Чаще всего в природе неметаллы встречаются в виде соединений.
Слайд 19

Слайд 20

Слайд 21





















 Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Соединения галогенов
Соединения галогенов Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Химическая связь
Химическая связь Массовая доля вещества в растворе
Массовая доля вещества в растворе Визначення іонів лужних і лужноземельних іонів у природних водах
Визначення іонів лужних і лужноземельних іонів у природних водах Уникальная соль (для дошколников)
Уникальная соль (для дошколников) Пищевые добавки
Пищевые добавки Коллигативные свойства растворов
Коллигативные свойства растворов Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7
Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7 Литий. Физические свойства лития
Литий. Физические свойства лития Типы заданий. ЕГЭ №32
Типы заданий. ЕГЭ №32 20230419_izomery
20230419_izomery Растворы и растворители
Растворы и растворители Фосфор и его соединения
Фосфор и его соединения Общая характеристика неметаллов
Общая характеристика неметаллов Простые вещества. Игра Счастливый случай
Простые вещества. Игра Счастливый случай Элемент, имеющий относительную атомную массу
Элемент, имеющий относительную атомную массу Введение в аналитическую химию. Введение в качественный анализ
Введение в аналитическую химию. Введение в качественный анализ Алканы. Гомологи
Алканы. Гомологи Методы разделения и исследования состава нефти и газа
Методы разделения и исследования состава нефти и газа Формальная кинетика. Предмет химической кинетики
Формальная кинетика. Предмет химической кинетики Хром. Элемент под № 24
Хром. Элемент под № 24 Аммиак. Состав вещества
Аммиак. Состав вещества Галогены. Фтор, хлор, бром, йод, астат
Галогены. Фтор, хлор, бром, йод, астат Породообразующие минералы
Породообразующие минералы Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Взрывоопасные грузы
Взрывоопасные грузы