Конкретные цели:
Трактовать общие требования ГФУ к качеству лекарственных средств, которые
количественно определяются методом комплексонометрии, лекарственных средств производных ртути и серебра.
Изучить методы анализа лекарственных средств, которые количественно определяются методом комплексонометрии, лекарственных средств производных ртути и серебра.
Использовать химические методы анализа лекарственных средств неорганической природы и оценить качество исследуемых субстанций.
Объяснять особенности хранения лекарственных средств, которые количественно определяются методом комплексонометрии, а также лекарственных средств производных ртути и серебра.
Предложить и объяснить физические и физико-химические методы анализа органических соединений.
Усвоить свойства лекарственных и парфюмерно-косметических средств алифатической структуры (галогенпроизводные алифатических углеводородов, производные спиртов и альдегидов, карбоновых кислот и их солей, аминокислот, простых и сложных эфиров, ароматических соединений).
Предложить методы получения органических лекарственных и парфюмерно-косметических средств.
Объяснять особенности методов анализа лекарственных и парфюмерно-косметических средств алифатической, ароматической структуры.
Использовать химические методы анализа органических лекарственных и парфюмерно-косметических средств алифатической, ароматической структуры, оценить качество исследуемых субстанций.
Объяснять особенности хранения лекарственных и парфюмерно-косметических средств органической структуры.
Организация контроля качества парфюмерно-косметических и лекарственных средств в Украине. Государственные стандарты, отраслевые стандарты и технические условия. Государственная фармакопея Украины. Общие методы анализа, которые используются для характеристики качества лекарственных и парфюмерно-косметических средств. Анализ качества лекарственных и парфюмерно-косметических средств неорганической и органической структуры











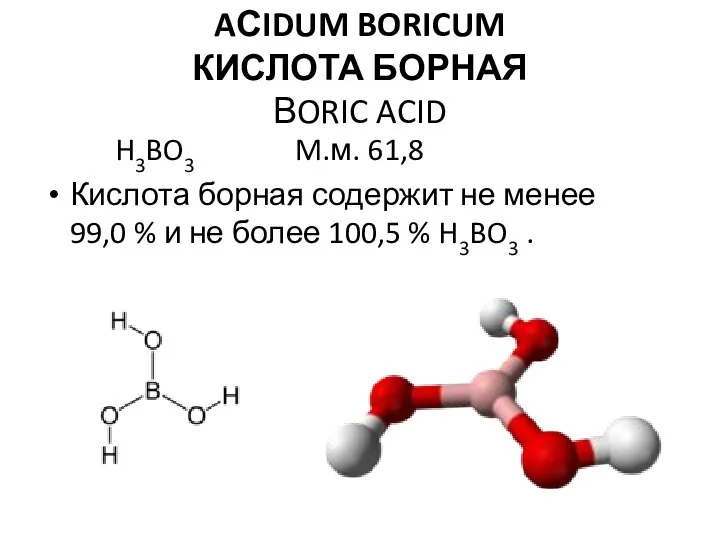

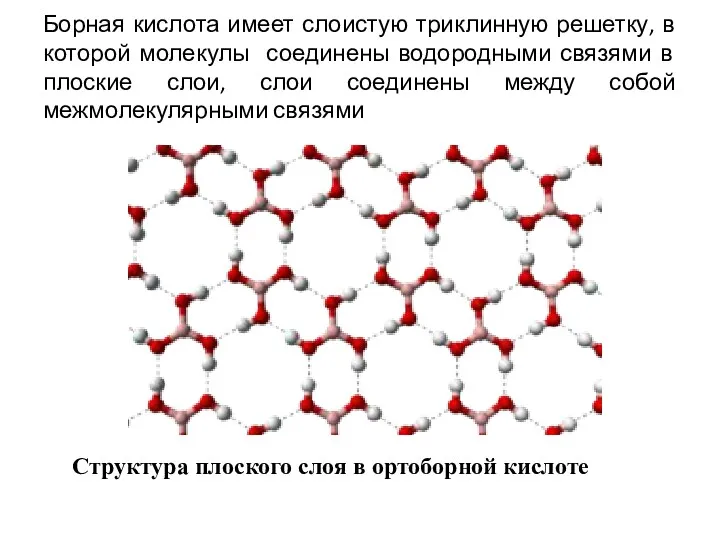

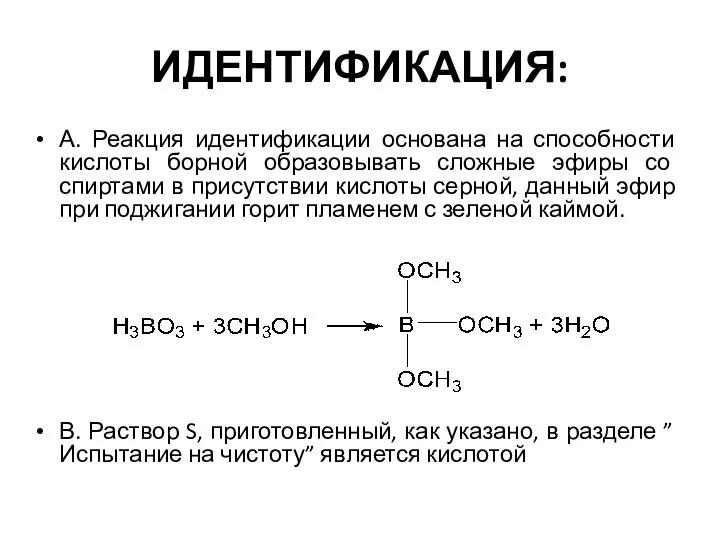

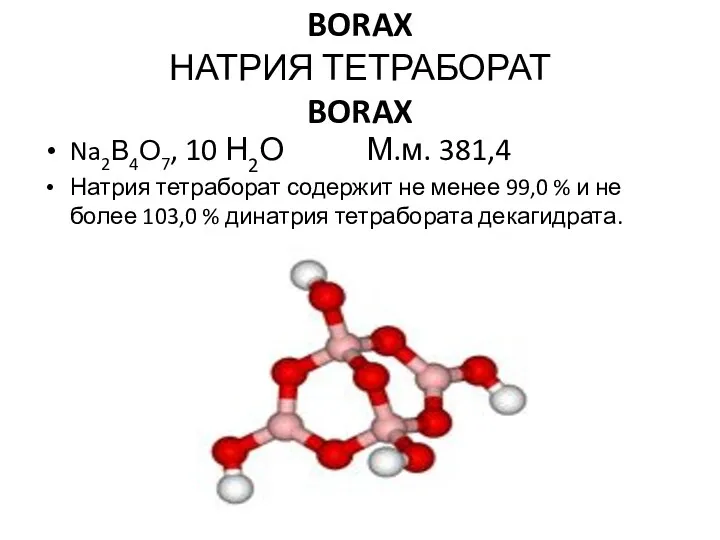

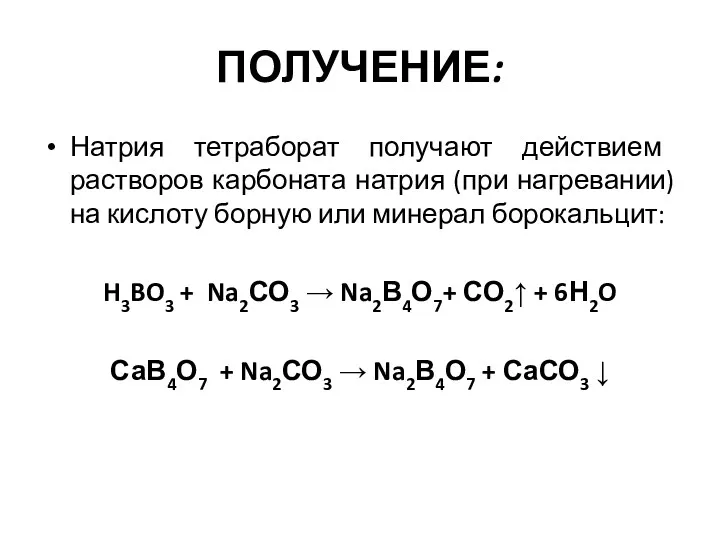




 Sulfur and its compounds. Contact method for producing sulfuric acid
Sulfur and its compounds. Contact method for producing sulfuric acid Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов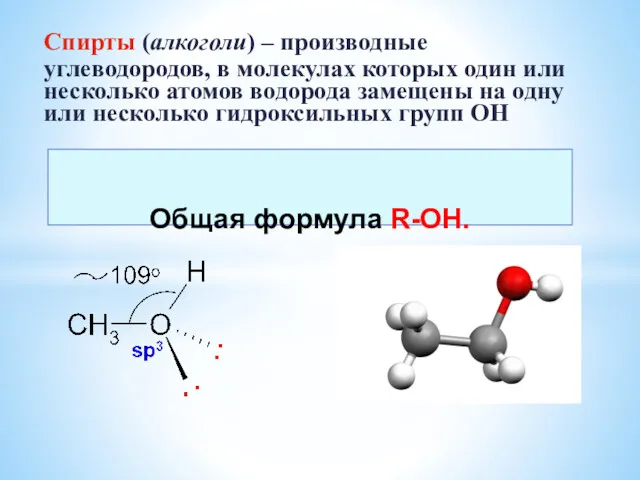 Спирты. Многоатомные спирты
Спирты. Многоатомные спирты Соли. Определение солей
Соли. Определение солей The role of chemistry in the solution of the food problem
The role of chemistry in the solution of the food problem Адсорбция. Физическая и химическая адсорбция
Адсорбция. Физическая и химическая адсорбция Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Стекловолокно. Что такое стекловолокно?
Стекловолокно. Что такое стекловолокно? Три правила взаимодействия элементов симметрии
Три правила взаимодействия элементов симметрии Простые и сложные полиэфиры. Пентапласт
Простые и сложные полиэфиры. Пентапласт Вольфрам — химический элемент
Вольфрам — химический элемент Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Совйства спиртов. 10 класс
Совйства спиртов. 10 класс Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Растворы. Процесс растворения
Растворы. Процесс растворения Сульфиды. Лекция 6
Сульфиды. Лекция 6 Термопластичные полимеры
Термопластичные полимеры Состав, свойства и роль молока в жизни человека
Состав, свойства и роль молока в жизни человека Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Биологически важные окислительно-восстановительные реакции органических соединений
Биологически важные окислительно-восстановительные реакции органических соединений Непредельные углеводороды. Алкены. Номенклатура алкенов
Непредельные углеводороды. Алкены. Номенклатура алкенов Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла Карбоновые кислоты. 10 класс
Карбоновые кислоты. 10 класс Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття
Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття Азотные удобрения
Азотные удобрения Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль