Содержание
- 2. ПРОВЕРОЧНЫЙ ТЕСТ Задание : подбери соответствие. 1.Аргентум 2.Аурум 3.Гидраргирум 4.Силициум 5.Натрий 6.Плюмбум 7.Фосфор 8.Кальций 9.Купрум 10.Феррум
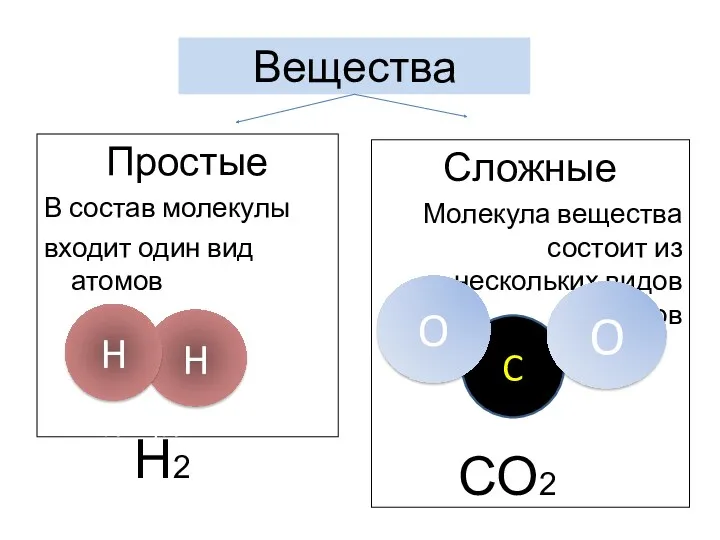
- 3. Вещества Простые В состав молекулы входит один вид атомов в состав молекулы веществв состав молекулы вD
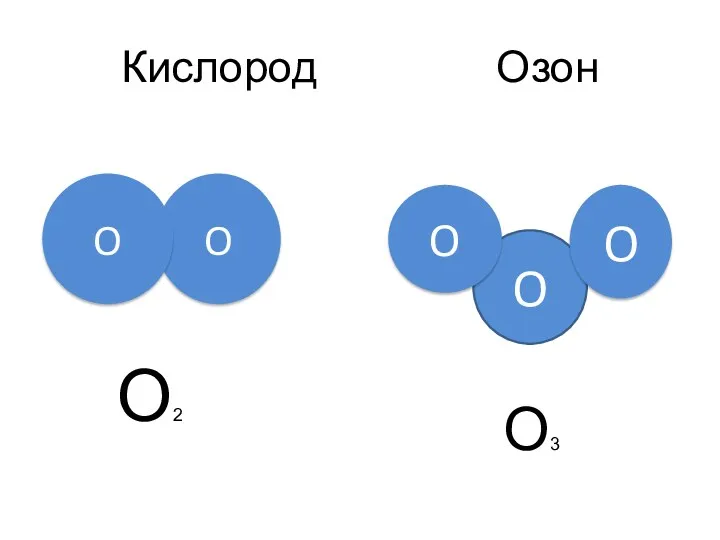
- 4. O O O O O Кислород Озон O2 O3
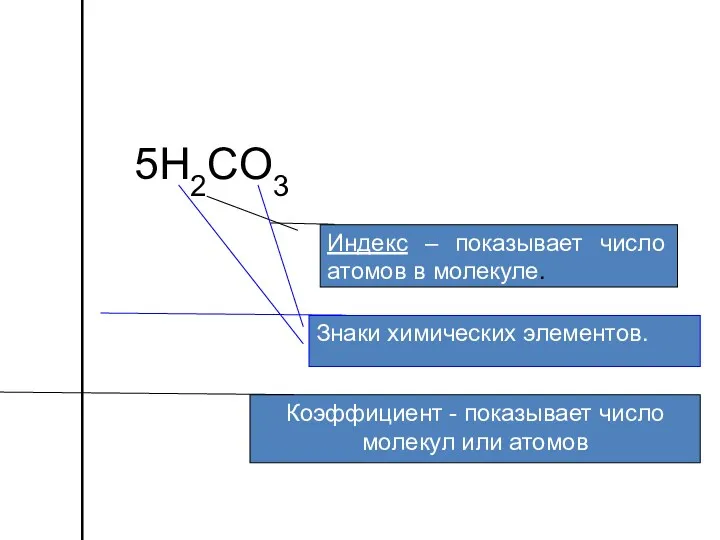
- 5. 5H2СO3 Коэффициент - показывает число молекул или атомов Индекс – показывает число атомов в молекуле. Знаки
- 6. Химическая формула – это условная запись состава вещества, посредствам химических знаков и символов.
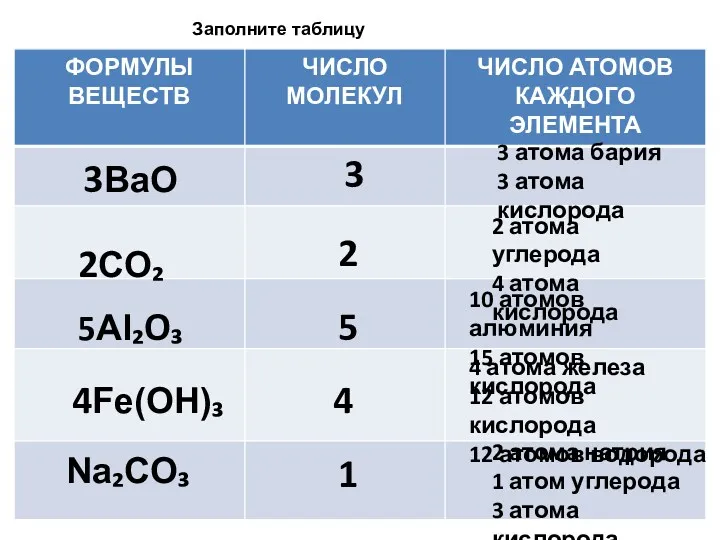
- 7. 3BaO 2CO₂ 5Al₂O₃ 4Fe(OH)₃ Na₂CO₃ 3 2 5 4 1 2 атома натрия 1 атом углерода
- 8. Относительная масса атома mат (Н) = 0,000 000 000 000 000 000 000 001674 г =
- 9. mат (Н) = 0,000 000 000 000 000 000 000 001674 г = 0,1674∙10-23 г mат
- 10. II. Нахождение Ar с помощью периодической системы. Правила округления: - если после запятой стоит цифра меньше
- 11. ОТНОСИТЕЛЬНАЯ МОЛЕКУЛЯРНАЯ МАССА Мr(Н2О) = 2∙Ar(H) + A r(O) = 2∙1 + 16 = 18 Мr(Н2SО4)
- 12. Тема урока: «Химические формулы. Относительная молекулярная масса»
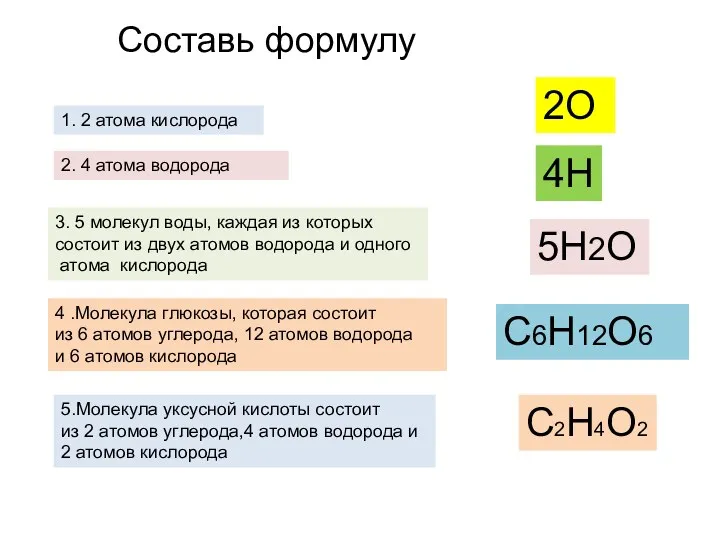
- 13. 3. 5 молекул воды, каждая из которых состоит из двух атомов водорода и одного атома кислорода
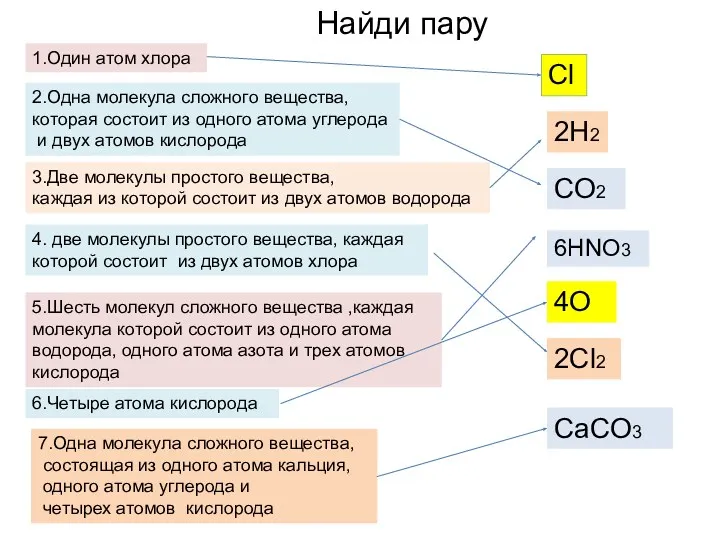
- 14. 1.Один атом хлора 2.Одна молекула сложного вещества, которая состоит из одного атома углерода и двух атомов
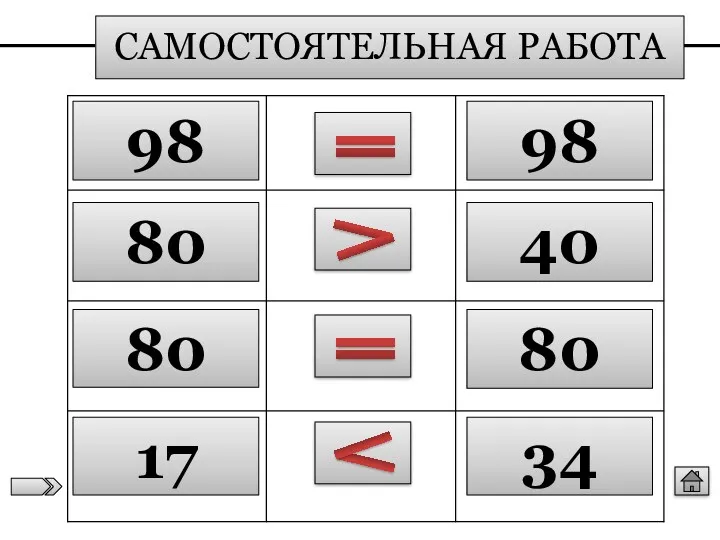
- 15. САМОСТОЯТЕЛЬНАЯ РАБОТА 98 98 80 40 80 80 17 34
- 16. Домашнее задание 1.Прочитать § 9, 10 2.Найти относительную молекулярную массу молекулы белка молока: Мr ( C1864H3031O576N468S26)-?
- 18. Скачать презентацию








 Ертінділер. Ерітінді концентрациясын білдіру тәсілдері
Ертінділер. Ерітінді концентрациясын білдіру тәсілдері Жиры
Жиры Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль Кислоты, содержащие серу (S)
Кислоты, содержащие серу (S) Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях ОВР в органической химии
ОВР в органической химии Классификация и свойства оксидов
Классификация и свойства оксидов Лекция Атомное строение твердых тел. 1-01
Лекция Атомное строение твердых тел. 1-01 Классификация химических реакций
Классификация химических реакций Презентация по химии _Классификация веществ_ 11 класс
Презентация по химии _Классификация веществ_ 11 класс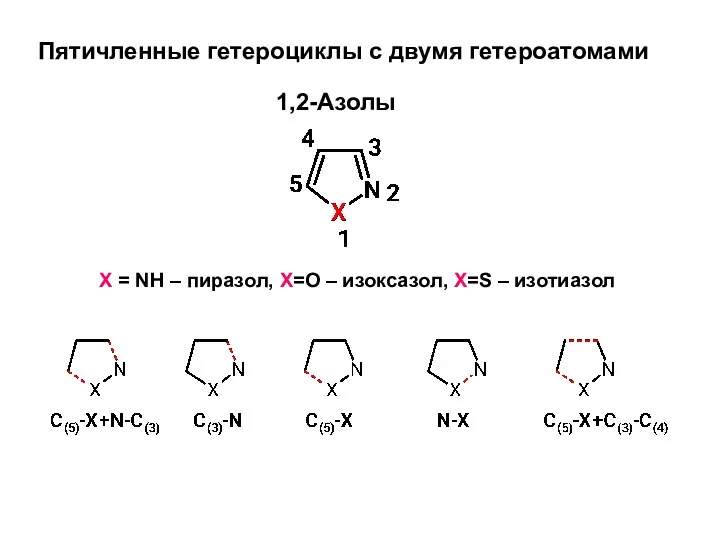 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами Physiology lab
Physiology lab Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов
Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов Периодическая система химических элементов. Знаки химических элементов
Периодическая система химических элементов. Знаки химических элементов Природный газ
Природный газ Застосування арт-терапевтичних технік на уроках хімії
Застосування арт-терапевтичних технік на уроках хімії Нефть и ее роль в мировой экономике
Нефть и ее роль в мировой экономике Циклические углеводороды. Циклоалканы
Циклические углеводороды. Циклоалканы Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Швидкість хімічної реакції
Швидкість хімічної реакції Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Новые катализаторы
Новые катализаторы Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Металлы. Общая характеристика
Металлы. Общая характеристика Кремний и его соединения для 11 класса
Кремний и его соединения для 11 класса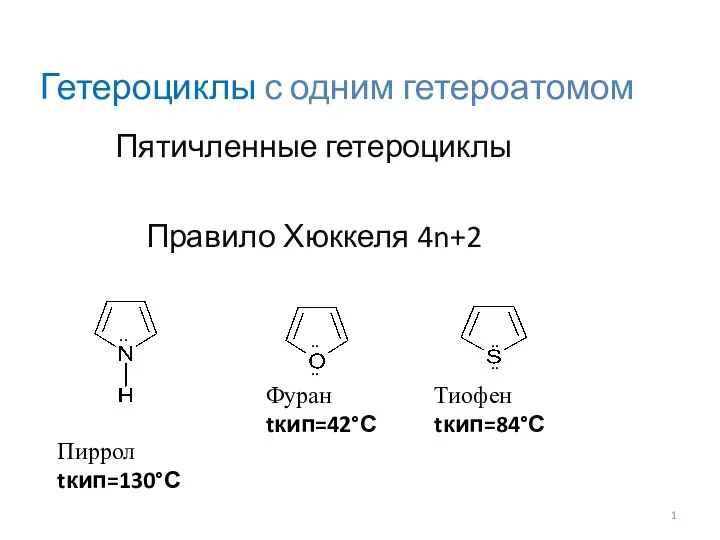 Гетероциклы с одним гетероатомом
Гетероциклы с одним гетероатомом Химический элемент, минерал, горная порода. (Лекция 6)
Химический элемент, минерал, горная порода. (Лекция 6) Химиялық тепе-теңдік
Химиялық тепе-теңдік