Содержание
- 2. Цели урока Обобщить знания учащихся о классах неорганических и органических соединений. Продолжить формирование умений сравнивать, анализировать,
- 3. Самая простая классификкация вешеств заключается в том, что все известные вещества делят на неорганические и органические.
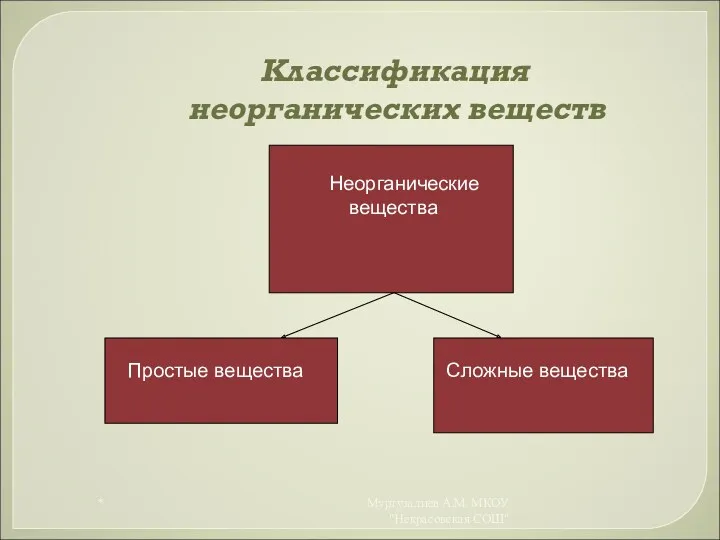
- 4. Классификация неорганических веществ Неорганические вещества Простые вещества Сложные вещества * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
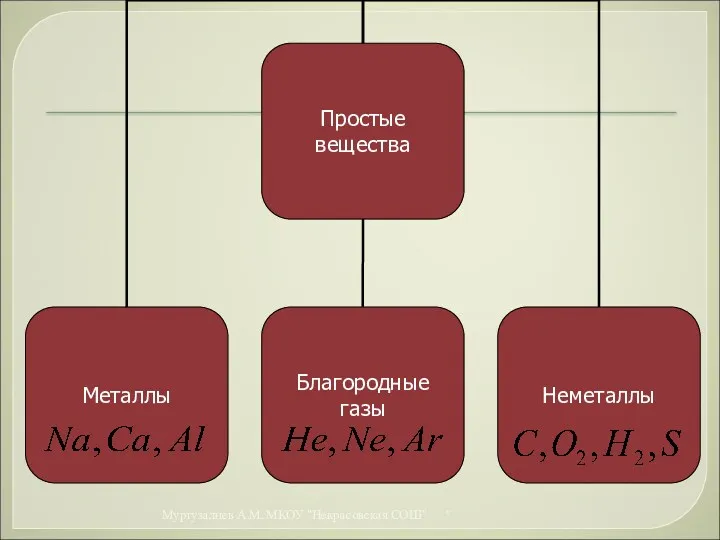
- 5. Простые вещества состоят из атомов одного химического элемента и подразделяются на металлы, неметаллы и благородные (инертные)
- 6. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 7. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
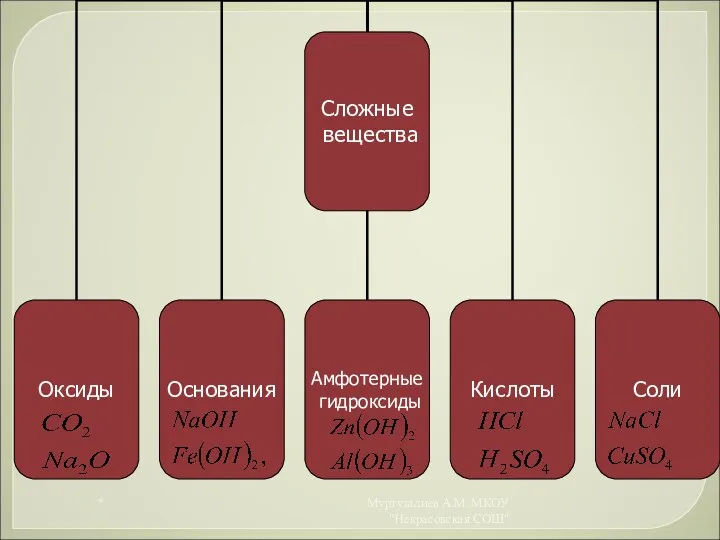
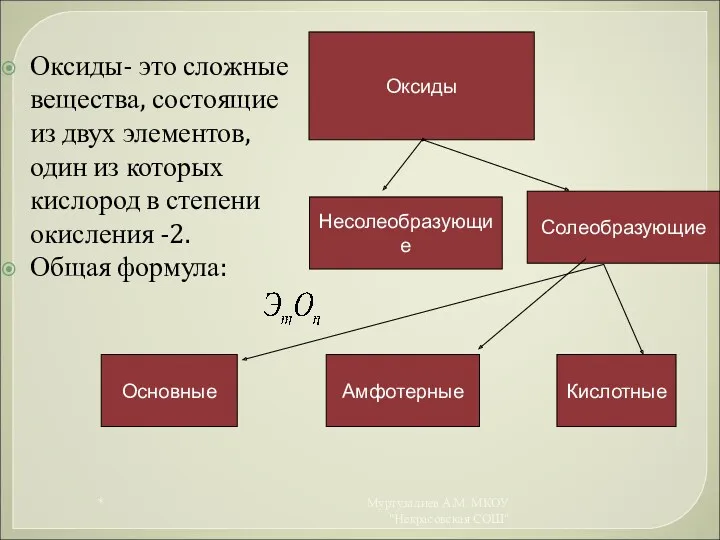
- 8. Оксиды- это сложные вещества, состоящие из двух элементов, один из которых кислород в степени окисления -2.
- 9. Оксиды ЭаОс - ? * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
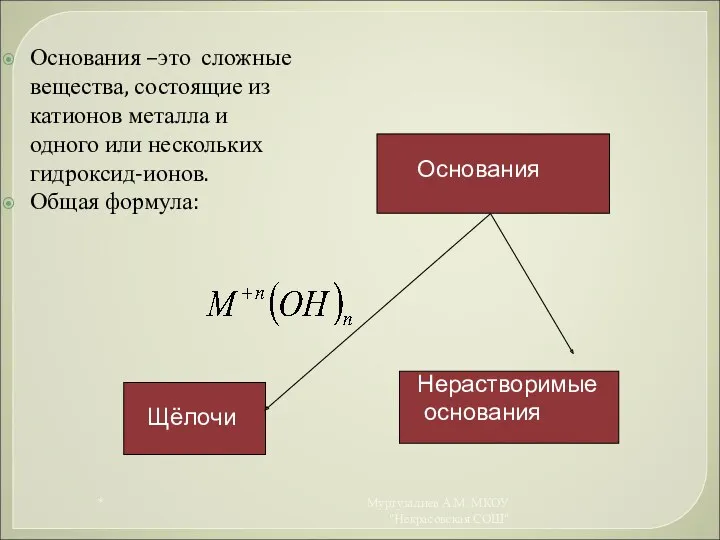
- 10. Основания –это сложные вещества, состоящие из катионов металла и одного или нескольких гидроксид-ионов. Общая формула: Основания
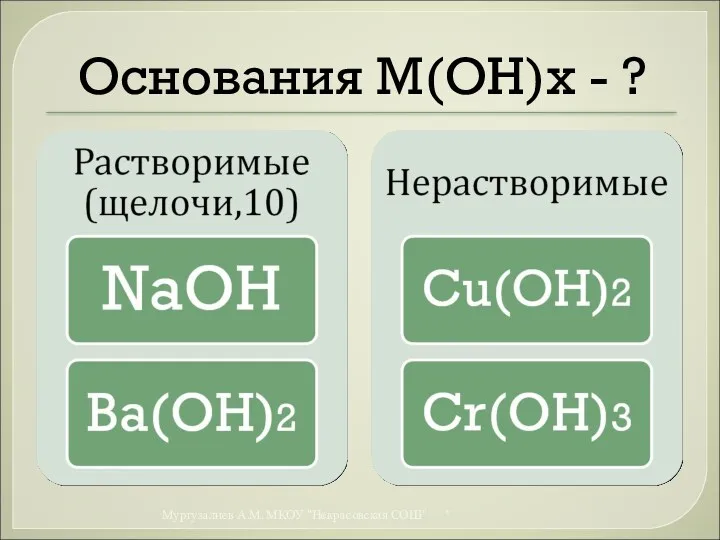
- 11. Основания М(ОН)x - ? * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 12. Амфотерные гидроксиды проявляют и свойства кислот и оснований, поэтому можно записывать в двух видах: Zn(OH)2 или
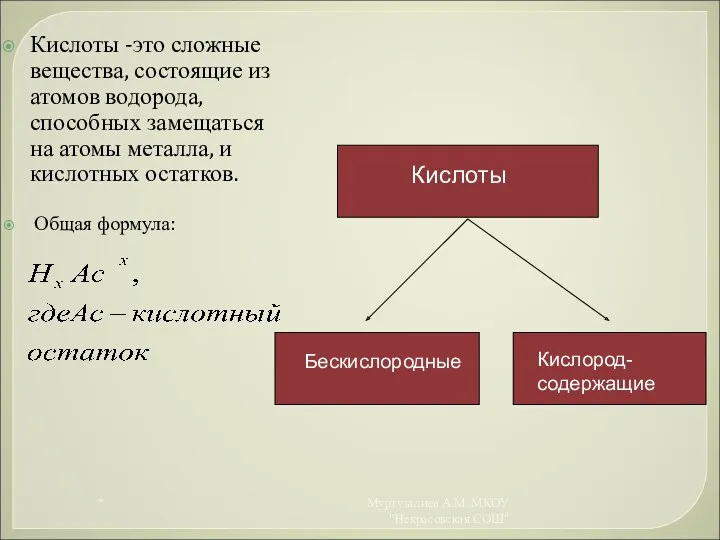
- 13. Кислоты -это сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металла, и кислотных остатков.
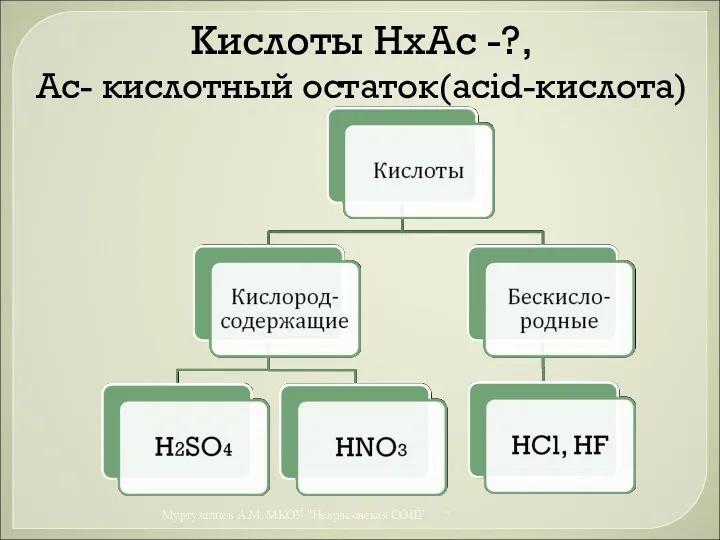
- 14. Кислоты НxАс -?, Ас- кислотный остаток(acid-кислота) * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
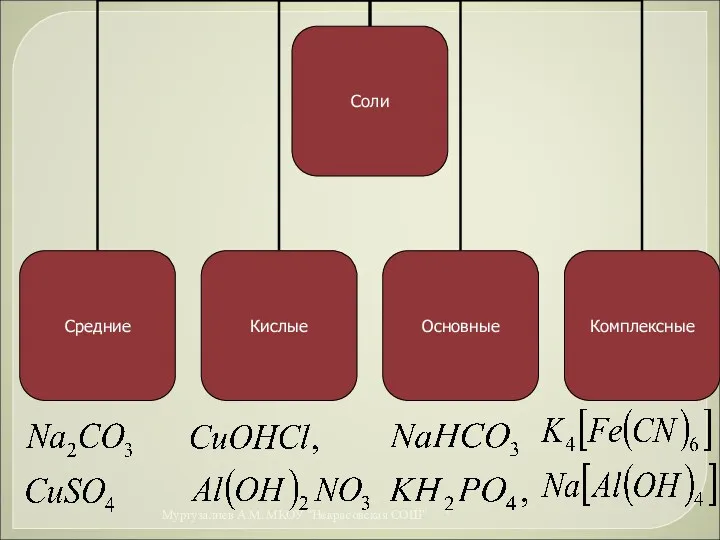
- 15. Соли Средние соли- это сложные вещества, состоящие из катионов металла и анионов кислотных остатков. Средние соли
- 16. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
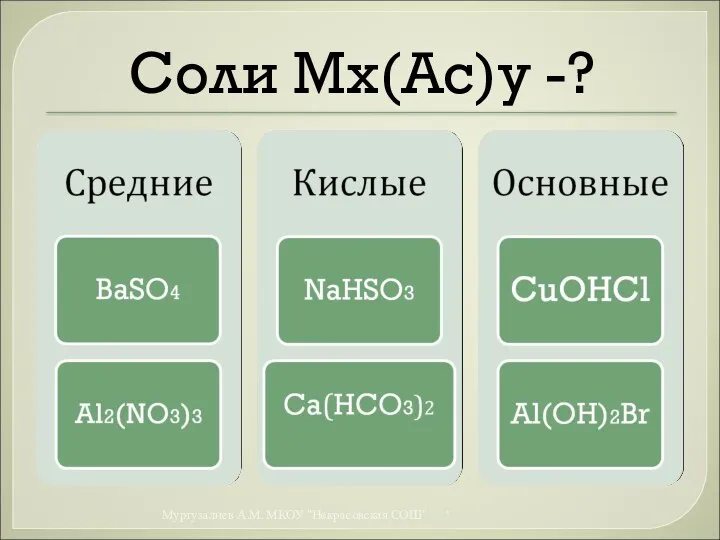
- 17. Соли Мx(Ас)y -? * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
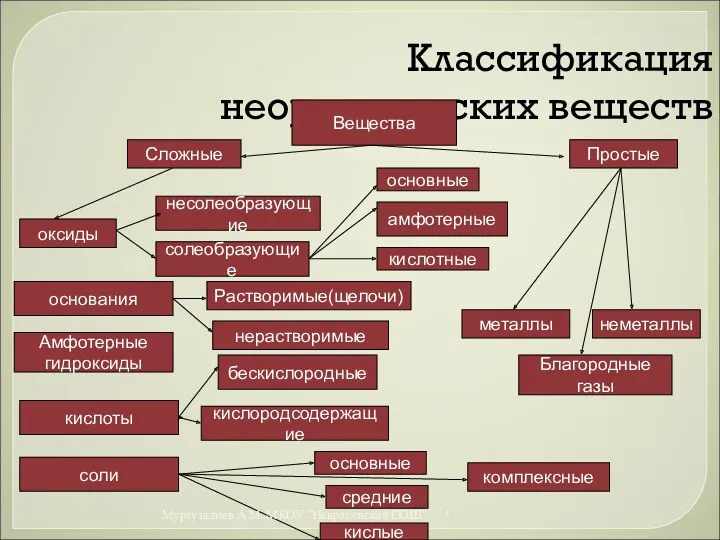
- 18. Классификация неорганических веществ Вещества Сложные Простые Благородные газы металлы неметаллы Амфотерные гидроксиды соли основания оксиды кислоты
- 19. Классификация органических веществ * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
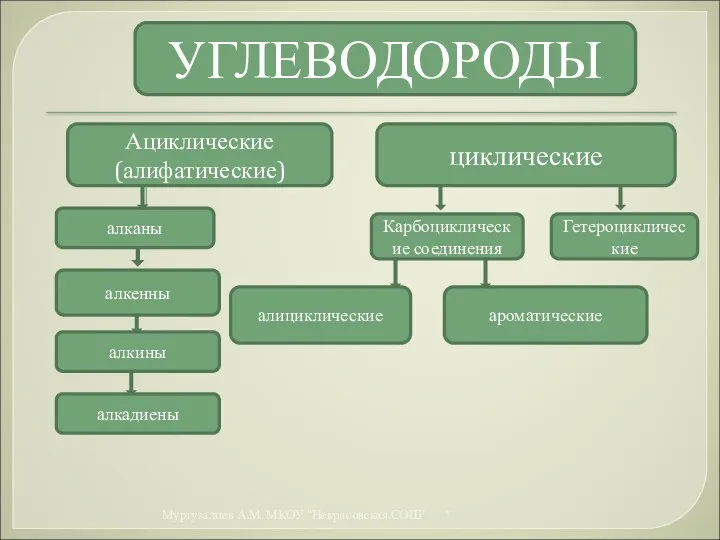
- 20. УГЛЕВОДОРОДЫ Ациклические (алифатические) циклические Карбоциклические соединения Гетероциклические алициклические ароматические алканы алкенны алкины алкадиены * Муртузалиев А.М.
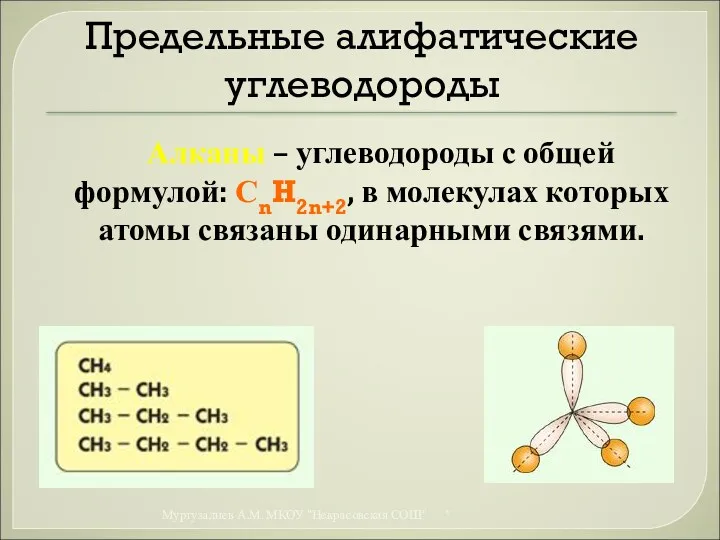
- 21. Предельные алифатические углеводороды Алканы – углеводороды с общей формулой: СnH2n+2, в молекулах которых атомы связаны одинарными
- 22. Непредельные алициклические углеводороды Алкены (этиленовые углеводороды, олефины) – непредельные алифатические углеводороды, молекулы которых содержат двойную связь.
- 23. Алкадиены – это соединения с двумя двойными связями. Общая формула алкадиенов - СnН2n-2, причем n>3. СН2=СН–СН=СН2
- 24. Алкины – непредельные углеводороды с общей формулой CnH2n-2 . В их молекулах одна тройная связь между
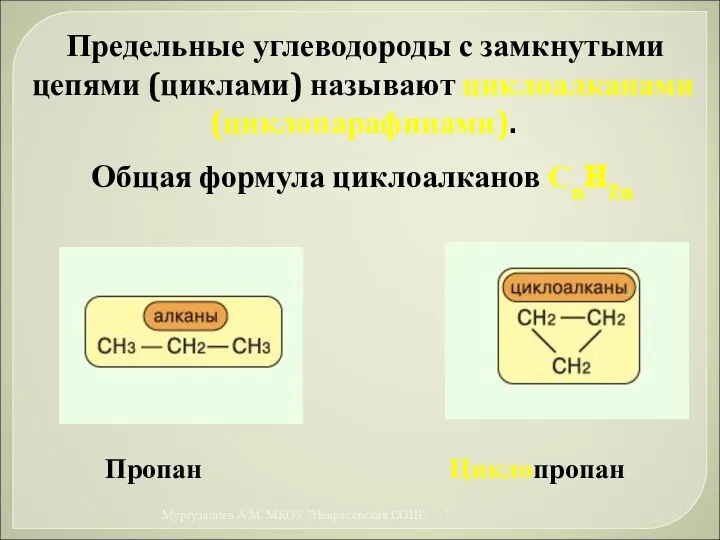
- 25. Предельные углеводороды с замкнутыми цепями (циклами) называют циклоалканами (циклопарафинами). Общая формула циклоалканов СnH2n Пропан Циклопропан *
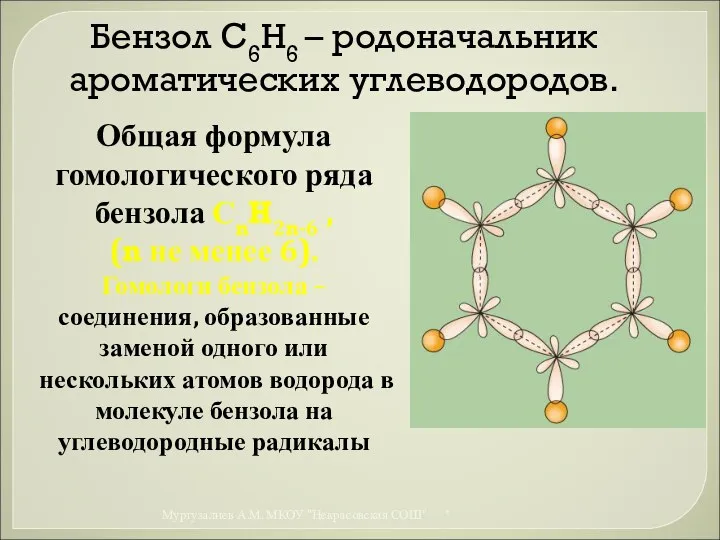
- 26. Бензол С6Н6 – родоначальник ароматических углеводородов. Общая формула гомологического ряда бензола СnH2n-6 , (n не менее
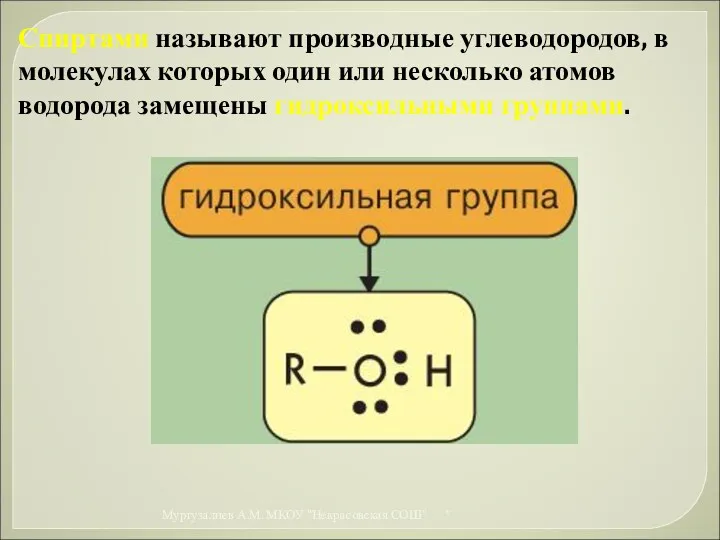
- 27. Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами. *
- 28. По числу гидроксильных групп спирты подразделяются на одноатомные (одна группа -ОН) и многоатомные (две и более
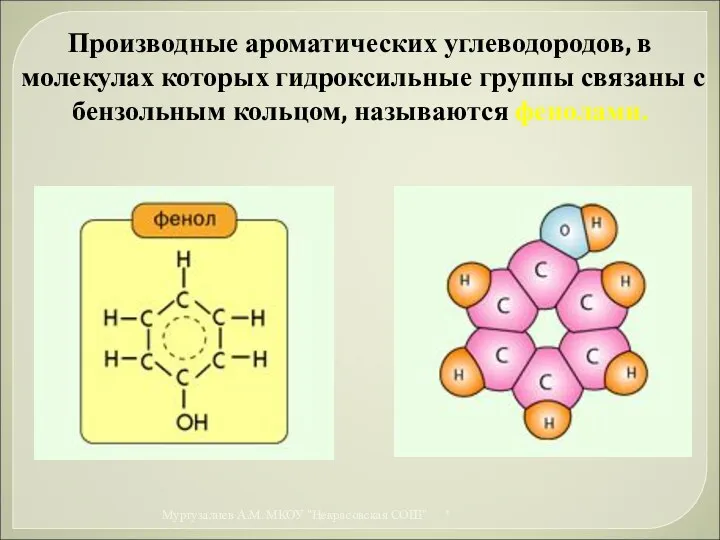
- 29. Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным кольцом, называются фенолами. * Муртузалиев
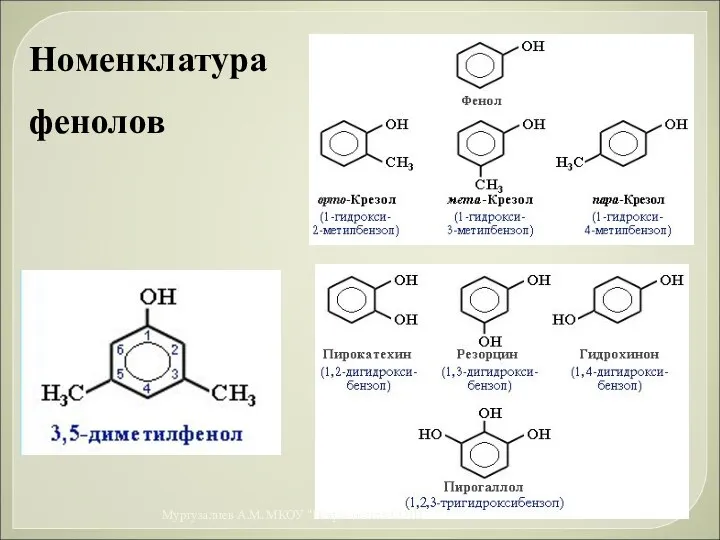
- 30. Номенклатура фенолов * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
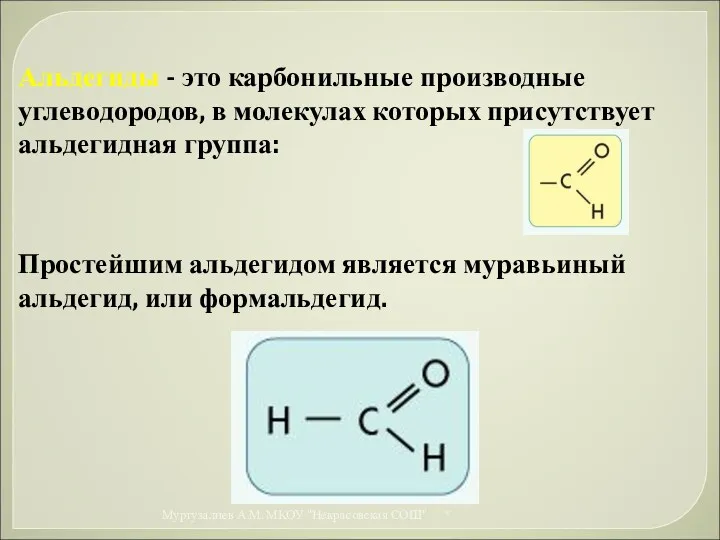
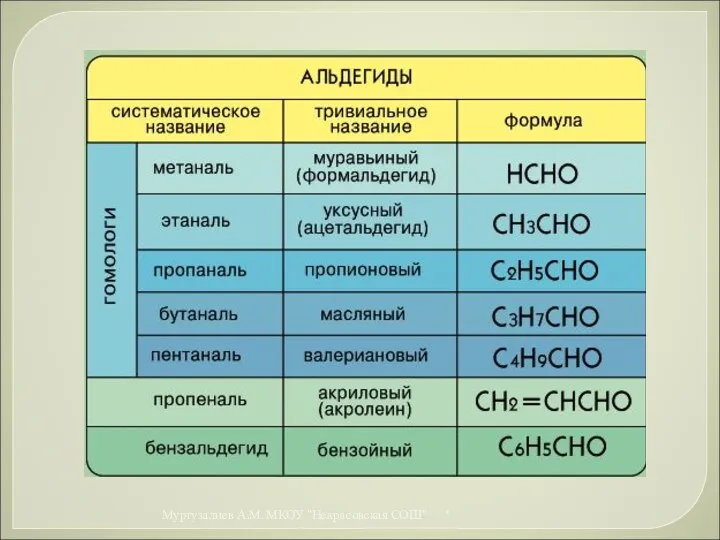
- 31. Альдегиды - это карбонильные производные углеводородов, в молекулах которых присутствует альдегидная группа: Простейшим альдегидом является муравьиный
- 32. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
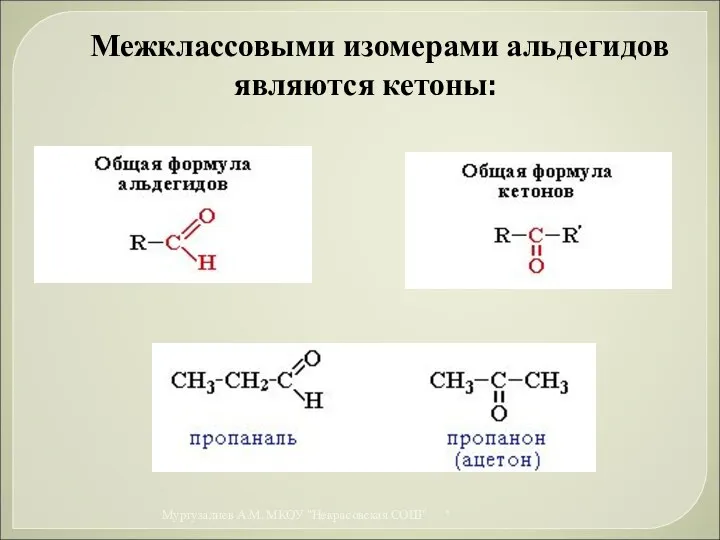
- 33. Межклассовыми изомерами альдегидов являются кетоны: * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 34. Карбоновые кислоты – это сложные органические вещества, в которых углеводородный радикал соединён с одной или несколькими
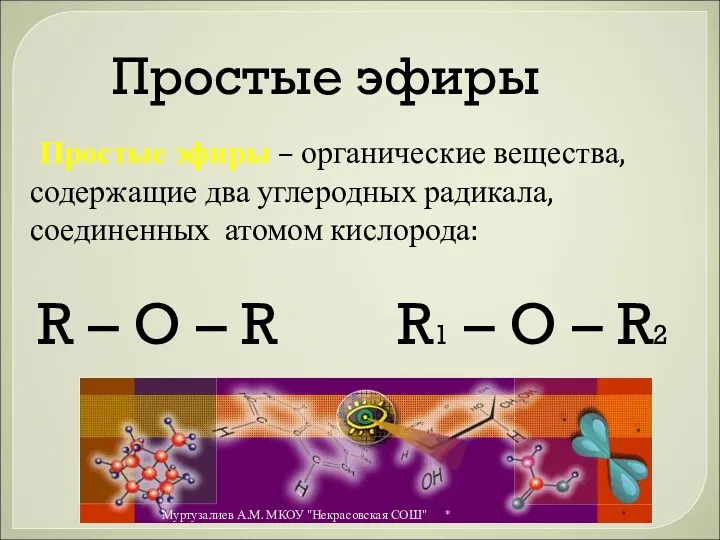
- 35. Простые эфиры Простые эфиры – органические вещества, содержащие два углеродных радикала, соединенных атомом кислорода: R –
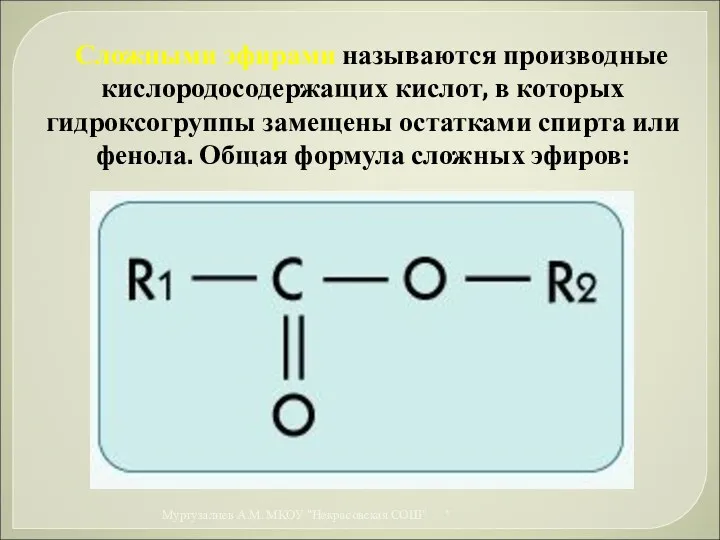
- 36. Сложными эфирами называются производные кислородосодержащих кислот, в которых гидроксогруппы замещены остатками спирта или фенола. Общая формула
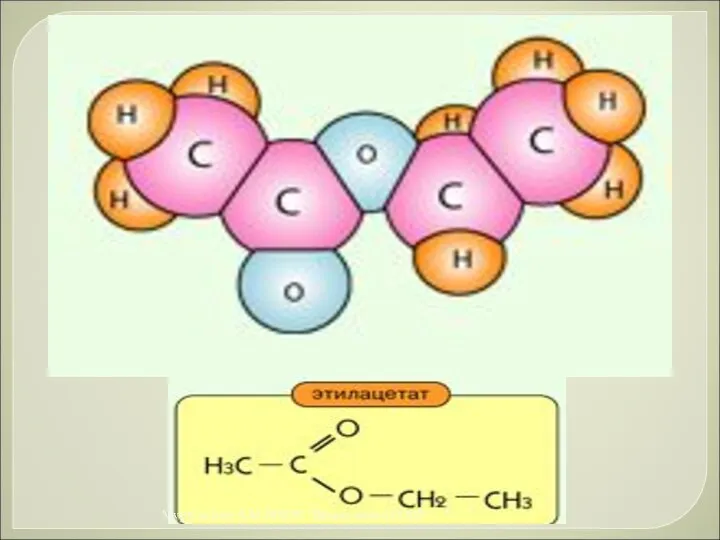
- 37. Свойства эфиров Сложные эфиры представляют собой легковоспламеняющиеся жидкости с невысокими температурами кипения. Сложные эфиры широко распространены
- 38. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
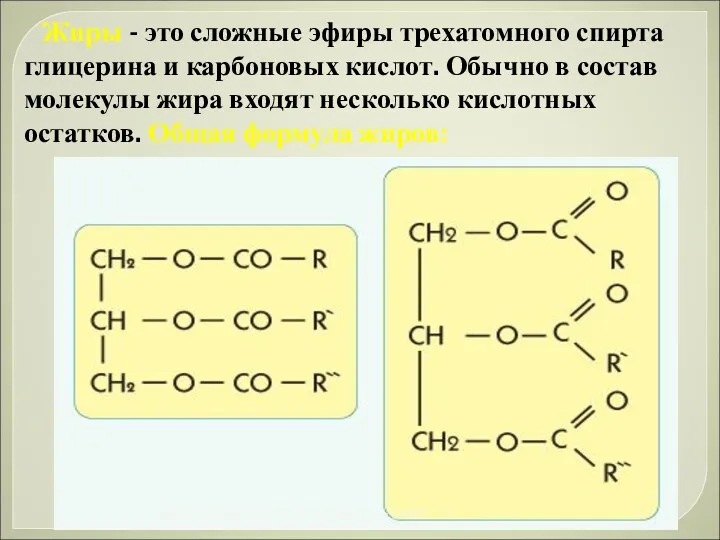
- 39. Жиры - это сложные эфиры трехатомного спирта глицерина и карбоновых кислот. Обычно в состав молекулы жира
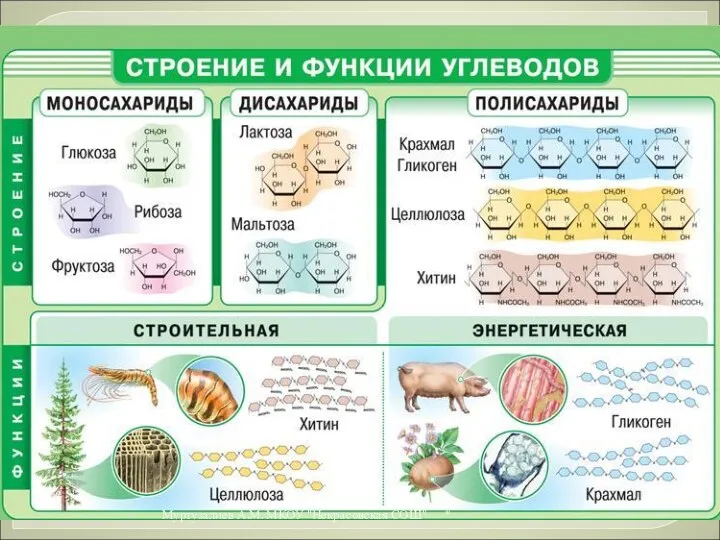
- 40. Углеводы (сахара) - органические вещества, состав которых выражается формулой Cx(H2O)y, где x и y > 3.
- 41. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 42. Азотсодержащие соединения * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 43. Амины – это производные аммиака, в молекуле которого один, два или три атома водорода замещены на
- 44. Номенклатура аминов * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
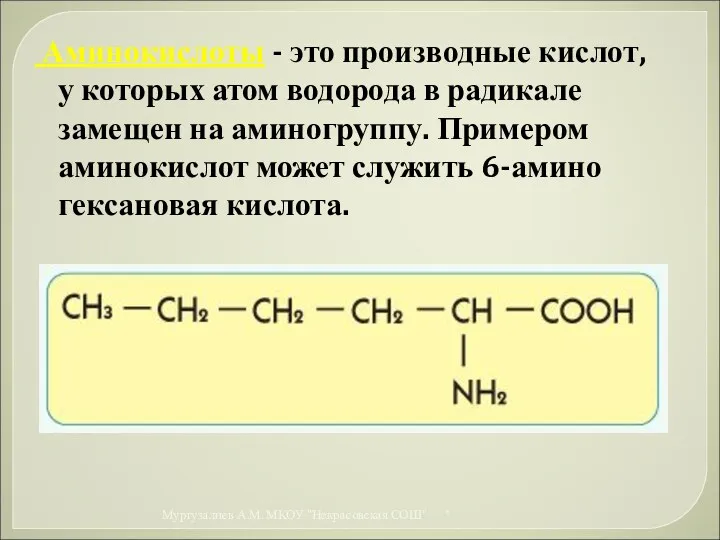
- 45. Аминокислоты - это производные кислот, у которых атом водорода в радикале замещен на аминогруппу. Примером аминокислот
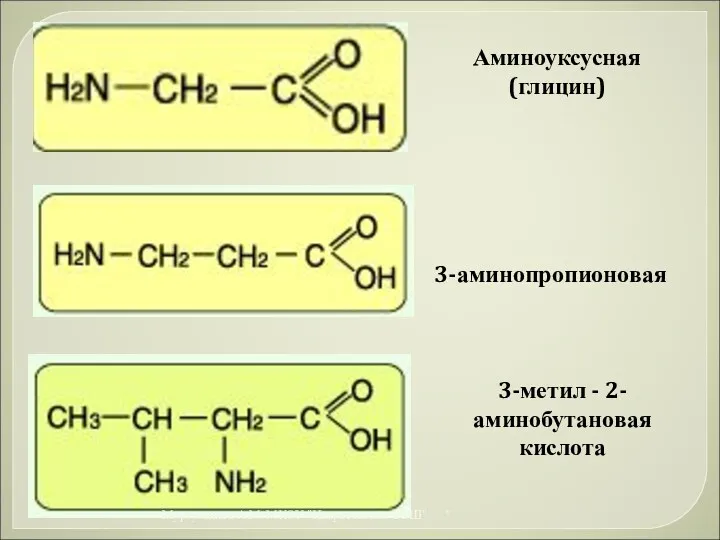
- 46. Аминоуксусная (глицин) 3-аминопропионовая 3-метил - 2-аминобутановая кислота * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
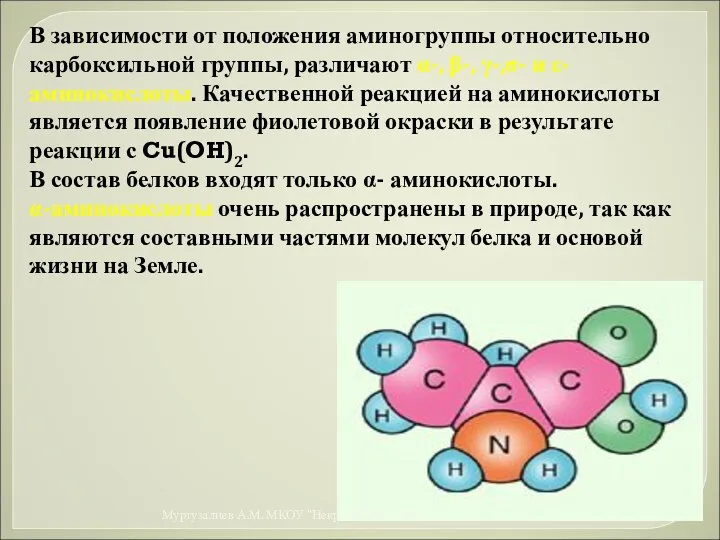
- 47. В зависимости от положения аминогруппы относительно карбоксильной группы, различают α-, β-, γ-,σ- и ε-аминокислоты. Качественной реакцией
- 48. Белки (полипептиды) − биополимеры, построенные из остатков α-аминокислот, соединенных пептидными связями. Пептидной связью называют амидную связь
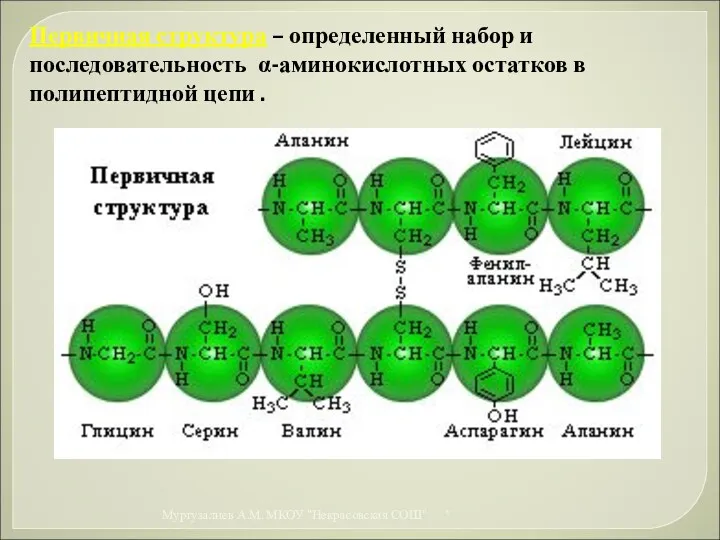
- 49. Первичная структура – определенный набор и последовательность α-аминокислотных остатков в полипептидной цепи . * Муртузалиев А.М.
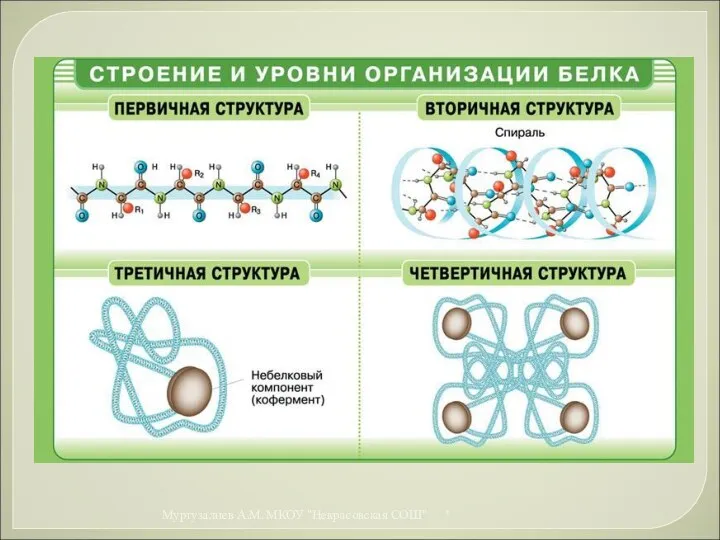
- 50. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 51. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 52. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
- 53. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
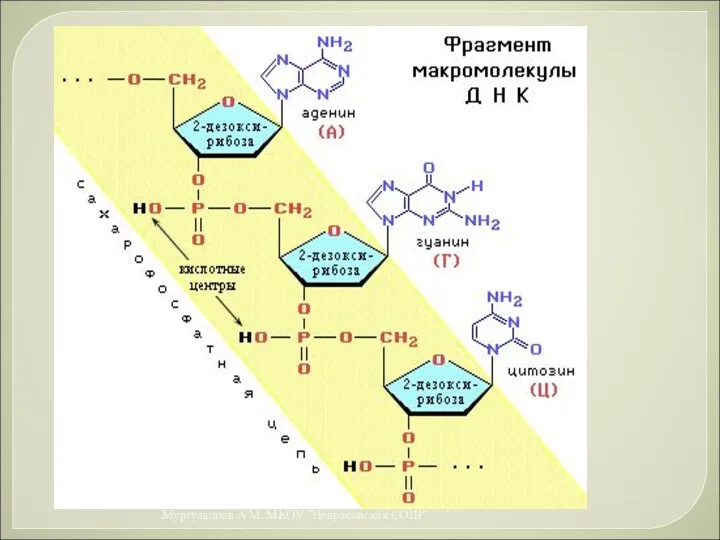
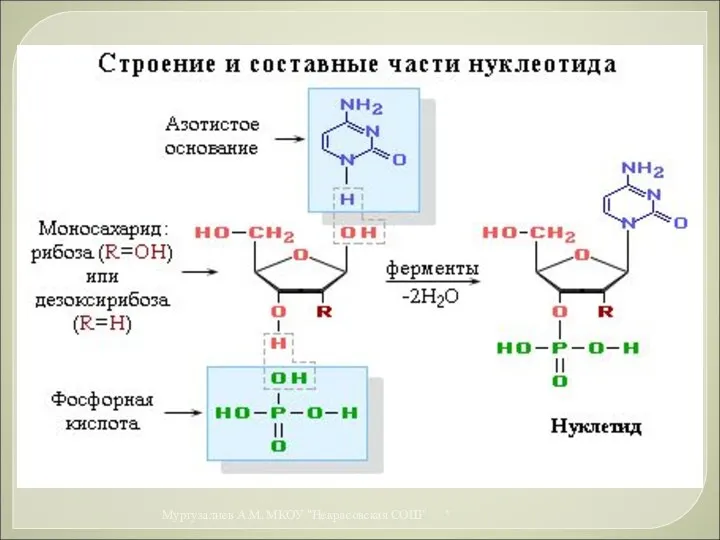
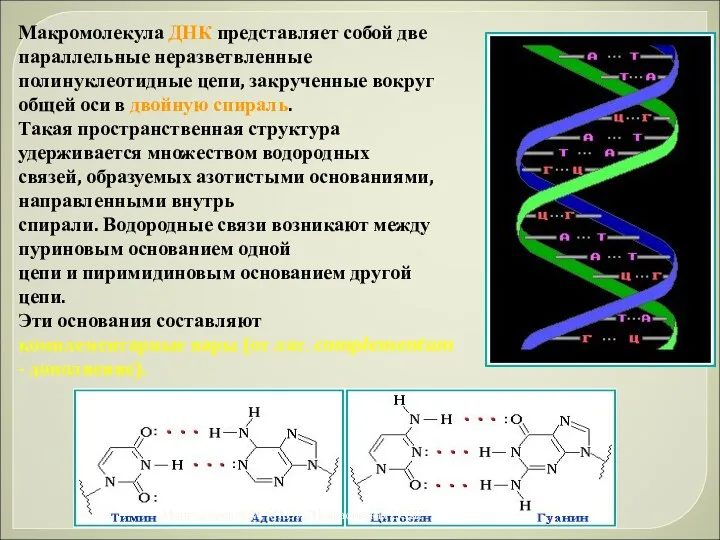
- 54. Макромолекула ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг общей оси в двойную спираль.
- 55. * Муртузалиев А.М. МКОУ "Некрасовская СОШ"
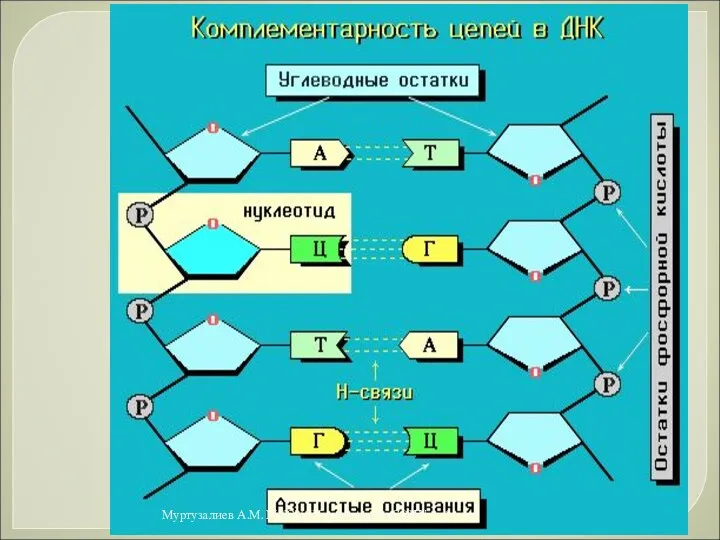
- 56. Способность ДНК не только хранить, но и использовать генетическую информацию определяется следующими ее свойствами: 1. Молекулы
- 57. Изомерия Явление изомерии состоит в том, что могут существовать несколько разных по свойствам веществ, имеющих одинаковый
- 58. Структурная изомерия 1. Изомерия положения сопряженных двойных связей: СН2=СН–СН=СН–СН2–СН3 СН3–СН=СН–СН=СН–СН3 гексадиен-1,3 гексадиен-2,4 2. Изомерия углеродного скелета:
- 60. Скачать презентацию





















 Rates of reaction
Rates of reaction Пластмассалар, пластикалық материалдар
Пластмассалар, пластикалық материалдар Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки
Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки Азот. Аммиак (9 класс)
Азот. Аммиак (9 класс) Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції
Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню
Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii
osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii Ароматические соединения
Ароматические соединения Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Относительная атомная и молекулярная массы
Относительная атомная и молекулярная массы Кислоты. Состав, названия и определение кислот
Кислоты. Состав, названия и определение кислот Introduction to Periodic Table
Introduction to Periodic Table Алкилсульфонаттарды алу және технологиялық сызбанұсқасы
Алкилсульфонаттарды алу және технологиялық сызбанұсқасы Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Етери та естери
Етери та естери Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1)
Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1) Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Вуглеводи. Класифікація вуглеводів
Вуглеводи. Класифікація вуглеводів Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров
Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров Аминокислоты N H2 – C H – C O O H
Аминокислоты N H2 – C H – C O O H Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички
Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички Азотная кислота
Азотная кислота Коррозия металлов. Классификация коррозионных процессов
Коррозия металлов. Классификация коррозионных процессов Подземное хранение газа и жидкости
Подземное хранение газа и жидкости Масса и формулы. Химия 8 класс
Масса и формулы. Химия 8 класс Метал конструкциялық материалдар
Метал конструкциялық материалдар Вуглеводи
Вуглеводи Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ