Содержание
- 2. Растворы играют важную роль в природе, науке и технике. Особую роль на нашей планете играет вода.
- 3. Изучение свойств растворов занимает важное место в современной науке. В химии процессы растворения рассматриваются с позиций
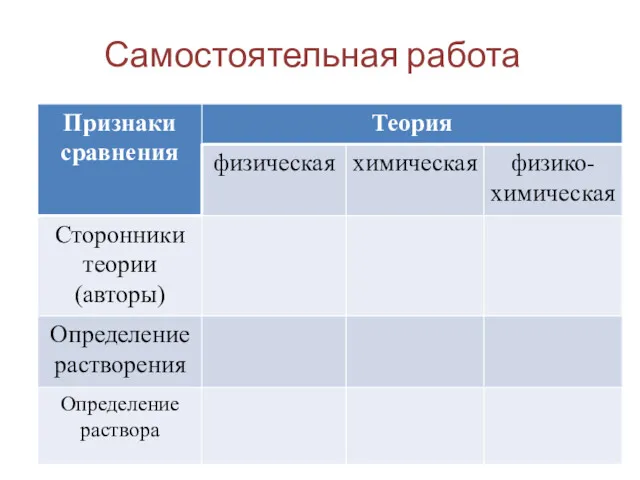
- 4. Самостоятельная работа
- 5. Физическая теория Процесс растворения является процессом диффузии, т.е проникновение растворенного вещества в промежутки между молекулами воды
- 6. Химическая теория Дмитрий Иванович Менделеев Иван Алексеевич Каблуков Процесс растворения – это результат взаимодействия вещества с
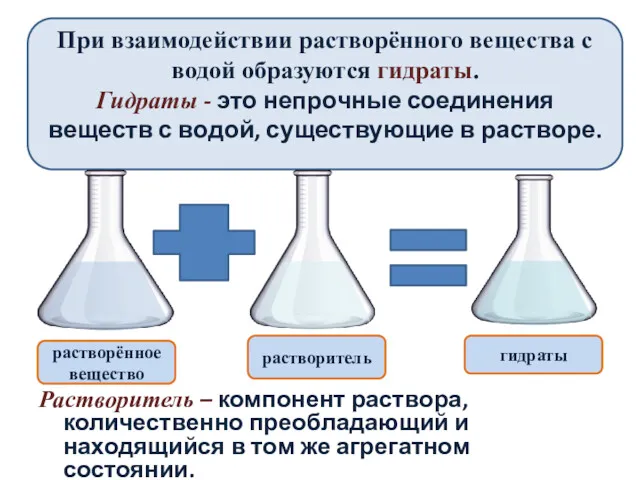
- 7. При взаимодействии растворённого вещества с водой образуются гидраты. Гидраты - это непрочные соединения веществ с водой,
- 8. Физико-химическая теория В настоящее время принята теория, которая объединяет обе точки зрения,- физико-химическая теория растворов. Её
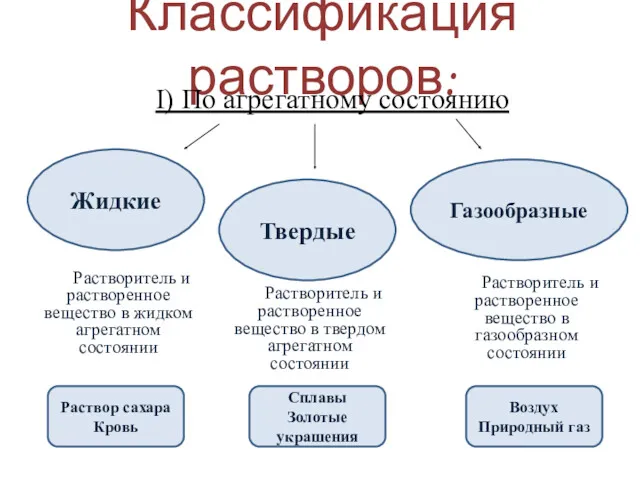
- 9. Классификация растворов: I) По агрегатному состоянию Жидкие Газообразные Твердые Растворитель и растворенное вещество в газообразном состоянии
- 10. От чего зависит растворимость веществ? 2. От природы растворителя От температуры 3. От природы вещества
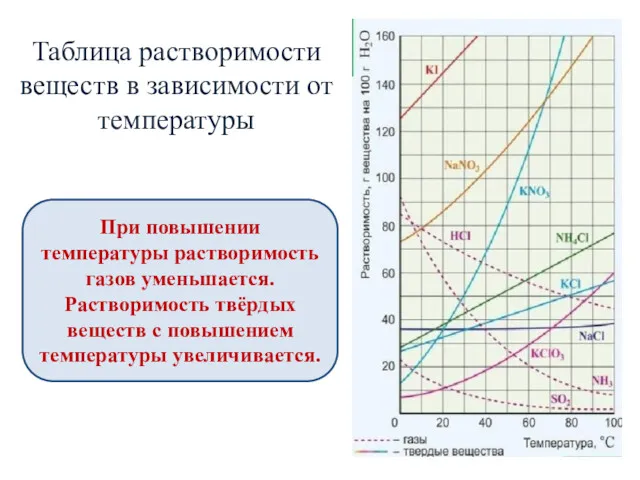
- 11. Таблица растворимости веществ в зависимости от температуры При повышении температуры растворимость газов уменьшается. Растворимость твёрдых веществ
- 12. II) В зависимости от количества растворённого в растворителе вещества Классификация растворов: Насыщенные Ненасыщенные Перенасыщенные Ненасыщенным называют
- 13. В зависимости от способности вещества растворятся в воде, оно может быть: Вещество малорастворимо, если при комнатной
- 14. Таблица растворимости кислот, оснований и солей в воде при комнатной температуре
- 16. Скачать презентацию








 Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Соединения галогенов
Соединения галогенов Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Химическая связь
Химическая связь Массовая доля вещества в растворе
Массовая доля вещества в растворе Визначення іонів лужних і лужноземельних іонів у природних водах
Визначення іонів лужних і лужноземельних іонів у природних водах Уникальная соль (для дошколников)
Уникальная соль (для дошколников) Пищевые добавки
Пищевые добавки Коллигативные свойства растворов
Коллигативные свойства растворов Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7
Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7 Литий. Физические свойства лития
Литий. Физические свойства лития Типы заданий. ЕГЭ №32
Типы заданий. ЕГЭ №32 20230419_izomery
20230419_izomery Растворы и растворители
Растворы и растворители Фосфор и его соединения
Фосфор и его соединения Общая характеристика неметаллов
Общая характеристика неметаллов Простые вещества. Игра Счастливый случай
Простые вещества. Игра Счастливый случай Элемент, имеющий относительную атомную массу
Элемент, имеющий относительную атомную массу Введение в аналитическую химию. Введение в качественный анализ
Введение в аналитическую химию. Введение в качественный анализ Алканы. Гомологи
Алканы. Гомологи Методы разделения и исследования состава нефти и газа
Методы разделения и исследования состава нефти и газа Формальная кинетика. Предмет химической кинетики
Формальная кинетика. Предмет химической кинетики Хром. Элемент под № 24
Хром. Элемент под № 24 Аммиак. Состав вещества
Аммиак. Состав вещества Галогены. Фтор, хлор, бром, йод, астат
Галогены. Фтор, хлор, бром, йод, астат Породообразующие минералы
Породообразующие минералы Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Взрывоопасные грузы
Взрывоопасные грузы