Слайд 2
Спирты
Спирты (алканолы) – это органические вещества, молекулы которых содержат одну или
несколько гидроксильных групп (групп – OH), соединенных с углеводородным радикалом.
Слайд 3

Виды спиртов
Одноатомные спирты, например:
CH3-OH метанол или метиловый спирт,
CH3-CH2-OH этанол
или этиловый спирт.
Двухатомные (гликоли), например:
HO-CH2-CH2-OH этандиол-1,2 или этиленгликоль.
Трехатомные спирты, например:
Пропантриол-1,2,3 или глицерин.
Слайд 4
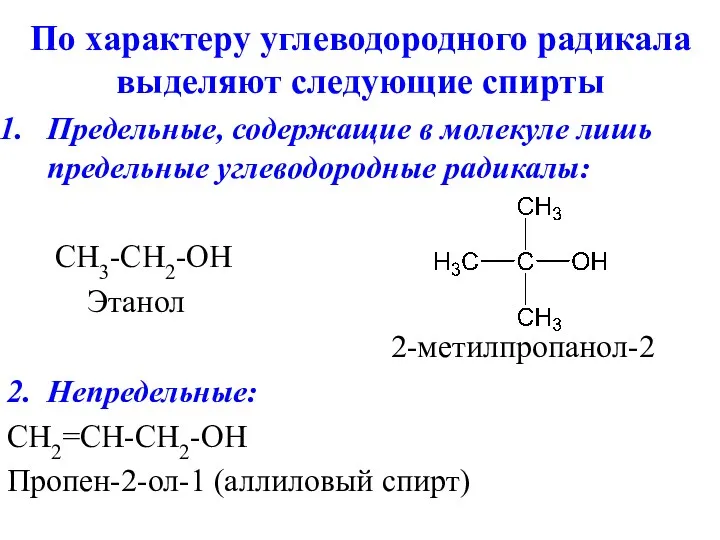
По характеру углеводородного радикала выделяют следующие спирты
Предельные, содержащие в молекуле лишь
предельные углеводородные радикалы:
CH3-CH2-OH
Этанол
2-метилпропанол-2
2. Непредельные:
CH2=CH-CH2-OH
Пропен-2-ол-1 (аллиловый спирт)
Слайд 5

Ароматические
Фенилметанол 2-фенилэтанол
(бензиловый спирт)
Слайд 6
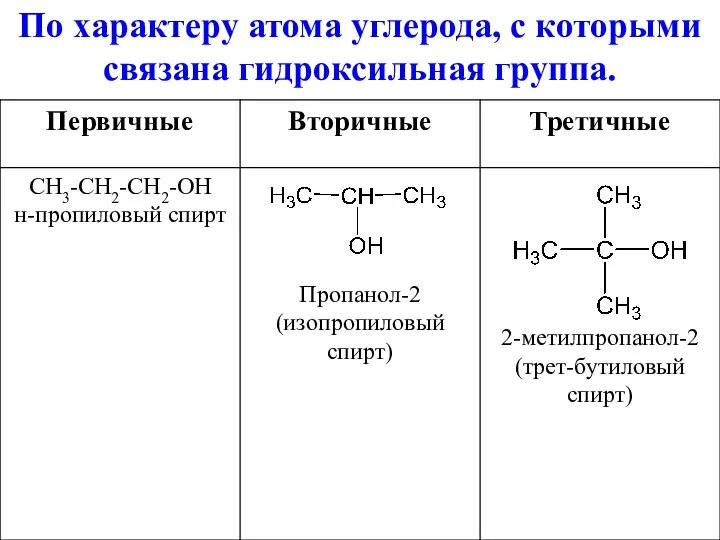
По характеру атома углерода, с которыми связана гидроксильная группа.
Слайд 7
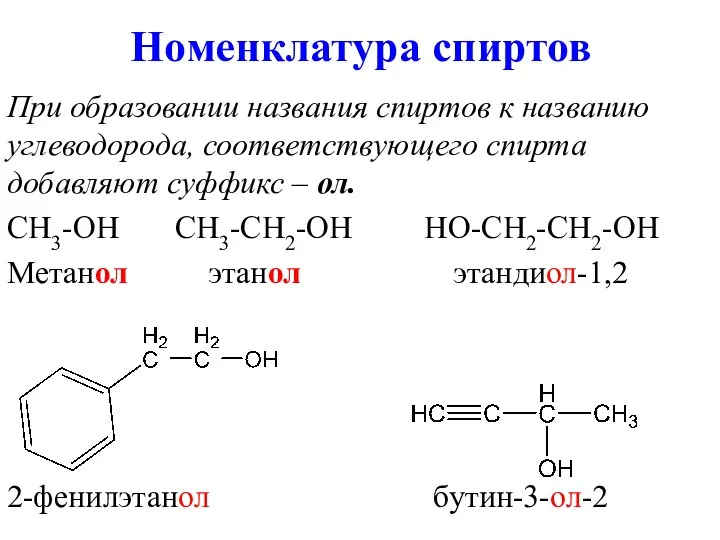
Номенклатура спиртов
При образовании названия спиртов к названию углеводорода, соответствующего спирта добавляют
суффикс – ол.
CH3-OH CH3-CH2-OH HO-CH2-CH2-OH
Метанол этанол этандиол-1,2
2-фенилэтанол бутин-3-ол-2
Слайд 8

Изомерия спиртов
Изомерия положения OH-группы (начиная с С3):
Углеродного скелета (начиная с
С4):
Слайд 9

Изомерия спиртов
Межклассовая изомерия с простыми эфирами:
Слайд 10

Способы получения спиртов
1. Гидролиз галогеналканов.
CH3–Cl + NaOH → CH3–OH + NaCl
+ H2O
2. Гидратация алкенов:
Слайд 11
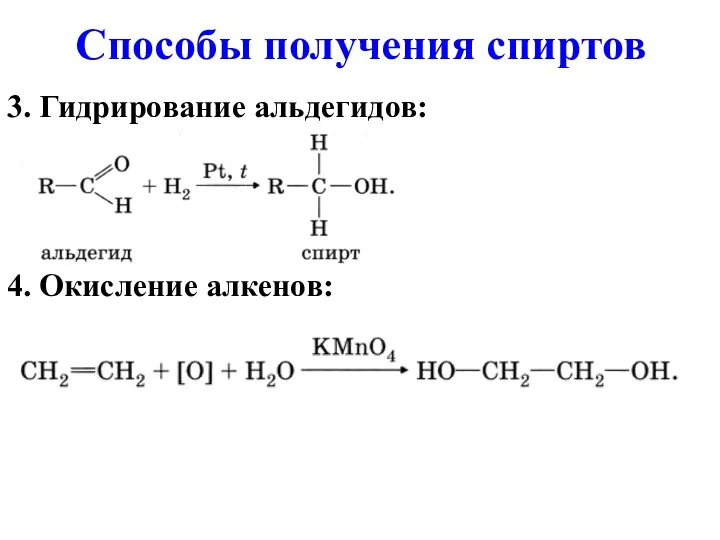
3. Гидрирование альдегидов:
4. Окисление алкенов:
Способы получения спиртов
Слайд 12
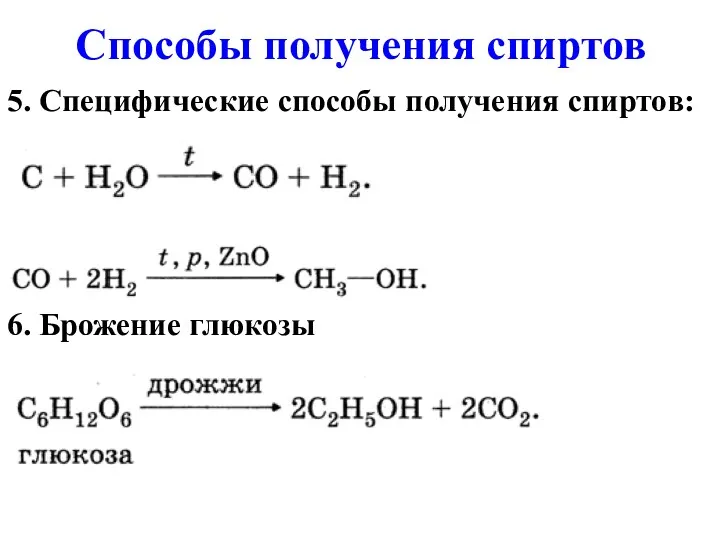
5. Специфические способы получения спиртов:
6. Брожение глюкозы
Способы получения спиртов
Слайд 13

Химические свойства спиртов
1. Взаимодействие спиртов со щелочными и щелочноземельными металлами:
2Na +
2C2H5OH → 2C2H5ONa + H2
2. Взаимодействие спиртов с галогеноводородами:
C2H5OH + HBr → C2H5Br + H2O
3. Межмолекулярная дегидратация спиртов:
H2SO4
CH3OH + HOCH3 → CH3 – O – CH3 + H2O
Слайд 14
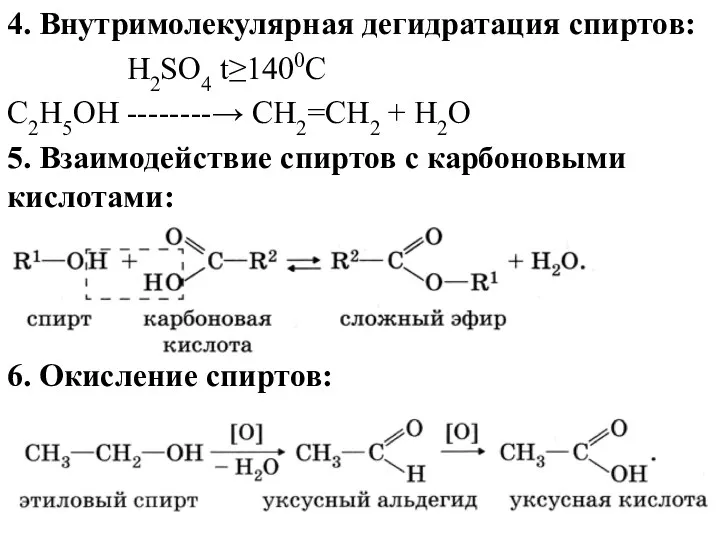
4. Внутримолекулярная дегидратация спиртов:
H2SO4 t≥1400C
С2H5OH --------→ CH2=CH2 + H2O
5. Взаимодействие
спиртов с карбоновыми кислотами:
6. Окисление спиртов:













 Алкадиены, нафтены
Алкадиены, нафтены Аминокислоты
Аминокислоты Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами
Биологически важные пяти- и шестичленные гетероциклы с одним и двумя гетероатомами Серная кислота
Серная кислота Фізичні та хімічні властивості кислот (урок хімії у 8 класі)
Фізичні та хімічні властивості кислот (урок хімії у 8 класі) Типы химических реакций , признаки и условия их протекания
Типы химических реакций , признаки и условия их протекания Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азот
Азот Хімічні властивості кислот
Хімічні властивості кислот Поширення солей у природі
Поширення солей у природі Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия ПЛАСТИК НОВЫЙ
ПЛАСТИК НОВЫЙ Stirring in liquid media
Stirring in liquid media Литий
Литий Липиды (Жиры)
Липиды (Жиры) В чём соль соли
В чём соль соли Классификация химических реакций по различным основаниям. 9 класс
Классификация химических реакций по различным основаниям. 9 класс Технологии получения полимерных нанокомпозитов
Технологии получения полимерных нанокомпозитов Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Правила роботи на уроці
Правила роботи на уроці Задачи на процентную концентрацию
Задачи на процентную концентрацию Углероды. Строение и свойства атомов
Углероды. Строение и свойства атомов Спирт µндіру технологиясы
Спирт µндіру технологиясы Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Основная. Первоначальные представления об органических веществах
Основная. Первоначальные представления об органических веществах Химические свойства серной кислоты
Химические свойства серной кислоты Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Полистирол өндірісі
Полистирол өндірісі