Содержание
- 2. Нахождение в природе К0 → К++282,15 кДж (ΔH 0 = -282,15 кДж); Mg0→ Mg2+ +126,25 кДж
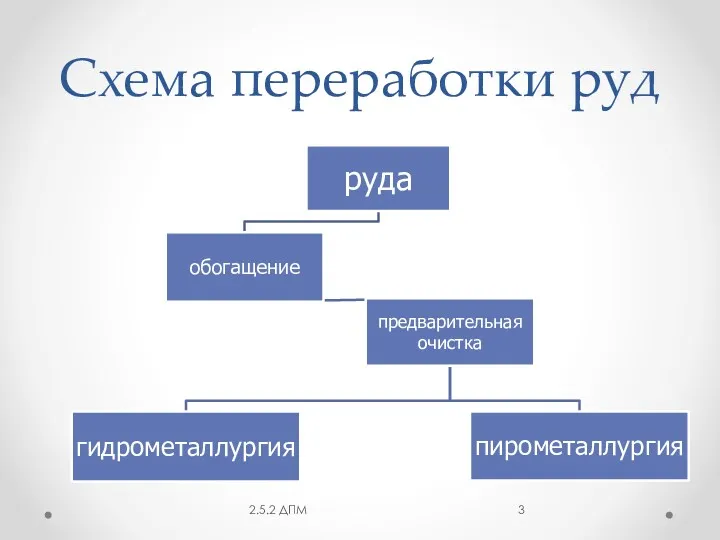
- 3. Схема переработки руд 2.5.2 ДПМ
- 4. Пирометаллургия а) восстановление из оксидов металлов: ZnO (тв) + С (тв) →СО (г) + Zn (г)
- 5. б) восстановление из сульфидов: 2ZnS + 3O2 → 2ZnO + 2SO2 (обжиг) ZnO + C →
- 6. Электрометаллургия Восстановление металла происходит при электролизе на катоде. Электролизом водных растворов могут быть получены лишь сравнительно
- 7. Получение алюминия Al - самый распространенный на Земле металл: 8.5 массовых процентов в земной коре Основные
- 8. Гидрометаллургия Извлечение металлов из руд с помощью водных растворов тех или иных реагентов: (CuOH)2CO3 + H2SO4=2CuSO4
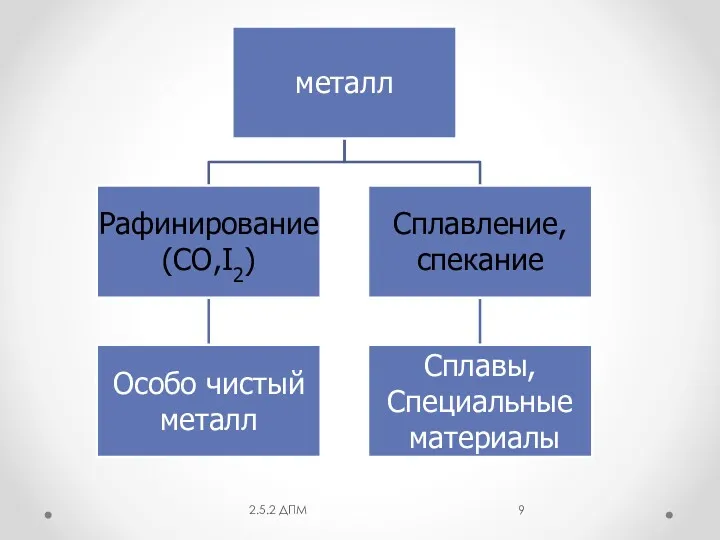
- 9. 2.5.2 ДПМ
- 10. Сплавы- см. 2.5.1 ДПМ Константан, нихром,ферронихром, с эффектом «памяти» и т.д. «Сверхпластичные» Композиты, керметы Свойства сплавов
- 11. Очистка металлов Полупроводниковая электроника, ядерная энергетика предъявляют высокие требования к чистоте металла. Массовая доля меди в
- 12. Постоянные и случайные примеси В «чистом» железе при спектральном анализе было обнаружено 27 химических элементов. Примеси
- 13. Степени очистки веществ В технике вещества по степени очистки делят на следующие четыре класса: Чистые —
- 14. Классы чистоты Чистоту вещества иногда выражают числом «девяток» после запятой. Например, три девятки означают 99,999% основного
- 15. Металлы высокой чистоты классифицируются: 2.5.2 ДПМ Для веществ классов группы А возможно прямое химическое определение содержания
- 16. Рафинирование : Физические способы - плавка в вакууме или в атмосфере инертного газа: Дуговая плавка Электроннолучевая
- 17. Зонная плавка 2.5.2 ДПМ Слиток металла 2 помещают в контейнер-лодочку 1, который устанавливается в кварцевой трубе
- 18. Рафинирование : Химические методы- избирательное взаимодействие очищаемого вещества, либо примеси с вводимыми реагентами. Электролиз расплавов галогенидов
- 19. Титан, очищенный методом иодидного рафинирования 2.5.2 ДПМ
- 20. Схема получения германия полупроводниковой чистоты: 2.5.2 ДПМ
- 21. 2.5.2 ДПМ
- 23. Скачать презентацию


















 Теплота згоряння. Температура горіння
Теплота згоряння. Температура горіння Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Лекция 6. Желтые пигменты
Лекция 6. Желтые пигменты Полимеры. Пластмассы. Волокна
Полимеры. Пластмассы. Волокна Електролітична дисоціація. Гідроліз солей
Електролітична дисоціація. Гідроліз солей Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ
Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ Зерттеу әдістері
Зерттеу әдістері Хлороводород..Соляная кислота
Хлороводород..Соляная кислота Фазовое равновесие
Фазовое равновесие Сероводород
Сероводород Франций (Francium)
Франций (Francium) Роль хімії у суспільстві
Роль хімії у суспільстві Кислородсодержащие органические вещества. Фенолы
Кислородсодержащие органические вещества. Фенолы Разнообразие неметаллов
Разнообразие неметаллов Минералогия с основами кристаллографии
Минералогия с основами кристаллографии Фізичні властивості та хімічний склад природних вод
Фізичні властивості та хімічний склад природних вод Припекание взаимно растворимых твердых тел
Припекание взаимно растворимых твердых тел Металл цирконий (ZR)
Металл цирконий (ZR) Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Химия в повседневной жизни человека
Химия в повседневной жизни человека Alyuminiy_ego_soedinenia
Alyuminiy_ego_soedinenia Углерод. Общая характеристика элементов подгруппы углерода
Углерод. Общая характеристика элементов подгруппы углерода Физические и химические свойства алкенов
Физические и химические свойства алкенов Тип соли. Задачи к вопросу 34 по спецификации ЕГЭ-2019
Тип соли. Задачи к вопросу 34 по спецификации ЕГЭ-2019 Особенности органических веществ. Теория химического строения А.М.Бутлерова
Особенности органических веществ. Теория химического строения А.М.Бутлерова Химия нефти и газа
Химия нефти и газа Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Кислоты, их классификация и свойства
Кислоты, их классификация и свойства