Содержание
- 2. Тема 3. Строение вещества Преподаватель Вера Дмитриевна Колобова Киров, 2020 г ККМИ им. И. В. Казенина
- 3. Переписать всё (если иное не указано) с каждого слайда и осмыслить
- 4. 1. Природа химической связи Химическую связь обусловливает электростатическое взаимодействие между отрицательно заряженными электронами и положительно заряженными
- 5. Почему атомы объединяются в молекулы? Молекулярное состояние наиболее устойчивое, чем атомное. То есть оно, во-первых, энергетически
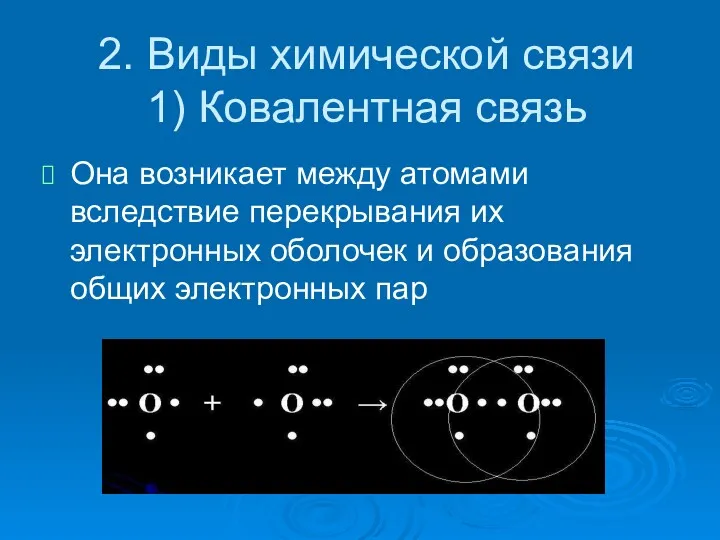
- 6. 2. Виды химической связи 1) Ковалентная связь Она возникает между атомами вследствие перекрывания их электронных оболочек
- 7. ПРОЧИТАТЬ Характерные свойства 1. Направленность связи обусловлена молекулярным строением вещества и геометрической формы их молекулы. 2.
- 8. Ковалентная неполярная связь Такую связь образуют атомы одного и того же химического элемента - неметалла (например,
- 9. ПРОЧИТАТЬ И ПОНЯТЬ Механизм образования ковалентной неполярной связи: Каждый атом неметалла отдает в общее пользование другому
- 10. Ковалентная полярная связь Такую связь образуют атомы разных неметаллов, отличающихся по значения электроотрицательности (например, HCl, H2O)
- 11. ПРОЧИТАТЬ И ПОНЯТЬ Механизм образования ковалентной полярной связи: Каждый атом неметалла отдает в общее пользование другому
- 12. Вещества с ковалентной связью могут быть твёрдыми, жидкими и газообразными с атомной или молекулярной решётками и
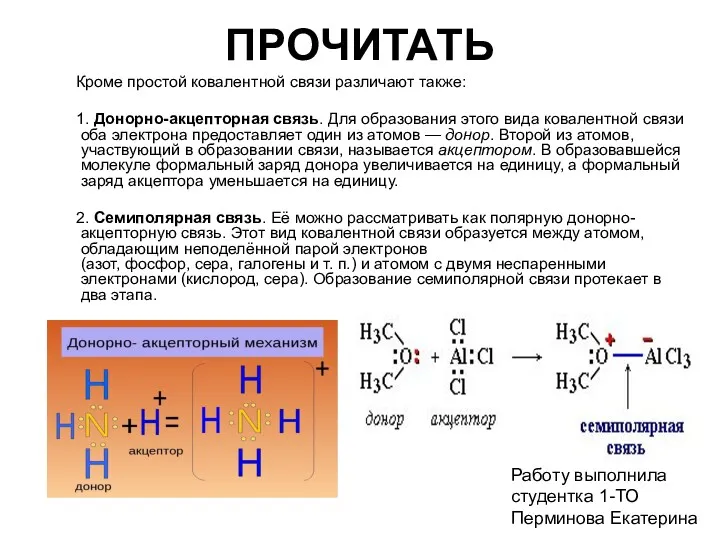
- 13. ПРОЧИТАТЬ Кроме простой ковалентной связи различают также: 1. Донорно-акцепторная связь. Для образования этого вида ковалентной связи
- 14. Эта химическая связь образуется между ионами по электростатическому механизму Ионные соединения образуются атомами элементов, резко отличающихся
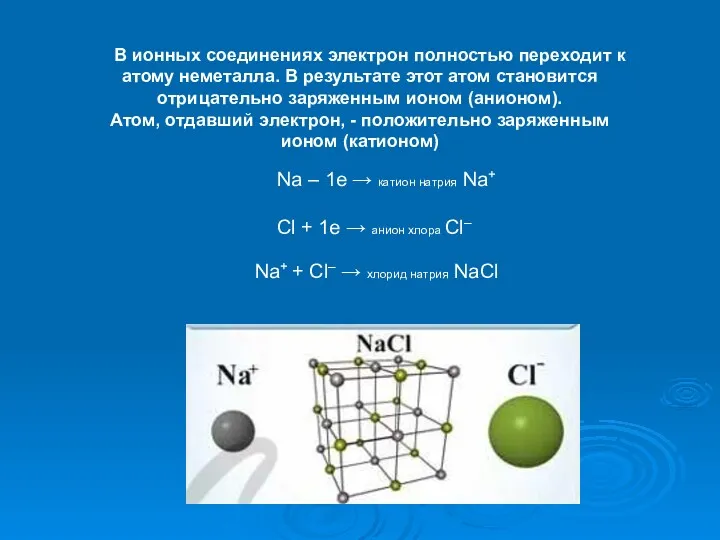
- 15. В ионных соединениях электрон полностью переходит к атому неметалла. В результате этот атом становится отрицательно заряженным
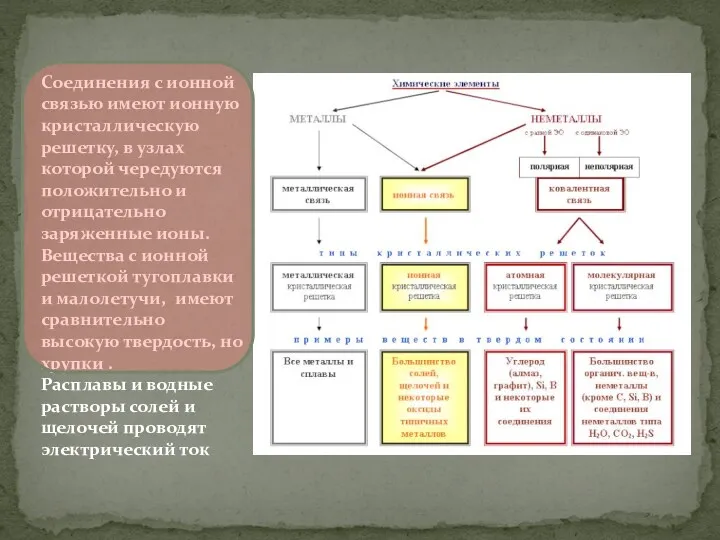
- 16. Соединения с ионным типом связи – это твёрдые кристаллические вещества с ионной кристаллической решёткой и они
- 17. Это связь в металлах При сближении, а значит и при перекрывании атомных оболочек соседних атомов электроны
- 18. ПРОЧИТАТЬ Характеристики металлической связи Ненаправленность (изотропность) – внутри кристалла движение электронов происходит в любом направлении, они
- 19. Металлическая связь не закреплена между отдельными атомами, как ковалентная и ионная. Она определяет общие свойства металлов:
- 20. ПРОЧИТАТЬ Металлическая связь характерна для чистых металлов и для смесей различных металлов — сплавов (бронза, сталь,
- 21. 2. Виды химической связи 4) Водородная связь Далее переписать то, что выделено рамкой:
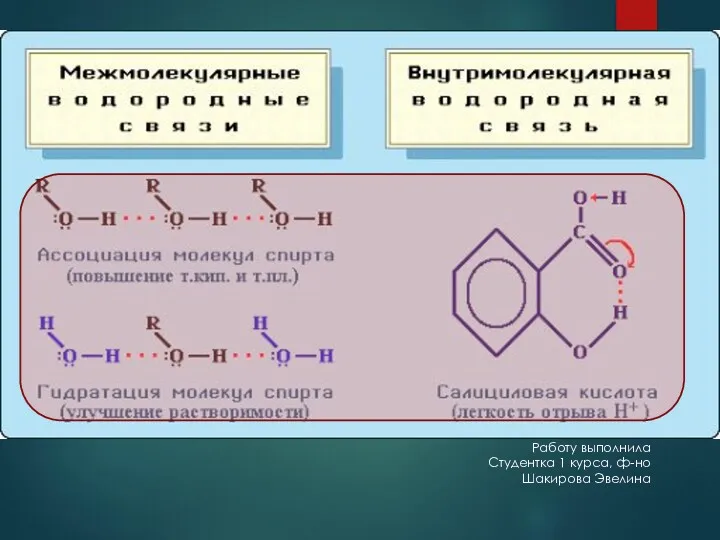
- 22. Водородная связь – это связь, образующаяся между атомом водорода одной молекулы и другим электроотрицательным атомом другой
- 23. Свойства и типы водородных связей Ковалентная и водородная связь сильно различаются по силе. Водородная значительно слабее,
- 24. Работу выполнила Студентка 1 курса, ф-но Шакирова Эвелина
- 25. Подготовлено студентом ККМИ 1ф-но Зверевым Денисом 3. Взаимодействие кристаллических решеток веществ с различными типами химической связи
- 26. Строение кристаллов и типы кристаллических решеток Кристаллами называются твёрдые вещества, частицы которых образуют трёхмерную периодическую пространственную
- 27. Соединения с ковалентной связью имеют два типа кристаллических решеток: атомные и молекулярные. В атомной кристаллической решетке
- 28. Соединения с ионной связью имеют ионную кристаллическую решетку, в узлах которой чередуются положительно и отрицательно заряженные
- 29. Самостоятельная работа на оценку на отдельном листочке
- 31. Скачать презентацию























 Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Соединения щелочных металлов
Соединения щелочных металлов Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ
Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ Відносна молекулярна маса речовини, її обчислення за хімічною формулою
Відносна молекулярна маса речовини, її обчислення за хімічною формулою Алканы
Алканы Химические свойства основных классов неорганических веществ
Химические свойства основных классов неорганических веществ Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек
Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек Углеводородное сырье: способы переработки
Углеводородное сырье: способы переработки Предельные углеводороды
Предельные углеводороды Комплесные соединения
Комплесные соединения Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты
Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу
Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер
Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер Неметаллические материалы, используемые в машино- и приборостроении
Неметаллические материалы, используемые в машино- и приборостроении Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Алюминий и его соединения
Алюминий и его соединения Метаболизм нуклеиновых кислот
Метаболизм нуклеиновых кислот Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Формы минералов и их агрегатов
Формы минералов и их агрегатов Химические свойства металлов
Химические свойства металлов Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Угарный газ
Угарный газ Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Адсорбция. Разделение однородных и неоднородных смесей
Адсорбция. Разделение однородных и неоднородных смесей Ферум та його сполуки
Ферум та його сполуки Аминокислоты. Белки
Аминокислоты. Белки